- ЛчТэәЕЈә44628065XB/2017-1221534
- ·ўІј»ъ№№ЈәОАЙъәНјЖ»®ЙъУэҫЦ
- №«ҝӘ·¶О§ЈәИ«Іҝ№«ҝӘ
- ЙъіЙИХЖЪЈә2017-05-05
- №«ҝӘИХЖЪЈә2017-05-05
- №«ҝӘ·ҪКҪЈәХюё®НшХҫ
»ӘОА·ў[2017]33әЕ
»ӘИЭПШОАЙъәНјЖ»®ЙъУэҫЦ
№ШУЪУЎ·ў»ӘИЭПШФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨ
ҙ«ІҘ№ӨЧчКөК©·Ҫ°ёЈЁ2017Дк°жЈ©өД
НЁ ЦӘ
ёчТҪБЖОАЙъ»ъ№№Јә
ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧчКЗ№ъјТЦШҙ󹫹ІОАЙъПоДҝЈ¬КЗҙ«ИҫІЎЧЫәП·АЦОөДЦШТӘЧйіЙІҝ·ЦЈ¬¶ФҪөөНФРІъёҫәН5ЛкТФПВ¶щНҜЛАНцВКЈ¬МбёЯіцЙъИЛҝЪЛШЦКЈ¬ҙЩҪшёҫЕ®¶щНҜҪЎҝөҫЯУРЦШТӘТвТеЎЈёщҫЭЎ¶әюДПКЎОАЙъәНјЖЙъОҜ№ШУЪУЎ·ўәюДПКЎФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧчКөК©·Ҫ°ёЈЁ2017Дк°жЈ©Ў·(ПжОАёҫУЧ·ў[2017]4әЕ)әНКРОАјЖОҜөД№ӨЧчТӘЗуЈ¬ПЦҪ«Ў¶»ӘИЭПШФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧчКөК©·Ҫ°ёЈЁ2017Дк°жЈ©Ў·УиТФУЎ·ўЈ¬ЗлИПХж№бі№ЦҙРРЎЈ
ёҪјюЈә1Ўў»ӘИЭПШФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧчКөК©·Ҫ°ёЈЁ2017Дк°жЈ©
2Ўў»ӘИЭПШФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧч¶ҪІйПёФт
»ӘИЭПШОАЙъәНјЖ»®ЙъУэҫЦ
2017Дк4ФВ27ИХ
»ӘИЭПШФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧч
КөК©·Ҫ°ёЈЁ2017Дк°жЈ©
ОӘҪшТ»ІҪ№ж·¶ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧчЈ¬И«ГжВдКөЧЫәПёЙФӨҙлК©Ј¬КөПЦЧоҙуПЮ¶ИөШјхЙЩТтДёУӨҙ«ІҘФміЙөД¶щНҜёРИҫЈ¬ёщҫЭЎ¶әюДПКЎФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧчКөК©·Ҫ°ёЈЁ2017Дк°жЈ©Ў·(ПжОАёҫУЧ·ў[2017]4әЕ)Па№ШТӘЗуЈ¬ҪбәПОТПШКөјКЈ¬ЦЖ¶ЁұҫКөК©·Ҫ°ёЎЈ
Т»Ўў№ӨЧчДҝұк
ЈЁТ»Ј©ЧЬДҝұкЎЈҪЁБўХюё®ЦчөјЎўІҝГЕЕдәПЎўЧЁјТЦ§іЕЎўИәЦЪІОУлөД№ӨЧч»ъЦЖЈ¬ОӘФРІъёҫј°ЛщЙъ¶щНҜМṩФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘЧЫәПёЙФӨ·юОсЈ¬ЧоҙуіМ¶ИөШјхЙЩДёУӨҙ«ІҘЈ¬ҙпөҪПыіэДёУӨҙ«ІҘ№ъјКДҝұкЈ¬ҪөөН°¬ЧМІЎЎўГ·¶ҫәНТТёО¶ФёҫЕ®¶щНҜөДУ°ПмЈ¬ҪшТ»ІҪМбёЯёҫЕ®¶щНҜЙъ»оЦКБҝәНҪЎҝөЛ®ЖҪЎЈ
ЈЁ¶юЈ©ҫЯМеДҝұкЎЈЦБ2020ДкөЧЈ¬КөПЦТФПВДҝұкЈә
1Ј®ФРІъёҫ°¬ЧМІЎЎўГ·¶ҫәНТТёОјмІвВКҙп95%ТФЙПЈ¬ФРФзЦРЖЪјмІвВКҙп90%ТФЙПЎЈ
2Ј®°¬ЧМІЎёРИҫФРІъёҫҝ№°¬ЧМІЎ¶ҫУГТ©ВКҙп95%ТФЙПЈ¬ЛщЙъУӨ¶щҝ№°¬ЧМІЎ¶ҫУГТ©ВКҙп95%ТФЙПЎЈ
3Ј®Г·¶ҫёРИҫФРІъёҫГ·¶ҫЦОБЖВКҙп95%ТФЙПЈ¬№ж·¶ЦОБЖВКҙп80%ТФЙПЈ¬ЛщЙъ¶щНҜФӨ·АРФЦОБЖВКҙп95%ТФЙПЎЈ
4Ј®ТТёОёРИҫФРІъёҫЛщЙъРВЙъ¶щТТёОГвТЯЗтө°°ЧЧўЙдВКҙп95%ТФЙПЎЈ
5Ј®°¬ЧМІЎДёУӨҙ«ІҘВКФЪ·ЗДёИйО№СшИЛИәЦРПВҪөЦБ2%ТФПВЈ¬ФЪДёИйО№СшИЛИәЦРПВҪөЦБ5%ТФПВЎЈ
6Ј®ПИМмГ·¶ҫұЁёж·ўІЎВКПВҪөЦБ15/10Нт»оІъТФПВЎЈ
¶юЎў№ӨЧчДЪИЭ
ҪбәПФРІъЖЪұЈҪЎУл¶щНҜұЈҪЎ·юОсЈ¬ОӘЛщУРФРІъёҫј°ЛщЙъ¶щНҜМṩȫГжЎўХыәПөДФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ·юОсЈ¬ХыәП·юОсБчіМјыёҪјю1ЎЈЦчТӘ№ӨЧчДЪИЭИзПВЈә
ЈЁТ»Ј©ҪЎҝөҪМУэј°ҪЎҝөҙЩҪшЎЈПШОАЙъјЖЙъРРХюІҝГЕУлёчПа№ШІҝГЕГЬЗРәПЧчЈ¬·ў»УІҝГЕУЕКЖЈ¬Іўід·ЦАыУГҪМУэЎўёҫБӘЎўјЖ»®ЙъУэРӯ»бЎўҪЎҝөҪМУэРыҙ«ЦРРДөИЖҪМЁҝӘХ№РОКҪ¶аСщөДҪЎҝөҪМУэ»о¶ҜЎЈёчТҪБЖОАЙъ»ъ№№УҰөұҪбәП»йЗ°ұЈҪЎЎўФРЗ°ұЈҪЎЎўФРІъЖЪұЈҪЎЎўЗаЙЩДкұЈҪЎЎўРФІЎ·АЦОЎўЙзЗшОАЙъ·юОсөИіЈ№жТҪБЖұЈҪЎ·юОсҝӘХ№ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘөДҙуЦЪҪЎҝөҪМУэәНЧЙСҜЦёөјЈ¬МбёЯУэБдёҫЕ®ј°ЖдјТНҘЈ¬МШұрКЗФРІъёҫ¶ФФӨ·АДёУӨҙ«ІҘөДИПЦӘЈ¬ҙЩҪшҪЎҝөРРОӘЎЈЦЖЧчРыҙ«АёЎўХЕМщРыҙ«»ӯЈ¬ҫЩ°мУРХл¶ФРФөДҪІЧщЈ¬ЧйЦҜ¶аЦЦРОКҪөД»о¶ҜЈ¬АыУГ№гІҘәНөзКУЧЁАёЎўС§РЈҝОіМЎўҪЪјЩИХЧЁМвРыҙ«ЎўЧЙСҜөИ»о¶ҜЈ¬ҝӘХ№ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘЦӘК¶өДРыҙ«Ј¬МбёЯИәЦЪөД·АЦОЦӘК¶Л®ЖҪЎЈ
ЈЁ¶юЈ©ФРІъёҫјмІвУлЧЙСҜ·юОсЎЈ
1.јмІвЗ°ЧЙСҜЎЈёчТҪБЖОАЙъ»ъ№№ОӘЛщУРФРІъёҫЈЁ°ьАЁБч¶ҜИЛҝЪФРІъёҫЈ©ҪшРРФРІъЖЪұЈҪЎ·юОсКұЈ¬УҰЦч¶ҜМṩГв·СјмІвөД»ЭГсХюІЯј°јмІвЗ°ЧЙСҜөИ·юОсЎЈТ»КЗёжЦӘФРІъёҫј°ЖдјТНҘ°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘөДОЈәҰЈ¬ІўМṩФӨ·АДёУӨҙ«ІҘөДРЕПўЎЈ¶юКЗНЁ№эЧЙСҜ·юОс·ўПЦЗұФЪөДёРИҫХЯЎЈИэКЗҙЩҪшФРІъёҫФЪіЈ№жФРЖЪұЈҪЎәНТҪБЖјмІйЦРҪУКЬ°¬ЧМІЎЎўГ·¶ҫәНТТёОГв·СјмІвЎЈ
2.°¬ЧМІЎЎўГ·¶ҫәНТТёОөДГв·СјмІвЎЈ
ЈЁ1Ј©°¬ЧМІЎөДјмІвЎЈёчТҪБЖОАЙъ»ъ№№ФЪФРІъёҫіхҙОҪУКЬФРІъЖЪұЈҪЎКұЈ¬УҰёГЦч¶ҜМṩ1ҙОГв·С°¬ЧМІЎІЎ¶ҫҝ№МеЙёІй·юОсЎЈ
ўЩФРЖЪјмІвЎЈФРІъёҫөД°¬ЧМІЎІЎ¶ҫҝ№МејмІвЗҝөчФРФзЖЪјмІвЈ¬ҙпөҪ№ж·¶ЦОБЖЈ¬МбёЯДёУӨЧи¶ПР§№ыЎЈУЙПа№ШТҪОсИЛФұОӘЖдМṩјмІвЗ°әуөДЧЙСҜЈЁФРЖЪ°¬ЧМІЎјмІвј°·юОсБчіМјыёҪјю2-Нј2Ј©ЎЈ¶ФФРЗ°»тФРФзЖЪТСҪшРР°¬ЧМІЎІЎ¶ҫҝ№МејмІвөДФРёҫЈ¬Из·ЦГдЗ°јмІвјдёфКұјдТСі¬№э6ёцФВЈ¬ІъЗ°УҰФЩҙОјмІвЎЈ
ўЪІъКұјмІвЎЈІъКұјмІвЧчОӘФРЖЪОҙҪУКЬјмІвөДІ№ідКЦ¶ОЎЈФРЖЪОҙҪУКЬ°¬ЧМІЎјмІвөДБЩІъІъёҫЈ¬УҰУЙЦъІъ»ъ№№ІъҝЖТҪКҰҝӘҫЯ»ҜСйөҘјұХпЛНјмЈ¬јмСйҝЖН¬КұІЙУГБҪЦЦІ»Н¬өДҝмЛЩјмІвКФјБҪшРРјмІвЈ¬ј°КұҪ«јмІвҪб№ы·ҙАЎЦБІъҝЖЎЈОЮјмІвМхјюөД»ъ№№Ј¬УҰМоРҙ°¬ЧМІЎІЎ¶ҫҝ№МејмІвЙкЗлөҘЈ¬ҫӯ1ГыјмСйИЛФұәН1ГыТҪЙъЗ©ГыЈ¬Ҫ«СӘЗеұкұҫУЪІЙјҜ4РЎКұДЪЛНөҪУРЧКЦКөД»ъ№№јмІвЈ¬ҪУКХұкұҫјмІвјұХпјмІвЈ¬Іўј°КұҪ«јмІвҪб№ы·ҙАЎЦБЛНјм»ъ№№ІъҝЖ(ІъКұ°¬ЧМІЎјмІвј°·юОсБчіМјыёҪјю2-Нј3Ј©ЎЈ
ЈЁ2Ј©Г·¶ҫөДјмІвЎЈёчТҪБЖОАЙъ»ъ№№ФЪФРІъёҫіхҙОҪУКЬФРІъЖЪұЈҪЎКұЈ¬УҰЦч¶ҜМṩ1ҙОГв·СГ·¶ҫЙёІй·юОсЎЈМṩФРІъЖЪұЈҪЎ·юОсТҪБЖОАЙъ»ъ№№ТӘҫЯұё·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйәНГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйөДДЬБҰЈ¬ФӯФтЙПКЧСЎГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйҪшРРЙёІйЈ¬ЙёІйҪб№ыіКСфРФ·ҙУҰХЯЈ¬УҰФЪұҫ»ъ№№БўјҙУГН¬Т»ұкұҫІЙУГБнТ»АајмІв·Ҫ·ЁҪшРРёҙјмЈ¬И·¶ЁЖдКЗ·сОӘГ·¶ҫёРИҫЎЈЈЁФРІъёҫГ·¶ҫјмІвј°·юОсБчіМПкјыёҪјю2-Нј4Ј©ЎЈ
ЈЁ3Ј©ТТёОөДјмІвЎЈёчј¶ТҪБЖОАЙъ»ъ№№ФЪФРІъёҫіхҙОҪУКЬФРІъЖЪұЈҪЎКұЈ¬УҰЦч¶ҜМṩ1ҙОГв·СТТёОұнГжҝ№ФӯјмІв·юОсЎЈјмІвҪб№ыСфРФЈ¬јМ¶шҪшРРТТёОІЎ¶ҫёРИҫСӘЗеС§ұкЦҫОп(БҪ¶Ф°лЈ©өИПа№ШјмІвЈЁФРІъёҫТТёОјмІвј°·юОсБчіМПкјыёҪјю2-Нј5Ј©ЎЈ
ОӘВдКөКЧХпјмІвЦЖ¶ИЈ¬ұЈХПЛщУРФРІъёҫФЪФРФзЖЪ¶јДЬөГөҪГв·СјмІвЈ¬І»ҫЯұёјмІвДЬБҰөДТҪБЖОАЙъ»ъ№№УҰЙиБўІЙСӘөгЈ¬°ҙХХПа№ШТӘЗуҪшРРҙўҙжәНЧӘФЛЈ¬ЛНЦБПҪЗшДЪЦё¶ЁөД»ъ№№ҪшРРјмІвЎЈ
3.јмІвәуЧЙСҜЎЈ
ЈЁ1Ј©ТхРФҪб№ыЧЙСҜЎЈ»йЗ°ЎўФРЗ°ұЈҪЎИЛИәәНФРІъёҫјмІвҪб№ыОӘТхРФЈ¬УЙКЧХпТҪОсИЛФұҪшРРТхРФҪб№ыёжЦӘЈ¬°пЦъЖдБЛҪвФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОёРИҫөДЦШТӘРЕПўЈ¬К№ЖдЧФҫхөШІЙИЎФӨ·АҙлК©Ј¬ёДұдёЯОЈРРОӘЈ¬ұЬГвёРИҫЎЈҝЙТФІЙУГГж¶ФГжЎўКйГжёжЦӘөИ·ҪКҪҪшРРЧЙСҜёжЦӘЎЈ
ЈЁ2Ј©СфРФҪб№ыЧЙСҜЎЈ
ўЩ°¬ЧМІЎСфРФҪб№ыЧЙСҜЎЈЙёІйСфРФҪб№ыөДЧЙСҜЎЈУЙКЧХпТҪОсИЛФұМṩЧЙСҜ·юОсЈ¬ТӘЧсСӯұЈГЬФӯФтЈ¬ҪвКНЙёІйСфРФҪб№ыЈ¬ёжЦӘРиТӘҪшТ»ІҪЧцІ№ідКөСйЈ¬ДёУӨЧи¶ПөДУРР§ҙлК©өИЦШТӘРЕПўЎЈ
И·ЦӨСфРФҪб№ыЧЙСҜЎЈУЙКЧХпТҪОсИЛФұМṩЧЙСҜ·юОсЈ¬ЧсСӯұЈГЬЎў№Ш°®өДФӯФтЈ¬¶ФИ·ЦӨКөСйҪб№ыОӘСфРФөД»йЗ°ЎўФРЗ°ұЈҪЎИЛИәТӘіхІҪҪвКНСфРФҪб№ыЈ¬Мṩ°¬ЧМІЎ·АЦОЎў°ІИ«РФРРОӘөИПа№ШРЕПўЈ¬ІўЧӘҪйЦБПҪЗшДЪјІІЎФӨ·АҝШЦЖ»ъ№№МṩПа№Ш·юОсЎЈ¶ФИ·ЦӨҪб№ыОӘСфРФөДФРІъёҫТӘМṩСфРФёжЦӘЧЙСҜ·юОсЈ¬ЦШөгМṩЦӘЗйСЎФсИСЙпҪбҫЦЈ¬ДёУӨ№ж·¶·юУГҝ№ІЎ¶ҫТ©ОпЈ¬ФЪ·юУГ№эіМЦРРиТӘҪшРРПа№ШјмІвЎўЧЎФә·ЦГдЎў°ІИ«ЦъІъЈ¬ЛщЙъ¶щНҜИЛ№ӨО№СшЎў¶щНҜ°¬ЧМІЎёРИҫФзЖЪХп¶ПәН¶щНҜЛж·ГЎўЕдЕј/РФ°йјмІвөИЦШТӘРЕПўЎЈ
ўЪГ·¶ҫјмІвСфРФҪб№ыЧЙСҜЎЈКөРРКЧХпёәФрЦЖЈ¬УЙКЧХпТҪОсИЛФұМṩЧЙСҜ·юОсЈ¬ЧсСӯұЈГЬЎў№Ш°®өДФӯФтЈ¬¶ФГ·¶ҫёРИҫФРІъёҫТӘМṩ№ж·¶»ҜЦОБЖЎўЧЎФә·ЦГдЎў°ІИ«ЦъІъЎўЛщЙъ¶щНҜФӨ·АРФЦОБЖәНЛж·ГөИЦШТӘРЕПўЎЈ
ўЫТТёОјмІвСфРФҪб№ыЧЙСҜЎЈКөРРКЧХпёәФрЦЖ,УЙКЧХпТҪОсИЛФұМṩЧЙСҜ·юОсЈ¬ЧсСӯұЈГЬЎў№Ш°®өДФӯФтЈ¬МṩФРІъЖЪұЈҪЎЎўФРЖЪРиТӘҪшРРТТёОІЎ¶ҫФШБҝјмІвЈ¬ұШТӘКұРиТӘЧӘёОІЎҝЖҪшТ»ІҪ№ж·¶ЦОБЖЎўЧЎФә·ЦГдЎў°ІИ«ЦъІъәНЛщЙъ¶щНҜФЪіцЙъәуҫЎФзЧўЙдТТёОГвТЯЗтө°°ЧәНҪУЦЦТТёОТЯГзөИЦШТӘРЕПўЎЈ
ФРІъёҫ°¬ЧМІЎЎўГ·¶ҫәНТТёОјмІв·юОсјјКхТӘөгјыёҪјю2ЎЈ
ЈЁИэЈ©ёРИҫФРІъёҫј°ЛщЙъ¶щНҜөДұЈҪЎ·юОсЎЈ
1.ёРИҫФРІъёҫұЈҪЎЎЈ
ЈЁ1Ј©°¬ЧМІЎёРИҫФРІъёҫұЈҪЎЎЈёчТҪБЖОАЙъ»ъ№№УҰөұ¶ФёРИҫФРІъёҫКөРРКЧХпёәФрЦЖЈ¬І»өГТФИОәОАнУЙҫЬҫшәННЖЪГ°¬ЧМІЎёРИҫФРІъёҫҫНХпЈ¬Ҫ«ЖдДЙИлёЯОЈ№ЬАнәН°¬ЧМІЎ·АЦОМеПөҪшРРЧЫәП№ЬАнЎЈ
ёчТҪБЖОАЙъ»ъ№№ОӘёРИҫФРІъёҫМṩФРІъЖЪұЈҪЎ·юОсЈ¬°ьАЁІЙИЎ°ІИ«РФРРОӘЦёөјЎўПа№ШёРИҫЦўЧҙәНМеХчөДјаІвЎўУӘСшЦ§іЦЎўРДАнЦ§іЦөИ·юОсЎЈОӘЧФФёСЎФсЦХЦ№ИСЙпөДёРИҫФРІъёҫМṩ°ІИ«өДЦХЦ№ИСЙп·юОсЎЈОӘјМРшИСЙпөД°¬ЧМІЎёРИҫФРІъёҫМṩ°ІИ«өДЦъІъ·юОсЎЈҫЎБҝұЬГвҝЙДЬФцјУ°¬ЧМІЎДёУӨҙ«ІҘОЈПХөД»бТхІаЗРЎўИЛ№ӨЖЖДӨЎўК№УГМҘН·ОьТэЖч»тІъЗҜЦъІъЎў№¬ДЪМҘ¶щН·ЖӨјаІвөИЛрЙЛРФІЩЧчЈ¬јхЙЩФЪ·ЦГд№эіМЦРҙ«ІҘ°¬ЧМІЎІЎ¶ҫөД»ъВКЎЈ
ПШёҫУЧұЈҪЎФәЦё¶ЁЧЁИЛёәФр¶ҪҙЩВдКөёРИҫФРІъёҫИХіЈұЈҪЎЎўЦОБЖЎўЛж·ГәНРӯөчПҪЗшёРИҫФРІъёҫЧЎФә·ЦГдөИ№ӨЧчЈ¬ІўУлПШјІІЎФӨ·АҝШЦЖЦРРДЎў°¬ЧМІЎҝ№ІЎ¶ҫЦОБЖ¶ЁөгТҪБЖ»ъ№№№ІН¬ҝӘХ№ёРИҫФРІъёҫ°¬ЧМІЎІЎіМјаІв№ӨЧчЎЈ
ПШјІІЎФӨ·АҝШЦЖЦРРД¶Ф»йјмЦР·ўПЦөДОҙФРёРИҫёҫЕ®Ј¬ТФј°РРИЛ№ӨЦХЦ№ИСЙпЎў·ЦГд42МмәуөДёРИҫІъёҫәНВъ18ёцФВҫӯИ·ХпОӘСфРФөД°¬ЧМІЎёРИҫ¶щНҜҪшРР№ЬАнЎЈ
ЈЁ2Ј©Г·¶ҫәНТТёОёРИҫФРІъёҫөДұЈҪЎЎЈёчТҪБЖОАЙъ·юОс»ъ№№УҰҪ«Г·¶ҫәНТТёОёРИҫФРІъёҫДЙИлёЯОЈ№ЬАнЈ¬ЧсСӯұЈГЬФӯФтЈ¬МṩіЈ№жФРІъЖЪұЈҪЎЎў°ІИ«РФРРОӘЦёөјЎўёРИҫЦўЧҙәНМеХчјаІвЎўУӘСшЦ§іЦЎўРДАнЦ§іЦЎўРФ°йёжЦӘУлҪЎҝөРыҪМөИ·юОсЎЈОӘёРИҫФРІъёҫМṩККТЛөД°ІИ«ЦъІъ·юОсЈ¬КөК©ЖХұйРФ·А»ӨҙлК©Ј¬јхЙЩ·ЦГд№эіМЦРјІІЎөДҙ«ІҘЎЈПШёҫУЧұЈҪЎФәёәФрГ·¶ҫәНТТёОёРИҫФРІъёҫөД№ЬАнЈ¬¶ҪҙЩВдКөёчПоұЈҪЎ·юОсЈ¬МṩФРІъЖЪөДЛж·Г·юОсЎЈ
2.ёРИҫФРІъёҫЛщЙъ¶щНҜұЈҪЎЎЈ
ЈЁ1Ј©°¬ЧМІЎёРИҫФРІъёҫЛщЙъ¶щНҜұЈҪЎЎЈПШёҫУЧұЈҪЎФә¶Ф°¬ЧМІЎёРИҫФРІъёҫЛщЙъ¶щНҜМṩ¶ЁЖЪЛж·Г·юОсЈ¬¶ҪҙЩәНЦёөјЖдҪшРРФзЖЪХп¶П,ГчИ·ёРИҫЧҙМ¬ЎЈЛж·ГУЪВъ1Ўў3Ўў6Ўў9Ўў12әН18ФВБдКұҪшРРЈ¬МṩіЈ№жұЈҪЎЎўЙъіӨ·ўУэјаІвЎўёРИҫЧҙҝцјаІвЎўФӨ·АУӘСшІ»БјЦёөјЎўГвТЯҪУЦЦөИ·юОсЈ¬ПкПёјЗВјЛж·ГөДПа№ШРЕПўЎЈ
ЈЁ2Ј©Г·¶ҫёРИҫФРІъёҫЛщЙъ¶щНҜұЈҪЎЎЈёчТҪБЖОАЙъ»ъ№№¶ФГ·¶ҫёРИҫФРІъёҫЛщЙъ¶щНҜМṩіЈ№жұЈҪЎЈ¬ПШёҫУЧұЈҪЎФә¶ФЖдМṩЛж·Г·юОсЈ¬¶ҪҙЩЖдҪшРРГ·¶ҫСӘЗеС§јмІвЈ¬ЦұЦБЕЕіэ»тХп¶ПЖдГ·¶ҫёРИҫЧҙМ¬Ј¬ІўјЗВјПа№ШРЕПўЈЁГ·¶ҫёРИҫФРІъёҫЛщЙъ¶щНҜЛж·Гј°ПИМмГ·¶ҫёРИҫЧҙМ¬јаІвНјјыёҪјю4-Нј8Ј©ЎЈ
ЈЁ3Ј©ТТёОёРИҫФРІъёҫЛщЙъ¶щНҜұЈҪЎЎЈёчЦъІъ»ъ№№ОӘТТёОёРИҫФРІъёҫЛщЙъ¶щНҜМṩіЈ№жұЈҪЎ·юОсЎЈ
ЈЁЛДЈ©ФӨ·АДёУӨҙ«ІҘёЙФӨ·юОсЎЈ
1.ФӨ·А°¬ЧМІЎДёУӨҙ«ІҘёЙФӨ·юОсЎЈ
ЈЁ1Ј©УҰУГҝ№ІЎ¶ҫТ©ОпЎЈёчТҪБЖОАЙъ»ъ№№¶Ф°¬ЧМІЎёРИҫФРІъёҫФЪФРЖЪЎўІъКұЎўІъәу42МмТФДЪј°ЖдЛщЙъ¶щНҜФЪ18ёцФВДЪМṩёЙФӨҙлК©Ј¬ІўҪ«ёРИҫФРІъёҫЦОБЖ·Ҫ°ёЎўІЎЗй·ўХ№Ўў·ЦГдҪбҫЦөИРЕПўј°Кұ·ҙАЎЦБПШёҫУЧұЈҪЎФәЎЈПШёҫУЧұЈҪЎФәТӘЦч¶ҜјУЗҝУл°¬ЧМІЎҝ№ІЎ¶ҫЦОБЖ¶ЁөгТҪБЖ»ъ№№әНјІІЎФӨ·АҝШЦЖ»ъ№№өД№өНЁУлБӘПөЎЈ
ЈЁ2Ј©МṩФРІъЖЪУГТ©ЧЙСҜЦёөјј°Па№ШјаІвЎЈёчТҪБЖОАЙъ»ъ№№ТӘФЪУҰУГҝ№ІЎ¶ҫТ©ОпЗ°әНУГТ©№эіМЦРЈ¬УҰОӘёРИҫФРІъёҫј°ЛщЙъ¶щНҜМṩіЦРшөДЧЙСҜЦёөјј°Па№ШјаІвЈ¬МбёЯУГТ©ТАҙУРФЈ»ФРІъёҫФЪҝ№ІЎ¶ҫУГТ©З°ЎўУГТ©№эіМЦРУҰҪшРРПа№ШөДјмІвЈ¬ІўҪбәПБЩҙІЦўЧҙ¶ФФРІъёҫёРИҫЧҙҝцҪшРРЖА№АЈ¬ТФұгИ·¶ЁУГТ©·Ҫ°ёәНјаІвЦОБЖР§№ыЈ¬ГЬЗР№ШЧўҝЙДЬіцПЦөДТ©ОпёұЧчУГЎЈМШұрКЗУГТ©іхЖЪәНФРНнЖЪЈ¬ТӘҪшРРCD4+TБЬ°НПё°ыјЖКэЎўІЎ¶ҫФШБҝј°ЖдЛыПа№ШјмІвЈЁ°ьАЁСӘіЈ№жЎўДтіЈ№жЎўёО№ҰДЬЎўЙц№ҰДЬЎўСӘЦ¬ЎўСӘМЗөИЈ©ЎЈУГТ©№эіМЦРЈ¬ГҝИэёцФВҪшРР1ҙОCD4+TБЬ°НПё°ыјЖКэј°ЖдЛыПа№ШјмІвЈЁН¬З°Ј©ЎЈ
ПШёҫУЧұЈҪЎ»ъ№№УҰјУЗҝ¶Ф°¬ЧМІЎёРИҫФРІъёҫЦОБЖ№эіМөД№ЬАнј°Р§№ыЖА№АЈ¬ТФМбёЯДёУӨЧи¶ПР§№ыЎЈТӘ¶ҪҙЩ°¬ЧМІЎёРИҫФРІъёҫҪшРРCD4+TБЬ°НПё°ыјЖКэЎўІЎ¶ҫФШБҝөИПа№ШјмІвЈ¬Іўј°Кұ»сИЎҪб№ыЎЈ
ЈЁ3Ј©ОӘ°¬ЧМІЎёРИҫФРІъёҫЛщЙъ¶щНҜМṩјмІвЎЈ°ҙХХЎ¶УӨ¶щ°¬ЧМІЎёРИҫФзЖЪХп¶П№ӨЧч·Ҫ°ёЎ·ЈЁ№ъОАёҫУЧёҫОАұгәҜЎІ2014Ўі27әЕЈ©Па№ШјјКхәНКұјдТӘЗ󣬶ФЛщЙъ¶щНҜУЪіцЙъәу6ЦЬәН3ёцФВКұЈ¬·ЦұрІЙјҜСӘұкұҫЈ¬ҪшРРУӨ¶щёРИҫФзЖЪХп¶ПЈЁПкјыёҪјю3-Нј6УӨ¶щ°¬ЧМІЎёРИҫФзЖЪХп¶Пј°·юОсБчіМЈ©ЎЈОҙҪшРРУӨ¶щФзЖЪХп¶ПјмІв»тУӨ¶щФзЖЪХп¶ПјмІвҪб№ыОӘТхРФөД¶щНҜЈ¬УҰУЪ12Ўў18ФВБдҪшРР°¬ЧМІЎҝ№МеЙёІйј°ұШТӘөДІ№ідКФСйЈ¬ТФГчИ·°¬ЧМІЎёРИҫЧҙМ¬ЈЁ°¬ЧМІЎёРИҫФРІъёҫЛщЙъ¶щНҜ°¬ЧМІЎҝ№МејмІвј°·юОсБчіМёҪјю3-Нј7Ј©ЎЈ
КЎёҫУЧұЈҪЎФәёәФрЧйЦҜәНРӯөчИ«КЎ¶щНҜёРИҫФзЖЪХп¶ПјмІв№ӨЧчЎЈПШёҫУЧұЈҪЎФә°ІЕЕЧЁИЛёәФрұҫПҪЗшДЪ°¬ЧМІЎёРИҫФРІъёҫЛщЙъ¶щНҜөДСӘСщІЙјҜЎўЛНјмЎўРЕПў·ҙАЎөИ№ӨЧчөДЧйЦҜУлРӯөчЎЈ
ФӨ·А°¬ЧМІЎДёУӨҙ«ІҘёЙФӨ·юОсјјКхТӘөгјыёҪјю3ЎЈ
2.ФӨ·АГ·¶ҫДёУӨҙ«ІҘёЙФӨ·юОсЎЈ
ЈЁ1Ј©ОӘГ·¶ҫёРИҫФРёҫМṩ№ж·¶ЦОБЖЎЈёчТҪБЖОАЙъ»ъ№№ОӘГ·¶ҫёРИҫФРёҫМṩ№ж·¶ЈЁИ«іМЎўЧгБҝЈ©өДЦОБЖЈ¬јхЙЩГ·¶ҫДёУӨҙ«ІҘЎЈ¶ФФРФзЖЪ·ўПЦөДГ·¶ҫёРИҫФРІъёҫЈЁ°ьАЁјИНщёРИҫХЯЈ©ФЪФРФзЖЪј°ФРНнЖЪУҰөұҪшРР№ж·¶өДЗаГ№ЛШЦОБЖЈ»¶ФФРЦРЎўНнЖЪТФј°БЩІъ·ўПЦөДГ·¶ҫёРИҫФРІъёҫЈ¬ТІТӘј°КұёшУиЦОБЖЎЈ°ҙХХПҪЗш№ЬАнөДФӯФтЈ¬УЙПШёҫУЧұЈҪЎФәБӘәПЦОБЖ»ъ№№Цё¶ЁЧЁИЛјУЗҝ¶ФЦОБЖ№эіМөДја№ЬЈ¬ФЪЦОБЖ№эіМЦР¶ЁЖЪҪшРРЛж·ГәНБЖР§ЖАјЫЎЈПШёҫУЧұЈҪЎФә¶ҪҙЩІўВдКөПҪЗшДЪёРИҫФРІъёҫФЪ·ЦГдЗ°ұШРлҪшРР·ЗГ·¶ҫВЭРэҝ№Меҝ№ФӯСӘЗеС§КФСй¶ЁБҝјмІвЎЈ
ЈЁ2Ј©ОӘГ·¶ҫёРИҫФРІъёҫЛщЙъ¶щНҜМṩФӨ·АРФЦОБЖЎЈёчТҪБЖОАЙъ»ъ№№УҰ¶ФФРЖЪОҙҪУКЬ№ж·¶РФЦОБЖЈ¬°ьАЁФРЖЪОҙҪУКЬИ«іМЎўЧгБҝөД№ж·¶ЦОБЖЈ¬»тФЪ·ЦГдЗ°1ёцФВДЪІЕҪшРРҝ№Г·¶ҫЦОБЖөДФРІъёҫЛщЙъ¶щНҜҪшРРФӨ·АРФЦОБЖЈ»¶ФФРЖЪҪУКЬ№э№ж·¶РФЦОБЖЈ¬іцЙъКұ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйСфРФЎўөО¶ИІ»ёЯУЪДёЗЧ·ЦГдЗ°өО¶ИөД4ұ¶¶щНҜТІРиТӘҪшРРФӨ·АРФЦОБЖЎЈ
ЈЁ3Ј©ОӘГ·¶ҫёРИҫФРІъёҫЛщЙъ¶щНҜМṩПИМмГ·¶ҫөДХп¶ПУлЦОБЖЎЈёчТҪБЖОАЙъ»ъ№№¶ФГ·¶ҫёРИҫФРІъёҫЛщЙъ¶щНҜіцЙъКұјҙҪшРРГ·¶ҫёРИҫПа№ШјмІвЈ¬ј°Кұ·ўПЦПИМмГ·¶ҫ»ј¶щЎЈ¶ФіцЙъКұГчИ·Хп¶ПөДПИМмГ·¶ҫ¶щНҜј°КұёшУи№ж·¶ЦОБЖЈ¬ІўЙПұЁПИМмГ·¶ҫёРИҫРЕПўЈ»ФЪГ»УРМхјю»тОЮ·ЁҪшРРПИМмГ·¶ҫХп¶ПЎўЦОБЖөДЗйҝцПВУҰј°КұҪшРРЧӘХпЈ»¶ФіцЙъКұІ»ДЬГчИ·Хп¶ППИМмГ·¶ҫөД¶щНҜЈ¬УЙПШёҫУЧұЈҪЎФәЦё¶ЁЧЁИЛ¶ЁЖЪЛж·ГЈ¬ј°КұХп¶П»тЕЕіэПИМмГ·¶ҫЈ»¶ФЛж·Г№эіМЦРХп¶ПөДПИМмГ·¶ҫ¶щНҜј°КұёшУи№ж·¶ЦОБЖІўЙПұЁПИМмГ·¶ҫёРИҫРЕПўЎЈ
ФӨ·АГ·¶ҫДёУӨҙ«ІҘёЙФӨ·юОсјјКхТӘөгјыёҪјю4ЎЈ
3.ФӨ·АТТёОДёУӨҙ«ІҘёЙФӨ·юОсЎЈ
ЈЁ1Ј©ТТёОёРИҫФРІъёҫёЙФӨЎЈёчТҪБЖОАЙъ»ъ№№УҰөұОӘТТёОІЎ¶ҫұнГжҝ№ФӯСфРФөДёРИҫФРІъёҫМṩТТёОІЎ¶ҫёРИҫСӘЗеС§ұкЦҫОпЈЁБҪ¶Ф°лЈ©әНёО№ҰДЬјмІвЈ¬УРМхјюөДөҘО»ҝЙҪшРРТТёОІЎ¶ҫФШБҝЈЁHBV DNAЈ©јмІвЈ¬ГЬЗРјаІвёОФа№ҰДЬЗйҝцЈ¬ёшУиЧЁҝЖЦёөјЎЈұШТӘКұЧӘҪйЦБҙ«ИҫІЎЧЁҝЖҪУКЬПаУҰөДХпБЖ·юОсЎЈ
ЈЁ2Ј©ТТёОёРИҫФРІъёҫЛщЙъ¶щНҜёЙФӨЎЈёчТҪБЖОАЙъ»ъ№№ОӘЛщУРТТёОІЎ¶ҫұнГжҝ№ФӯСфРФФРІъёҫЛщЙъРВЙъ¶щГв·СМṩעЙдТТёОГвТЯЗтө°°Ч·юОсЈ¬°ҙХХЎ¶ФӨ·АҪУЦЦ№ӨЧч№ж·¶Ў·МṩТТёОТЯГзГвТЯ·юОсЎЈФЪНкіЙөЪ3јБҙОТТёОТЯГзҪУЦЦәу1-6ёцФВЈ¬јҙ¶щНҜ7ФВБдЦБ1ЦЬЛкЖЪјдЈ¬ҝЙҪшРРТТёОІЎ¶ҫёРИҫСӘЗеС§ұкЦҫОпЈЁБҪ¶Ф°лЈ©јмІвЈ¬ЕР¶ПГвТЯР§№ыЎЈ
ФӨ·АТТёОДёУӨҙ«ІҘ·юОсјјКхТӘөгјыёҪјю5ЎЈ
ЈЁОеЈ©ёРИҫФРІъёҫј°ЛщЙъ¶щНҜЧЫәП№Ш»іУлЦ§іЦЎЈТҪБЖОАЙъ»ъ№№ЎўЙзЗшј°ЖдЛыПа№ШЧйЦҜУҰөұёщҫЭЧФЙн·юОсөДМШөгәНДЬБҰЈ¬НЁ№э¶аЦЦРОКҪ»тЗюөАЈ¬ОӘ°¬ЧМІЎЎўГ·¶ҫәНТТёОёРИҫФРІъёҫЎў¶щНҜј°ЖдјТНҘЈ¬МṩФӨ·АДёУӨҙ«ІҘөДПа№ШЧЙСҜЦёөјЎўРДАнЦ§іЦЎўЧЫәП№Ш»іј°ЧӘҪйөИТҪБЖұЈҪЎЧЫәП·юОсЎЈ
ЈЁБщЈ©°¬ЧМІЎЎўГ·¶ҫёРИҫФРІъёҫј°ЛщЙъ¶щНҜЧӘҪй·юОсЎЈПШОАЙъјЖЙъРРХюІҝГЕЦё¶ЁЧЁИЛёәФрРӯөчЧӘҪй№ӨЧчЈ¬ПШёҫУЧұЈҪЎ»ъ№№ТӘЦё¶ЁЧЁИЛёәФрЧӘҪйПа№Ш№ӨЧчІўВдКөЈ¬ЧӘҪйКұРиМоРҙЎ¶әюДПКЎIPMTCTСфРФёц°ёЧӘҪйҝЁЎ·(јыёҪјю6Ј©Ј¬ФЪЧӘҪй·юОсЦРСПёсЧсКШұЈГЬФӯФтЈ¬І»өГұ©В¶ЧӘҪй¶ФПуөДёцИЛРЕПўЎЈ
1.»йЗ°ЎўФРЗ°ұЈҪЎЦРөДОҙФР°¬ЧМІЎёРИҫёҫЕ®Ўў°¬ЧМІЎёРИҫФРІъёҫИЛ№ӨЦХЦ№ИСЙпәуЎў·ЦГд42МмәуөДёРИҫФРІъёҫәНВъ18ФВБдИ·ХпОӘСфРФөД°¬ЧМІЎёРИҫ¶щНҜЧӘИлПШјІІЎФӨ·АҝШЦЖЦРРДҪшРР№ЬАнЎЈ
2.°¬ЧМІЎЎўГ·¶ҫёРИҫФРІъёҫј°ЛщЙъ¶щНҜФЪЦОБЖЖЪјдЈ¬Из·ўЙъұҫ»ъ№№І»ДЬҙҰАнөДјІІЎөИЈ¬ЙПұЁЦБПШёҫУЧұЈҪЎФәЈ¬УЙЧЁИЛЕгН¬»ӨЛНЈ¬ј°КұЧӘҪйөҪҫЯұёҙҰАнДЬБҰөДТҪБЖОАЙъ»ъ№№ЎЈ
3.°¬ЧМІЎёРИҫФРёҫЎўІъәуОҙВъ42МмөДІъёҫј°ЛщЙъОҙВъ18ёцФВөД¶щНҜЈ¬Г·¶ҫёРИҫФРІъёҫј°ЛщЙъ¶щНҜФЪұЈҪЎЛж·Г№ЬАнЖЪјдҝзөШЗшөДЧӘҪйЈ¬°ьАЁҝзПШЎўКРј°ҝзКЎЧӘҪйЎЈНЁ№эПШёҫУЧұЈҪЎФәЦё¶ЁЧЁИЛҪшРРЧӘҪйЈ¬ВдКөЦОБЖәНЛж·ГЈ¬ІўҪ«ЧӘҪйРЕПўј°Кұ·ҙАЎЦБЧӘіцөҘО»ЎЈ
ИэЎўұЈХПҙлК©
ЈЁТ»Ј©·юОсДЬБҰҪЁЙиЎЈТ»КЗҪЎИ«ХпБЖНшВзЈ¬ҪЁБўТФёҫУЧұЈҪЎ»ъ№№ОӘәЛРДЈ¬МṩФРІъЖЪұЈҪЎ·юОсөДТҪБЖОАЙъ»ъ№№ОӘЦ§іЕөДХпБЖНшВзЈ¬УИЖдТӘјУЗҝёҫУЧұЈҪЎ»ъ№№өДДЬБҰҪЁЙиЈ¬ОӘёРИҫФРІъёҫј°ЛщЙъ¶щНҜМṩ№ж·¶өДХпБЖ·юОсЎЈ¶юКЗҪЁБўіӨР§ЕаСө»ъЦЖЈ¬УРјЖ»®өШҝӘХ№ПШЎўПзЎўҙеөДЦрј¶ЕаСөЈ¬К№ЛщУРіРөЈФӨ·АДёУӨҙ«ІҘ·юОсөДПа№ШИЛФұЈ¬¶јДЬ¶ЁЖЪөГөҪПа№ШөДЧЁТөјјДЬЕаСөәНёҙСөЎЈИэКЗјУЗҝКөСйКТҪЁЙиЈ¬ЕдұёұШТӘөДјмІвЙиұёәНәПёсөДјмСйИЛФұЈ¬НкЙЖКөСйКТПа№ШјмІв·юОсЦЖ¶Иј°БчіМ,СПёсКөСйКТКТДЪәНКТјдЦКБҝҝШЦЖЈ¬ұЈХП№ӨЧчЛіі©ФЛЧӘЎЈЛДКЗјУЗҝІъҝЖҪЁЙиЈ¬И·ұЈФЪТҪБЖІЩЧчЦРЧсСӯЖХұйРФ·А»ӨФӯФтЈ¬ЦҙРРУР№ШПы¶ҫёфАлЦЖ¶ИЈ¬ЧоҙуПЮ¶ИөШұЬГвТҪФҙРФёРИҫј°ТҪ»ӨИЛФұөДЦ°Төұ©В¶ЎЈ
ЈЁ¶юЈ©РЕПў№ЬАнЎЈёчТҪБЖОАЙъ»ъ№№УҰөұЦё¶ЁЧЁИЛёәФрРЕПў№ЬАн№ӨЧчЈ¬ТӘФЪ»йЗ°ұЈҪЎЎўФРІъЖЪұЈҪЎЎўІъКұұЈҪЎЎў¶щНҜұЈҪЎөИПа№ШөЗјЗЦРјЗВјУР№ШРЕПўЎЈ¶ЁЖЪКХјҜЎўХыАнЎўМоұЁФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧчФВұЁұнј°ПөБРёц°ёөЗјЗҝЁЈ¬ј°КұҪшРРКэҫЭРЕПўөДНшВзұЁёжЎЈ°ҙХХЎ¶ЦР»ӘИЛГс№ІәН№ъҙ«ИҫІЎ·АЦО·ЁЎ·ЎўЎ¶ҙ«ИҫІЎРЕПўұЁёж№ЬАн№ж·¶Ў·өИПа№ШТӘЗуҪшРР°¬ЧМІЎЎўГ·¶ҫәНТТёОТЯЗйұЁёжЈ¬ІўұЈХПТЯЗйұЁёжЧјИ·РФЎЈ
ёчТҪБЖОАЙъ»ъ№№ФЪКэҫЭРЕПўКХјҜ№эіМЦРУҰИПХжәЛ¶ФёчАаФӯКјөЗјЗУлјЗВјЈ¬И·ұЈПа№ШұЁұнРЕПў·ыәПВЯјӯЎўНкХыЎўЧјИ·Ј»ПШёҫУЧұЈҪЎФәУҰ°ҙХХТӘЗуҪшРРПа№ШКэҫЭРЕПўөДЙуәЛЎў№ЬАнЎўЦКБҝҝШЦЖј°·ЦОцАыУГЈ¬И·ұЈКэҫЭРЕПўЙПұЁөДј°КұРФЎўНкХыРФәНЧјИ·РФЈ¬Гҝ°лДкПтПШОАЙъјЖЙъРРХюІҝГЕМбҪ»Т»ҙОКэҫЭ·ЦОцұЁёжЎЈ
ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘПа№ШұЁұнЙПұЁБчіМј°ТӘЗујыёҪјю7ЎЈ
ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧч»щҙЎұнёсјыёҪјю8ЎЈ
ЈЁИэЈ©ја¶ҪЦёөјУлЖА№АЎЈУЙПШОАЙъјЖЙъҫЦЦЖ¶©ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧчөДја¶ҪЦёөјУлЖА№А·Ҫ°ёЈ¬ЧйЦҜҝӘХ№ЧФІйЎўја¶ҪЦёөјәНЖА№АЈ¬ГҝДкҝӘХ№ЧЁПо¶Ҫөј1-2ҙОІўІ»¶ЁЖЪНЁұЁЈ»¶ФҙжФЪОКМвҪП¶аЎўХыёДІ»БҰөДөҘО»ТӘЖф¶ҜФјМёОКФр»ъЦЖЈ¬¶ФПоДҝВдКөҙжФЪСПЦШОКМвөДөҘО»Ј¬УиТФНЁұЁЕъЖАЎўПЮЖЪХыёДЎўИЎПыЦъІъ·юОсөИ№ЬАнҙлК©ЎЈ
ЈЁЛДЈ©ЧКҪрәНОпЧК№ЬАнЎЈПШёҫУЧұЈҪЎФәТӘ°ҙХХЧЁПоЧКҪр№ЬАн°м·ЁЈ¬јУЗҝЧКҪр№ЬАнЈ¬КөРРЧЁҝоЧЁУГЈ¬ұЈХПЧКҪрУГУЪјмІвЙёІйЎўЧЫәПёЙФӨЎўЧ·ЧЩЛж·ГЎўРЕПў№ЬАнЎўДЬБҰҪЁЙиөИФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘПа№Ш№ӨЧчЈ¬МбёЯҫӯ·СК№УГР§ВКЎЈ
ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧчЧКҪрЎўОпЧК№ЬАн№ж¶ЁјыёҪјю9ЎЈ
ЛДЎўЦ°Фр·Ц№Ө
ЈЁТ»Ј©ОАЙъјЖЙъРРХюІҝГЕЎЈПШОАјЖҫЦёҫУЧҪЎҝө·юОс№ЙЗЈН·ёәФрИ«ПШФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧчөДЧйЦҜРӯөчУл№ЬАнЈ»ТҪХю№ЙёәФрРӯөч°¬ЧМІЎЎўГ·¶ҫәНТТёОёРИҫФРІъёҫј°ЖдЛщЙъ¶щНҜөДПа№ШХпБЖ№ӨЧчЈ»јІІЎФӨ·АҝШЦЖЦРРДёәФр°¬ЧМІЎЎўГ·¶ҫТЯЗйјаІвөДЧйЦҜ№ӨЧчЈ»ҪЎҪМ№ЙёәФрЧйЦҜҝӘХ№РОКҪ¶аСщөДЦчМвРыҙ«»о¶ҜЈ¬РӯөчГҪМеЧйЦҜРВОЕРыҙ«Ј¬ҪМУэТэөјҝЖС§өДЙъ»оАнДоәНҪЎҝөөДЙъ»о·ҪКҪЈ»»щІгОАЙъ№ЙёәФрја¶ҪПоДҝҪбәПФРІъёҫҪЎҝө№ЬАнәН0Ў«6Лк¶щНҜҪЎҝө№ЬАнФЪПзХтОАЙъФәәНЙзЗшОАЙъ·юОсЦРРДөДҝӘХ№әНВдКөЎЈ
ЈЁ¶юЈ©ТҪБЖОАЙъ»ъ№№ЎЈ
1.ПШёҫУЧұЈҪЎФәЎЈіРөЈПҪЗшФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧчөДјјКхЦёөјУл·юОсЈ¬РӯЦъіЙБўЧЁјТјјКхЦёөјЧйЈ»РӯЦъҪЁБў°¬ЧМІЎЎўГ·¶ҫәНТТёОёРИҫФРІъёҫј°ЛщЙъ¶щНҜөД№ж·¶»ҜХпЦОНшВзЈ»ёщҫЭ¶ҪөјЖА№А·Ҫ°ёЈ¬РӯЦъ¶Ф№ӨЧчҝӘХ№ЗйҝцҪшРРја¶ҪЦёөјәНЖА№АЈ»ёәФрФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘЧКҪрЎўОпЧК№ЬАнЈ»РӯЦъҝӘХ№ПоДҝИЛФұЕаСөЈ»ФЪФәДЪІҝіЙБўУЙФРІъұЈҪЎҝЖЎў¶щНҜұЈҪЎҝЖЎўРЕПў№ЬАнҝЖЎўјмСйҝЖЎўҪЎҝөҪМУэҝЖөИПа№ШҝЖКТИЛФұЧйіЙөДПоДҝ№ЬАнРЎЧйЈ»УРЧЁИЛёәФрОӘПҪЗшДЪ°¬ЧМІЎЎўГ·¶ҫёРИҫФРІъёҫј°ЛщЙъ¶щНҜҪЁБўөө°ёЈ¬ҪшРРұЈҪЎЛж·Г№ЬАнЈ»УРЧЁИЛёәФрФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘРЕПў№ЬАн№ӨЧчЈ¬ёәФрПоДҝЧКБПөДКХјҜЎўХыАнЎў·ЦОцЎўЧЬҪбЈ¬ЙПұЁөИ№ӨЧчЈ¬ІўНЁұЁПШјІІЎФӨ·АҝШЦЖЦРРДЎЈ
2.ПШјІІЎФӨ·АҝШЦЖЦРРДЎЈЕдәПҝӘХ№ёРИҫФРІъёҫј°ЛщЙъ¶щНҜөДХпЦОЎўЛж·Г·юОсЈ»іРөЈұҫПҪЗш°¬ЧМІЎәНГ·¶ҫТЯЗйјаІвЈ¬ГҝёцФВПтПҪЗшДЪёҫУЧұЈҪЎ»ъ№№НЁұЁТЯЗйЈ»іРөЈФРІъёҫ°¬ЧМІЎІ№ідКФСйЎўCD4+TБЬ°НПё°ыјЖКэәНІЎ¶ҫФШБҝјмІвөИ№ӨЧчЈ¬И·ИПҪб№ыУҰФЪҪУСщЦ®ИХЖр10ёц№ӨЧчИХДЪ·ҙАЎЈ¬CD4+TБЬ°НјЖКэҪб№ыУҰФЪҪУСщЦ®ИХЖрөД7ёц№ӨЧчИХ·ҙАЎЈ¬ІЎ¶ҫФШБҝөДҪб№ыУҰФЪҪУСщЦ®ИХЖр20ёц№ӨЧчИХ·ҙАЎЈ»ёәФрҪУКХПШёҫУЧұЈҪЎФә»йЗ°ЎўФРЗ°ТҪС§јмІйЦР·ўПЦөД°¬ЧМІЎёРИҫХЯЎўКөК©ЦХЦ№ИСЙпЎў·ЦГд42МмәуөД°¬ЧМІЎёРИҫёҫЕ®әНВъ18ёцФВҫӯИ·ИПСфРФөД°¬ЧМІЎёРИҫ¶щНҜЈ¬ІўДЙИлұҫөШ°¬ЧМІЎЧЫәП·АЦОМеПөҪшРР№ЬАнЈ»РӯЦъПШёҫУЧұЈҪЎФәҝӘХ№ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧчПа№ШЕаСөЎўјјКхЦёөјЈ»Цч¶ҜХЖОХФРІъёҫәНРВЙъ¶щёРИҫЧҙҝцЎЈ
3.ТҪБЖОАЙъ»ъ№№ЎЈҝӘХ№ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘҪЎҝөҪМУэЈ»ОӘЛщУРФРІъёҫМṩ°¬ЧМІЎЎўГ·¶ҫәНТТёОөДјмІвУлЧЙСҜЈ»¶ФёРИҫФРІъёҫКөРРКЧХпёәФрЦЖЈ¬МṩФРІъЖЪұЈҪЎ·юОсЈ»ОӘёРИҫФРІъёҫәНЛщЙъ¶щНҜМṩ№ж·¶ЦОБЖәНёЙФӨ·юОсЈ»УРЧКЦКөД»ъ№№іРөЈФРІъёҫ°¬ЧМІЎІ№ідКФСйЎўCD4+TБЬ°НПё°ыјЖКэЎўІЎ¶ҫФШБҝјмІвөИ№ӨЧчЈ»СПёс№ж·¶№ЬАнҫӯ·СәНПа№ШОпЧКЈ»°ҙТӘЗуПтПШёҫУЧұЈҪЎФәұЁёжФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧчКэҫЭРЕПўЈ»°ҙТӘЗуІОјУФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘТөОсјјКхЕаСөЈ¬ІўЧйЦҜКөК©ұҫ»ъ№№ДЪПа№ШТөОсЦӘК¶ЕаСөЈ»ҪУКЬПШёҫУЧұЈҪЎФәөДјјКхЦёөјЎЈ
ёҪјюЈә1Ј®ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘХыәП·юОсБчіМ
2Ј®ФРІъёҫ°¬ЧМІЎЎўГ·¶ҫәНТТёОјмІв·юОсјјКхТӘөг
3Ј®ФӨ·А°¬ЧМІЎДёУӨҙ«ІҘёЙФӨ·юОсјјКхТӘөг
4Ј®ФӨ·АГ·¶ҫДёУӨҙ«ІҘёЙФӨ·юОсјјКхТӘөг
5Ј®ФӨ·АТТёОДёУӨҙ«ІҘёЙФӨ·юОсјјКхТӘөг
6Ј®°¬ЧМІЎЎўГ·¶ҫёРИҫФРІъёҫј°ЛщЙъ¶щНҜЧӘҪйҝЁ
7Ј®ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘПа№ШұЁұнЙПұЁ
БчіМј°ТӘЗу
8Ј®ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧч»щҙЎұнёс
9Ј®ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧчЧКҪрЎўОп
ЧК№ЬАн№ж¶Ё
ёҪјю1
ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘХыәП·юОсБчіМ
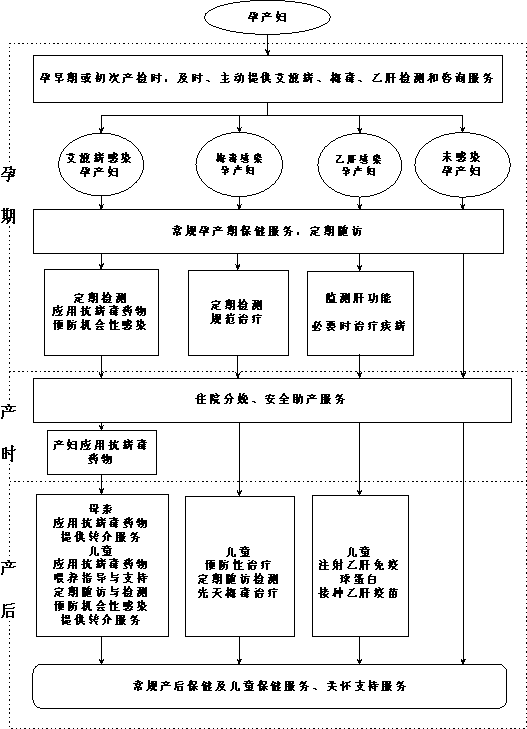
Нј1. ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘХыәП·юОсБчіМ
ёҪјю2
ФРІъёҫ°¬ЧМІЎЎўГ·¶ҫәНТТёОјмІв·юОсјјКхТӘөг
Т»ЎўФРІъёҫ°¬ЧМІЎјмІв
ІОХХЎ¶И«№ъ°¬ЧМІЎјмІвјјКх№ж·¶ЈЁ2014ДкРЮ¶©°жЈ©Ў·ЦРБЩҙІХп¶ППа№ШөДјмІвІЯВФҪшРРФРІъёҫ°¬ЧМІЎјмІвЎЈ
ЈЁТ»Ј©јмІв·Ҫ·ЁЎЈ
ФРІъёҫ°¬ЧМІЎјмІв·Ҫ·Ё°ьАЁҝ№МеЙёІйКФСйәНІ№ідКФСйЎЈ
ҝ№МеЙёІйКФСй°ьАЁҝмЛЩјмІвЈЁRTЈ©ЎўГёБӘГвТЯОьёҪКФСйЈЁELISAЈ©Ўў»ҜС§·ў№вГвТЯКФСйЈЁCLIAЈ©ЎўГчҪәҝЕБЈДэјҜКФСйЈЁPAЈ©өИЎЈ
І№ідКФСй°ьАЁҝ№МеІ№ідКФСйәНәЛЛбІ№ідКФСйөИЎЈҪЁТйКЧСЎҝ№МеІ№ідКФСйЈ¬Изө°°ЧГвТЯУЎјЈКФСйЈЁWBЈ¬ФӯИ·ЦӨКФСйЈ©ЎўМхҙш/ПЯРФГвТЯКФСйЈЁRIBA/LIAЈ©ЎЈ
ЈЁ¶юЈ©јмІвБчіМЎЈ
ФРІъёҫіхҙОҪУКЬФРІъЖЪұЈҪЎКұЈ¬КЧПИҪшРР°¬ЧМІЎҝ№МеЙёІйКФСйЎЈЙёІйКФСйҪб№ыУР·ҙУҰХЯЈ¬К№УГФӯУРКФјБәНБнНвТ»ЦЦЙёІйКФјБҪшРРёҙјмЈ¬ТІҝЙК№УГФӯУРКФјБЛ«·ЭҪшРРёҙјмЎЈёщҫЭёҙјмҪб№ыЈ¬И·¶ЁКЗ·сҪшРРІ№ідКФСйЎЈТАҫЭІ№ідКФСйҪб№ыЈ¬ЕР¶ЁёРИҫЧҙҝцЈЁПкјыНј2Ј©ЎЈ
БЩІъКұІЕС°ЗуЦъІъ·юОсөДФРІъёҫЈ¬РиН¬КұУҰУГБҪЦЦІ»Н¬өДҝмЛЩјмІвКФјБҪшРРЙёІйЈ¬ёщҫЭЙёІйјмІвҪб№ыЈ¬ј°КұМṩәуРш·юОсЈЁПкјыНј3Ј©ЎЈ
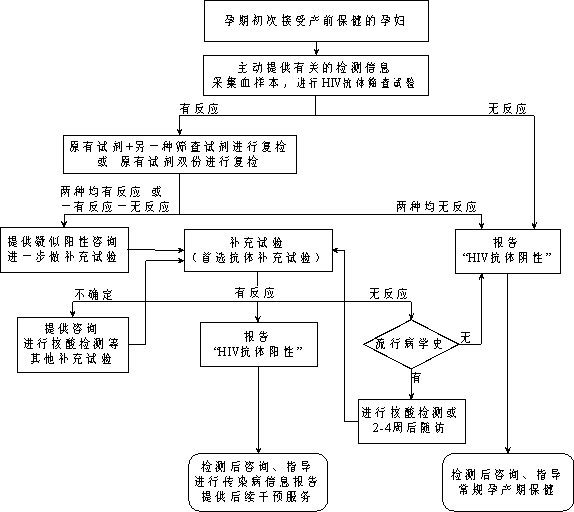
Нј2. ФРЖЪ°¬ЧМІЎјмІвј°·юОсБчіМ
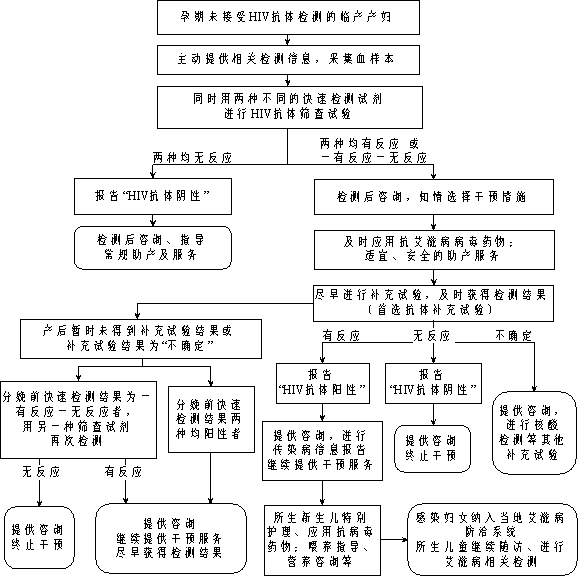
![]() Нј3. ІъКұ°¬ЧМІЎјмІвј°·юОсБчіМ
Нј3. ІъКұ°¬ЧМІЎјмІвј°·юОсБчіМ
ЈЁККУГУЪФРЖЪОҙҪУКЬ°¬ЧМІЎјмІвөДІъёҫЈ©
![]() ¶юЎўФРІъёҫГ·¶ҫСӘЗеС§јмІв
¶юЎўФРІъёҫГ·¶ҫСӘЗеС§јмІв
ЈЁТ»Ј©јмІв·Ҫ·ЁЎЈ
Г·¶ҫСӘЗеС§јмІв·Ҫ·Ё°ьАЁ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйәНГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйЎЈ
1. ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйіЈУГ·Ҫ·Ё°ьАЁјЧұҪ°·әмІ»јУИИСӘЗеКФСйЈЁTRUSTЈ©ЎўҝмЛЩСӘҪ¬·ҙУҰЛШ»·ЧҙҝЁЖ¬КФСйЈЁRPRЈ©өИЈ»
2. Г·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйіЈУГ·Ҫ·Ё°ьАЁГ·¶ҫВЭРэМеҝЕБЈДэјҜКФСйЈЁTPPAЈ©ЎўГёБӘГвТЯОьёҪКФСйЈЁELISAЈ©ЎўГвТЯІгОц·Ё-ҝмЛЩјмІвЈЁRTЈ©Ўў»ҜС§·ў№вГвТЯКФСйЈЁCLIAЈ©өИЎЈ
ЈЁ¶юЈ©јмІвБчіМЎЈ
ФРІъёҫіхҙОҪУКЬФРІъЖЪұЈҪЎКұЈ¬јҙІЙУГИОТвТ»АаГ·¶ҫСӘЗеС§јмІв·Ҫ·ЁҪшРРГ·¶ҫЙёІйЎЈЙёІйҪб№ыіКСфРФ·ҙУҰХЯФЪұҫ»ъ№№БўјҙУГН¬Т»СӘЗеСщұҫІЙУГБнТ»АајмІв·Ҫ·ЁҪшРРёҙјмЈ¬И·¶ЁЖдКЗ·сОӘГ·¶ҫёРИҫЈЁПкјыНј4Ј©ЎЈФЪУРМхјюөШЗшЈ¬ҪЁТйКЧСЎГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйҪшРРЙёІйЎЈ
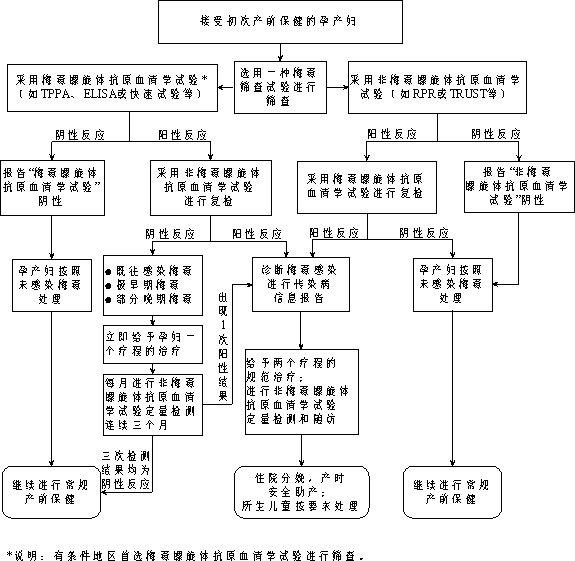
Нј4. ФРІъёҫГ·¶ҫјмІвј°·юОсБчіМ
ИэЎў![]() ФРІъёҫТТёОјмІв
ФРІъёҫТТёОјмІв
ЈЁТ»Ј©јмІв·Ҫ·ЁЎЈ
ТТёОІЎ¶ҫёРИҫСӘЗеС§ұкЦҫОпјмІв·Ҫ·Ё°ьАЁГёБӘГвТЯОьёҪКФСйЈЁELISAЈ©ЎўҪрұкјЗГвТЯ·ЦОцЈЁҪәМеҪрЈ©Ўў»ҜС§·ў№вГвТЯКФСйЈЁCLIAЈ©өИЎЈНЖјцК№УГГёБӘГвТЯОьёҪКФСйҪшРРјмІвЎЈёщҫЭРиТӘҝЙҪшРРөҘТ»ТТёОұнГжҝ№ФӯјмІвЈ¬»тТТёОІЎ¶ҫёРИҫСӘЗеС§ұкЦҫОпЈЁБҪ¶Ф°лЈ©јмІвЎЈ
ЈЁ¶юЈ©јмІвБчіМЎЈ
ФРІъёҫіхҙОҪУКЬФРІъЖЪұЈҪЎКұЈ¬МṩТТёОұнГжҝ№ФӯјмІвЎЈјмІвҪб№ыСфРФЈ¬ұЁёжЎ°ТТёОұнГжҝ№ФӯСфРФЎұЈ¬И·¶ЁТТёОІЎ¶ҫёРИҫЈ¬јМ¶шҪшРРТТёОІЎ¶ҫёРИҫСӘЗеС§ұкЦҫОпЈЁБҪ¶Ф°лЈ©өИПа№ШјмІвЎЈУРМхјюөДөШЗшЈ¬ҝЙФЪЙёІйКұЦұҪУҪшРРТТёОІЎ¶ҫёРИҫСӘЗеС§ұкЦҫОпЈЁБҪ¶Ф°лЈ©јмІвЈЁПкјыНј5Ј©ЎЈ
ТТёОІЎ¶ҫёРИҫСӘЗеС§ұкЦҫОпЈЁБҪ¶Ф°лЈ©°ьАЁұнГжҝ№ФӯЈЁHBsAgЈ©ЎўұнГжҝ№МеЈЁҝ№ЁCHBsЈ©Ўўeҝ№ФӯЈЁHBeAgЈ©Ўўeҝ№МеЈЁҝ№ЁCHBeЈ©әНәЛРДҝ№МеЈЁҝ№ЁCHBcЈ©ЎЈ
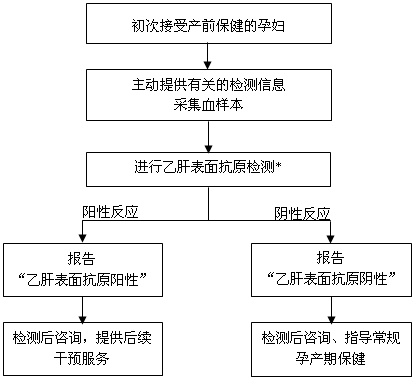 |
*УРМхјюөДөШЗшЈ¬ҝЙФЪЙёІйКұЦұҪУҪшРРТТёОІЎ¶ҫёРИҫСӘЗеС§ұкЦҫОпЈЁБҪ¶Ф°лЈ©јмІв
Нј5. ФРІъёҫТТёОјмІвј°·юОсБчіМ
ёҪјю3
ФӨ·А°¬ЧМІЎДёУӨҙ«ІҘёЙФӨ·юОсјјКхТӘөг
Т»ЎўФРІъёҫҝ№ІЎ¶ҫЦОБЖ·Ҫ°ё
ЈЁТ»Ј©НЖјц·Ҫ°ёЎЈ
1. ФРЖЪ»тБЩІъ·ўПЦёРИҫЎўЙРОҙҪУКЬҝ№ІЎ¶ҫЦОБЖөДФРІъёҫЈ¬УҰјҙҝМёшУиҝ№ІЎ¶ҫЦОБЖЎЈЦОБЖ·Ҫ°ёНЖјцСЎФсТФПВБҪЦЦ·Ҫ°ёЦРөДИОТвТ»ЦЦЈ¬ТІҝЙёщҫЭКөјКЗйҝцҪшРРөчХыЎЈ
·Ҫ°ёТ»ЈәЖл¶а·т¶ЁЈЁAZTЈ©+АӯГЧ·т¶ЁЈЁ3TCЈ©+ВеЖҘДЗОӨ/АыНРДЗОӨЈЁLPV/rЈ©Ј¬»т
·Ҫ°ё¶юЈәМжЕө·тОӨЈЁTDFЈ©+АӯГЧ·т¶ЁЈЁ3TCЈ©+ТА·ЗОӨВЧЈЁEFVЈ©
ұн1. іЈУГҝ№ІЎ¶ҫТ©ОпјББҝј°К№УГ·Ҫ·Ё
|
Т©Оп |
өҘҙОјББҝ |
К№УГ·Ҫ·Ё |
|
AZT |
300 mg |
1Мм2ҙО |
|
3TC |
300 mg |
1Мм1ҙО |
|
LPV/r |
200mg/50mg/Ж¬Ј¬2Ж¬ |
1Мм2ҙО |
|
TDF |
300mg |
1Мм1ҙО |
|
EFV |
600mg |
1Мм1ҙО |
2. ФРЗ°ТСҪУКЬҝ№ІЎ¶ҫЦОБЖөДФРІъёҫЈ¬ёщҫЭІЎ¶ҫФШБҝјмІвҪб№ыҪшРРІЎ¶ҫТЦЦЖР§№ыЖА№АЎЈИз№ыІЎ¶ҫТЦЦЖР§№ыАнПлЈЁјҙІЎ¶ҫФШБҝРЎУЪЧоөНјмІвПЮЈ©Ј¬ҝЙұЈіЦФӯЦОБЖ·Ҫ°ёІ»ұдЈ»·сФтЈ¬өчХыҝ№ІЎ¶ҫЦОБЖУГТ©·Ҫ°ёЎЈ
ЈЁ¶юЈ©ЧўТвКВПоЎЈ
1. Т»ө©·ўПЦ°¬ЧМІЎёРИҫФРІъёҫЈ¬ОЮВЫЖдКЗ·сҪшРРCD4+TБЬ°НПё°ыјЖКэәНІЎ¶ҫФШБҝјмІвЈ¬ТІОЮВЫЖдјмІвҪб№ыИзәОЈ¬¶јТӘҫЎҝмҝӘКјҝ№ІЎ¶ҫЦОБЖЎЈФЪ·ЦГдҪбКшәуЈ¬ОЮВЫІЙУГәОЦЦУӨ¶щО№Сш·ҪКҪЈ¬ҫщОЮРиНЈТ©Ј¬ҫЎҝмҪ«ЖдЧӘҪйөҪҝ№ІЎ¶ҫЦОБЖ»ъ№№Ј¬јМРшәуРшҝ№ІЎ¶ҫЦОБЖ·юОсЎЈМШұрЗҝөчЈ¬¶ФУЪСЎФсДёИйО№СшөДІъёҫЈ¬ИзТтМШКвЗйҝцРиТӘНЈТ©Ј¬УҰУГҝ№ІЎ¶ҫТ©ОпЦБЙЩТӘіЦРшЦБДёИйО№СшҪбКшәуТ»ЦЬЎЈ
2. өұФРІъёҫСӘәмө°°ЧөНУЪ90g/L»тЦРРФБЈПё°ыөНУЪ0.75ЎБ109/LЈ¬ҪЁТйІ»СЎ»тНЈУГAZTЎЈУҰУГTDFЗ°Ј¬РлҪшРРЙцФа№ҰДЬЖА№АЎЈ
ҫЯМеІОјыЎ¶ФӨ·А°¬ЧМІЎДёУӨҙ«ІҘјјКхЦёөјКЦІбЎ·ј°Ў¶№ъјТГв·С°¬ЧМІЎҝ№ІЎ¶ҫТ©ОпЦОБЖКЦІбЎ·ЎЈ
¶юЎўУӨ¶щҝ№ІЎ¶ҫУГТ©·Ҫ°ё
УӨ¶щУҰФЪіцЙъәуҫЎФзЈЁ6Ў«12РЎКұДЪЈ©ҝӘКј·юУГҝ№ІЎ¶ҫТ©ОпЈ¬ҝЙТФСЎФсТФПВБҪЦЦ·Ҫ°ёЦРөДИОТвТ»ЦЦЈЁПкјыұн2әНұн3Ј©ЎЈУӨ¶щИфҪУКЬДёИйО№СшЈ¬УҰКЧСЎNVP·Ҫ°ёЎЈ
ұн2. УӨ¶щФӨ·АУГТ©ҪЁТйјББҝЈәДООӨАӯЖҪЈЁNVPЈ©
|
іцЙъМеЦШ |
УГТ©јББҝ |
УГТ©Кұјд |
|
ЎЭ2500g |
NVP 15mgЈЁјҙ»мРьТә1.5mlЈ©Ј¬ГҝМм1ҙО |
ДёЗЧФРЖЪјҙҝӘКјУГТ©ХЯЈ¬УӨ¶щУҰ·юТ©ЦБіцЙъәу4Ў«6ЦЬЈ» ДёЗЧІъКұ»тХЯІъәуІЕҝӘКјУГТ©ХЯЈ¬УӨ¶щУҰ·юУГ6~12ЦЬЎЈ ДёЗЧІёИйЖЪОҙУҰУГҝ№ІЎ¶ҫТ©ОпЈ¬ФтУӨ¶щіЦРшУҰУГҝ№ІЎ¶ҫТ©ОпЦБДёИйО№СшНЈЦ№әу1ЦЬЎЈ |
|
Јј2500g ЗТЎЭ2000g |
NVP 10 mgЈЁјҙ»мРьТә1.0mlЈ©Ј¬ГҝМм1ҙО |
|
|
Јј2000g |
NVP 2 mg /kgЈЁјҙ»мРьТә0.2ml/kgЈ©Ј¬ГҝМм1ҙО |
ұн3. УӨ¶щФӨ·АУГТ©ҪЁТйјББҝЈәЖл¶а·т¶ЁЈЁAZTЈ©
|
іцЙъМеЦШ |
УГТ©јББҝ |
УГТ©Кұјд |
|
ЎЭ2500g |
AZT 15mgЈЁјҙ»мРьТә1.5mlЈ©Ј¬ГҝМм2ҙО |
ДёЗЧФРЖЪјҙҝӘКјУГТ©ХЯЈ¬УӨ¶щУҰ·юТ©ЦБіцЙъәу4~6ЦЬЈ» ДёЗЧІъКұ»тХЯІъәуІЕҝӘКјУГТ©ХЯЈ¬УӨ¶щУҰ·юУГ6~12ЦЬЎЈ ДёЗЧІёИйЖЪОҙУҰУГҝ№ІЎ¶ҫТ©ОпЈ¬ФтУӨ¶щіЦРшУҰУГҝ№ІЎ¶ҫТ©ОпЦБДёИйО№СшНЈЦ№әу1ЦЬЎЈ |
|
Јј2500g ЗТЎЭ2000g |
AZT 10mgЈЁјҙ»мРьТә1.0mlЈ©Ј¬ГҝМм2ҙО |
|
|
Јј2000g |
AZT 2mg/kgЈЁјҙ»мРьТә0.2ml/kgЈ©Ј¬ГҝМм2ҙО |
ИэЎўФРІъёҫҝ№ІЎ¶ҫЦОБЖөДПа№ШјмІв
ФРІъёҫҝ№ІЎ¶ҫУГТ©З°ЎўУГТ©№эіМЦРУҰҪшРРПа№ШөДјмІвЈ¬ІўҪбәПБЩҙІЦўЧҙ¶ФФРІъёҫёРИҫЧҙҝцҪшРРЖА№АЈ¬ТФұгИ·¶ЁУГТ©·Ҫ°ёәНјаІвЦОБЖР§№ыЎЈ
УГТ©З°Ј¬ҪшРРCD4+TБЬ°НПё°ыјЖКэЎўІЎ¶ҫФШБҝјмІвј°ЖдЛыПа№ШјмІвЈЁ°ьАЁСӘіЈ№жЎўДтіЈ№жЎўёО№ҰДЬЎўЙц№ҰДЬЎўСӘЦ¬ЎўСӘМЗөИЈ©ЎЈ
УГТ©№эіМЦРЈ¬ГҝИэёцФВҪшРР1ҙОCD4+TБЬ°НПё°ыјЖКэј°ЖдЛыПа№ШјмІвЈЁН¬З°Ј©ЎЈ
ФРНнЖЪЈ¬ҪшРР1ҙОІЎ¶ҫФШБҝјмІвЈ¬ІўФЪ·ЦГдЗ°»сөГјмІвҪб№ыЎЈ
ЛДЎў°ІИ«ЦъІъ·юОс
ФРЖЪМṩід·ЦөДЧЙСҜЈ¬°пЦъёРИҫФРёҫј°ЖдјТИЛҫЎФзИ·¶Ё·ЦГдТҪФәЈ¬ј°КұөҪТҪФәҙэІъЎЈ
°¬ЧМІЎёРИҫІ»ЧчОӘКөК©ЖК№¬ІъөДЦёХчЎЈ¶ФУЪФРФзЎўЦРЖЪТСҫӯҝӘКјҝ№ІЎ¶ҫЦОБЖЎў№жВЙ·юУГТ©ОпЎўГ»УР°¬ЧМІЎБЩҙІЦўЧҙЈ¬»тФРНнЖЪІЎ¶ҫФШБҝЈј1000ҝҪұҙКэ/әБЙэЈ¬»тТСҫӯБЩІъөДФРІъёҫЈ¬І»ҪЁТйК©РРЖК№¬ІъЎЈ
·ЦГд№эіМЦРУҰСПГЬ№ЫІмІў»эј«ҙҰАнІъіМЈ¬ҫЎБҝұЬГвҝЙДЬФцјУДёУӨҙ«ІҘОЈПХөДЛрЙЛРФІЩЧчЈ¬°ьАЁ»бТхІаЗРЎўИЛ№ӨЖЖДӨЎўК№УГМҘН·ОьТэЖч»тІъЗҜЎў№¬ДЪМҘ¶щН·ЖӨјаІвөИЎЈРВЙъ¶щіцЙъәуУҰј°КұК№УГБч¶ҜөДОВЛ®ҪшРРЗеПҙЈ¬УГПҙ¶ъЗтЗеАнұЗЗ»ј°ҝЪЗ»ХіДӨЈ¬Лх¶МРВЙъ¶щҪУҙҘДёЗЧСӘТәЎўСтЛ®ј°·ЦГЪОпөДКұјдЎЈЗеАн№эіМІЩЧчКЦ·ЁУҰЗбИбЈ¬ұЬГвЛрЙЛЖӨ·фәНрӨДӨЎЈ
ТҪОсИЛФұКөК©ЖХұйРФ·А»ӨҙлК©Ј¬јУЗҝёцИЛ·А»ӨЈ¬јхЙЩЦ°Төұ©В¶ЎЈ
ОеЎўУӨ¶щО№СшЧЙСҜУлЦёөј
Мбі«ИЛ№ӨО№СшЈ¬ұЬГвДёИйО№СшЈ¬¶Еҫш»мәПО№СшЎЈ
ТҪОсИЛФұУҰ¶Ф°¬ЧМІЎёРИҫФРІъёҫј°ЖдјТИЛҪшРРУӨ¶щО№Сш·ҪКҪөДҝЙҪУКЬРФЎўЦӘК¶әНјјДЬЎўҝЙёәөЈРФЎўҝЙіЦРшРФөИМхјюөДЧЫәПЖА№АЈ¬ёшУијјКхЦёөјЎЈ
¶ФСЎФсИЛ№ӨО№СшХЯЈ¬ЦёөјХэИ·іеЕдЎўЖчҫЯЗеҪаПы¶ҫөИЎЈ¶ФСЎФсДёИйО№СшХЯЈ¬ТӘЧцәГід·ЦөДЧЙСҜЈ¬ЗҝөчО№СшЖЪјдДёЗЧ»тУӨ¶щјбіЦ·юУГҝ№ІЎ¶ҫТ©ОпЈ¬ЦёөјХэИ·өДҙҝДёИйО№Сш·ҪКҪәНИй·ҝ»ӨАнЎЈёжЦӘДёИйО№СшКұјдЧоәГІ»і¬№э6ёцФВЈ¬Н¬Кұ»эј«ҙҙФмМхјюЈ¬ҫЎФзёДОӘИЛ№ӨО№СшЎЈ
БщЎў¶щНҜ°¬ЧМІЎёРИҫЧҙҝцјаІвәНЛж·Г
ёчј¶ТҪБЖОАЙъ»ъ№№УҰҪ«°¬ЧМІЎёРИҫФРІъёҫЛщЙъ¶щНҜДЙИлёЯОЈ№ЬАнЈ¬УЪ¶щНҜВъ1Ўў3Ўў6Ўў9Ўў12әН18ФВБдКұЈ¬·ЦұрҪшРРЛж·ГәНМеёсјмІйЈ¬№ЫІмУРОЮёРИҫЦўЧҙіцПЦЎЈ
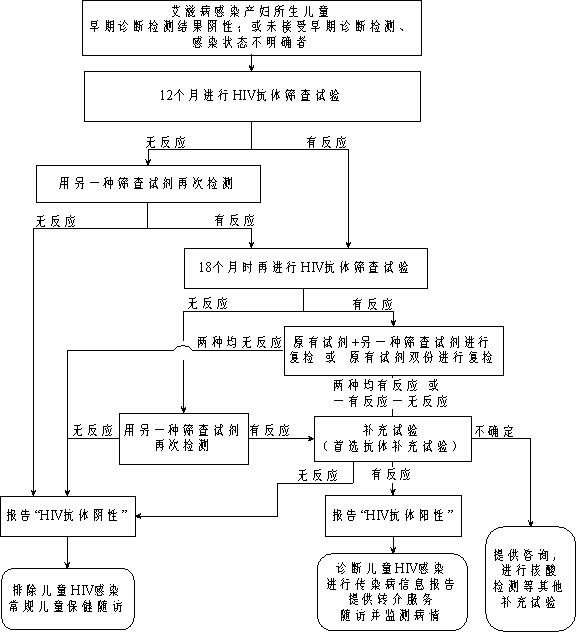
°ҙХХЎ¶УӨ¶щ°¬ЧМІЎёРИҫФзЖЪХп¶П№ӨЧч·Ҫ°ёЎ·өДПа№ШјјКхәНКұјдТӘЗ󣬶ФЛщЙъ¶щНҜУЪіцЙъәу6ЦЬәН3ёцФВКұЈ¬·ЦұрІЙјҜСӘұкұҫЈ¬ҪшРРУӨ¶щёРИҫФзЖЪХп¶ПЎЈПкјыНј6УӨ¶щ°¬ЧМІЎёРИҫФзЖЪХп¶ПјмІвј°·юОсБчіМЎЈ
ОҙҪшРРУӨ¶щФзЖЪХп¶ПјмІв»тУӨ¶щФзЖЪХп¶ПјмІвҪб№ыОӘТхРФөД¶щНҜЈ¬УҰУЪ12Ўў18ФВБдҪшРР°¬ЧМІЎҝ№МеЙёІйј°ұШТӘөДІ№ідКФСйЈ¬ТФГчИ·°¬ЧМІЎёРИҫЧҙМ¬ЎЈ¶щНҜҝ№МејмІвј°·юОсБчіМјыНј7ЎЈ

Нј6. °¬ЧМІЎёРИҫФРІъёҫЛщЙъ¶щНҜ°¬ЧМІЎёРИҫФзЖЪХп¶ПјмІвј°·юОсБчіМ
Нј7. °¬ЧМІЎёРИҫФРІъёҫЛщЙъ¶щНҜ°¬ЧМІЎҝ№МејмІвј°·юОсБчіМ
ЖЯЎўУҰУГёҙ·ҪРВЕөГчФӨ·А»ъ»бРФёРИҫ
УҰУГ¶ФПу°ьАЁЈәCD4+ TБЬ°НПё°ыјЖКэ<200ёцПё°ы/mm3өД°¬ЧМІЎёРИҫФРІъёҫәНCD4+TБЬ°НПё°ы°Щ·ЦұИ<15%өД°¬ЧМІЎёРИҫ¶щНҜЎЈ
ёҙ·ҪРВЕөГчУГТ©·Ҫ·ЁЎўНЈТ©ЦёХчј°ЧўТвКВПоөИПкјыЎ¶ФӨ·А°¬ЧМІЎДёУӨҙ«ІҘјјКхЦёөјКЦІбЎ·ЎЈ
ёҪјю4
ФӨ·АГ·¶ҫДёУӨҙ«ІҘёЙФӨ·юОсјјКхТӘөг
Т»ЎўГ·¶ҫёРИҫФРІъёҫЦОБЖ·Ҫ°ё
ЈЁТ»Ј©НЖјц·Ҫ°ёЎЈ
Т»ө©·ўПЦёРИҫЈ¬јҙҝМҝӘКјЦОБЖЈ¬ҝЙСЎФсТФПВИОТвТ»ЦЦТ©ОпЎЈ
1. ЬРРЗЗаГ№ЛШ240НтөҘО»Ј¬·ЦБҪІаНОІҝјЎДЪЧўЙдЈ¬ГҝЦЬ1ҙОЈ¬Б¬Рш3ҙООӘ1ёцБЖіМЎЈ
2. ЖХВіҝЁТтЗаГ№ЛШGЈ¬80НтөҘО»/ИХЈ¬јЎДЪЧўЙдЈ¬Б¬Рш15ИХОӘ1ёцБЖіМЎЈ
ЈЁ¶юЈ©Мжҙъ·Ҫ°ёЎЈ
1. ИфГ»УРЗаГ№ЛШЈ¬ҝЙУГН·жЯЗъЛЙЈ¬1g/ИХЈ¬јЎДЪЧўЙд»тҫІВцёшТ©Ј¬Б¬Рш10ИХОӘ1ёцБЖіМЈ»
2. ЗаГ№ЛШ№эГфХЯЈәҝЙУГәмГ№ЛШЦОБЖЈЁҪыУГЛД»·ЛШЎў¶аОч»·ЛШЈ©Ј¬әмГ№ЛШГҝҙО500mgЈ¬ГҝИХ4ҙОЈ¬ҝЪ·юЈ¬Б¬·ю15ИХОӘ1ёцБЖіМЎЈ
ЈЁИэЈ©ЦОБЖКұЖЪЎЈ
1. ФРФзЖЪ·ўПЦөДёРИҫФРёҫЈ¬УҰУЪФРФзЖЪәНФРНнЖЪёчҪшРР1ёцБЖіМөДЦОБЖЈ¬№І2ёцБЖіМЎЈ
2. ФРЦРЎўНнЖЪ·ўПЦөДёРИҫФРёҫЈ¬УҰБўҝМёшУи2ёцБЖіМөДЦОБЖЈ¬2ёцЦОБЖБЖіМЦ®јдРијдёф4ЦЬТФЙПЈЁЧоЙЩјдёф2ЦЬЈ©Ј¬өЪ2ёцБЖіМУҰөұФЪФРНнЖЪҝӘКјЈ¬ЧоәГФЪ·ЦГдЗ°Т»ёцФВНкіЙЎЈ
3. БЩІъКұ·ўПЦөДёРИҫФРІъёҫЈ¬ТІТӘБўјҙёшУи1ёцБЖіМөДЦОБЖЎЈ
4. ЦОБЖ№эіМЦРёҙ·ў»тЦШРВёРИҫХЯЈ¬ТӘЧ·јУ1ёцБЖіМөДЦОБЖЎЈ
5. јИНщёРИҫөДФРІъёҫЈ¬ТІТӘј°КұёшУи1ёцБЖіМөДЦОБЖЎЈ
ЈЁЛДЈ©ЧўТвКВПоЎЈ
1. Н¬КұВъЧгТФПВМхјюОӘ№ж·¶ЦОБЖЈәўЩУҰУГЧгБҝЗаГ№ЛШЦОБЖЈ»ўЪФРЖЪҪшРР2ёцБЖіМЦОБЖЈ¬2ёцБЖіМЦ®јдРијдёф2ЦЬТФЙПЈ»ўЫөЪ2ёцБЖіМФЪФРНнЖЪҪшРРІўНкіЙЎЈ
2. ЬРРЗЗаГ№ЛШЦОБЖЖЪјдЈ¬ИфЦР¶ПЦОБЖі¬№э1ЦЬЈ¬»тІЙУГЖдЛы·Ҫ°ёҪшРРЦОБЖКұЈ¬ГҝёцБЖіМЦОБЖЖЪјдТЕВ©ЦОБЖ1ИХ»ті¬№э1ИХЈ¬ТӘҙУФЩҙОЦОБЖҝӘКјКұјдЖрЦШРВјЖЛгЦОБЖБЖіМЎЈ
3. ЦОБЖЖЪјдУҰөұ¶ЁЖЪЛж·ГЎЈГҝФВЧц1ҙО·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСй¶ЁБҝјмІвЈ¬№ЫІмөО¶Иұд»ҜЈ¬ЕР¶ПУРОЮёҙ·ў»тФЩёРИҫЎЈЛж·Г№эіМЦРЈ¬Из№ы·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйөО¶ИЙПЙэ»тҪб№ыУЙТхЧӘСфЈ¬ФтЕР¶ПОӘФЩҙОёРИҫ»тёҙ·ўЈ¬УҰөұБўјҙФЩҝӘКј1ёцБЖіМөДГ·¶ҫЦОБЖЎЈ
4. ёРИҫФРІъёҫ·ЦГдЗ°ұШРлҪшРР·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСй¶ЁБҝјмІвЈ¬ТФұгУлЛщЙъРВЙъ¶щ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСй¶ЁБҝјмІвҪб№ыҪшРРұИҪПЈ¬ЧчОӘәуРшХпЦОөДТАҫЭЎЈ
¶юЎў¶щНҜФӨ·АРФЦОБЖ
1Ј®ЦОБЖ¶ФПуЈәФРЖЪОҙҪУКЬ№ж·¶РФЦОБЖЈ¬°ьАЁФРЖЪОҙҪУКЬИ«іМЎўЧгБҝөДЗаГ№ЛШЦОБЖЈ¬»тҪУКЬ·ЗЗаГ№ЛШ·Ҫ°ёЦОБЖЈ¬»тФЪ·ЦГдЗ°1ёцФВДЪІЕҪшРРҝ№Г·¶ҫЦОБЖөДФРІъёҫЛщЙъ¶щНҜЈ»ФРЖЪҪУКЬ№э№ж·¶РФЦОБЖЈ¬іцЙъКұ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйСфРФЎўөО¶ИІ»ёЯУЪДёЗЧ·ЦГдЗ°өО¶ИөД4ұ¶өД¶щНҜЎЈ
2. ЦОБЖ·Ҫ°ёЈәЬРРЗЗаГ№ЛШGЈ¬5НтөҘО»/З§ҝЛМеЦШЈ¬1ҙОјЎДЪЧўЙдЈЁ·ЦБҪІаНОјЎЈ©ЎЈ
ИэЎў¶щНҜГ·¶ҫёРИҫЧҙҝцјаІвәНЛж·Г
Г·¶ҫёРИҫФРІъёҫЛщЙъ¶щНҜЧФіцЙъКұҝӘКјЈ¬¶ЁЖЪҪшРРГ·¶ҫСӘЗеС§јмІвәНЛж·ГЈ¬ЦұЦБЕЕіэ»тХп¶ППИМмГ·¶ҫЎЈПкјыНј8ЎЈ
ЛДЎўПИМмГ·¶ҫөДХп¶ПУлЦОБЖ
ЈЁТ»Ј©ПИМмГ·¶ҫХп¶ПЎЈ
Г·¶ҫёРИҫФРІъёҫЛщЙъ¶щНҜ·ыәППВБРИОәОТ»ПоЈ¬ҝЙХп¶ПОӘПИМмГ·¶ҫЈә
ЈЁ1Ј©¶щНҜөДЖӨ·фрӨДӨЛрәҰ»тЧйЦҜұкұҫ°өКУТ°ПФОўҫөЈЁ»т¶ЖТшИҫЙ«Ј©јмІвөҪГ·¶ҫВЭРэМеЈ»
ЈЁ2Ј©Г·¶ҫВЭРэМеIgMҝ№МејмІвСфРФЈ»
ЈЁ3Ј©іцЙъКұ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСй¶ЁБҝјмІвҪб№ыСфРФЈ¬өО¶ИЎЭДёЗЧ·ЦГдЗ°өО¶ИөД4ұ¶Ј¬ЗТГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйҪб№ыСфРФЈ»
ЈЁ4Ј©іцЙъКұІ»ДЬХп¶ППИМмГ·¶ҫөД¶щНҜЈ¬ИОәОТ»ҙОЛж·Г№эіМЦР·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйУЙТхЧӘСф»төО¶ИЙПЙэЗТГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйСфРФЈ»
ЈЁ5Ј©18ФВБдЗ°І»ДЬХп¶ППИМмГ·¶ҫөД¶щНҜЈ¬18ФВБдәуГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйИФСфРФЎЈ
ЈЁ¶юЈ©ПИМмГ·¶ҫ»ј¶щөДЦОБЖ·Ҫ°ёЎЈ
1. ДФј№ТәХэіЈХЯЎЈ
ЬРРЗЗаГ№ЛШGЈ¬5НтөҘО»/З§ҝЛМеЦШЈ¬1ҙОјЎДЪЧўЙдЈЁ·ЦБҪІаНОјЎЈ©ЎЈ

Нј8Г·¶ҫёРИҫФРІъёҫЛщЙъ¶щНҜЛж·Гј°ПИМмГ·¶ҫёРИҫЧҙМ¬јаІвНј
2. ДФј№ТәТміЈХЯЎЈ
ҝЙСЎФсТФПВИОТвТ»ЦЦТ©ОпЎЈ
ЈЁ1Ј©Л®јБЗаГ№ЛШGЈ¬ГҝҙО5НтөҘО»/З§ҝЛМеЦШЈ¬Гҝ8РЎКұ1ҙОЈЁ7ИХДЪРВЙъ¶щЈ¬Гҝ12РЎКұ1ҙОЈ©Ј¬ҫІВцЧўЙдЈ¬Б¬Рш10~14ИХЎЈ
ЈЁ2Ј©ЖХВіҝЁТтЗаГ№ЛШGЈ¬ГҝҙО5НтөҘО»/З§ҝЛМеЦШЈ¬ГҝИХ1ҙОЈ¬јЎДЪЧўЙдЈ¬Б¬Рш10~14ИХЎЈ
ЦОБЖЖЪјдТЕВ©ЦОБЖ1ИХ»ті¬№э1ИХЈ¬ФтҙУФЩҙОЦОБЖҝӘКјКұјдЖрЦШРВјЖЛгЦОБЖБЖіМЎЈ
3. ИзОЮМхјюјмІйДФј№ТәЈ¬°ҙДФј№ТәТміЈХЯЦОБЖЎЈ
ёҪјю5
ФӨ·АТТёОДёУӨҙ«ІҘёЙФӨ·юОсјјКхТӘөг
Т»ЎўТТёОёРИҫФРІъёҫёЙФӨ
ОӘТТёОІЎ¶ҫұнГжҝ№ФӯСфРФөДёРИҫФРІъёҫМṩТТёОІЎ¶ҫёРИҫСӘЗеС§ұкЦҫОпЈЁБҪ¶Ф°лЈ©әНёО№ҰДЬјмІвЈ¬УРМхјюөДөШЗшҝЙҪшРРТТёОІЎ¶ҫФШБҝЈЁHBV DNAЈ©јмІвЈ¬ұШТӘКұЧӘҪйЦБҙ«ИҫІЎЧЁҝЖҪУКЬПаУҰөДХпБЖ·юОсЎЈФРІъёҫЧўЙдТТёОГвТЯЗтө°°ЧГ»УРФӨ·АДёУӨҙ«ІҘЧчУГЎЈ
¶юЎўТТёОёРИҫФРІъёҫЛщЙъ¶щНҜёЙФӨ
ЈЁТ»Ј©ТТёОГвТЯЗтө°°ЧЧўЙдЎЈ
ЛщУРТТёОІЎ¶ҫұнГжҝ№ФӯСфРФФРІъёҫЛщЙъРВЙъ¶щЈ¬ҫщУҰУЪіцЙъәу24РЎКұДЪЈЁЧоәГКЗ12РЎКұДЪЈ¬ФҪФзФҪәГЈ©ЧўЙдТТёОГвТЯЗтө°°Ч100№ъјКөҘО»ЎЈЧўЙд·Ҫ·ЁОӘјЎДЪЧўЙдЎЈЧўТвұШРлУлТТёОТЯГзөДЧўЙдІҝО»І»Н¬Ј¬ТІІ»ҝЙУлТТёОТЯГзОьИлН¬Т»ЧўЙдЖчДЪЧўЙдЎЈ
ЈЁ¶юЈ©ТТёОТЯГзҪУЦЦЎЈ
ЛщУРТТёОІЎ¶ҫұнГжҝ№ФӯСфРФФРІъёҫЛщЙъРВЙъ¶щЈ¬ҫщУҰ°ҙХХЎ¶ФӨ·АҪУЦЦ№ж·¶Ў·ЦРРВЙъ¶щТТёОТЯГзГвТЯіМРтЈ¬НкіЙ3јБҙОТТёОТЯГзҪУЦЦЎЈУРМхјюөДөШЗшЈ¬ФЪНкіЙөЪ3јБҙОТТёОТЯГзҪУЦЦәу1~6ёцФВЈ¬јҙ¶щНҜ7ФВБдЦБ1ЦЬЛкЖЪјдЈ¬ҝЙҪшРРТТёОІЎ¶ҫёРИҫСӘЗеС§ұкЦҫОпЈЁБҪ¶Ф°лЈ©јмІвЈ¬ЕР¶ПГвТЯР§№ыЎЈ
ёҪјю6
әюДПКЎIPMTCTСфРФёц°ёЧӘҪйҝЁ
ЧӘҪйҝЁ ЈЁ»ъ№№БӘЈ©
ЧӘИл»ъ№№Јә ПЦУРОТФә·юОс¶ФПу ФЪОТФәТСҪУКЬ ·юОсЈ¬ТтЖдТӘөҪ№уөҘО» Ј¬ДвөҪ№уөҘО»јМРшҪУКЬ·юОсЈ¬ЗлёшУи°пЦъЈ¬ИзУРТЙОКЈ¬ЗлУлОТФәБӘПөЎЈОТөҘО»өДФрИОТҪЙъКЗ Ј¬БӘПөөз»°КЗ ЎЈ
ЦВАс
ҫӯКЦИЛЗ©ГыЈә ЧӘіцөҘО»ЈЁёЗХВЈ©Јә
БӘПөөз»°Јә КЦ»ъЈә
Дк ФВ ИХ
ЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯ
ЧӘҪйҝЁ ЈЁІЎИЛБӘЈ©
ЧӘИл»ъ№№Јә ПЦУРОТФә·юОс¶ФПу ФЪОТФәТСҪУКЬ ·юОсЈ¬ТтЖдТӘөҪ№уөҘО» Ј¬ДвөҪ№уөҘО»јМРшҪУКЬ·юОсЈ¬ЗлёшУи°пЦъЈ¬ИзУРТЙОКЈ¬ЗлУлОТФәБӘПөЎЈОТөҘО»өДФрИОТҪЙъКЗ Ј¬БӘПөөз»°КЗ ЎЈ
ЦВАс
ҫӯКЦИЛЗ©ГыЈә ЧӘіцөҘО»ЈЁёЗХВЈ©Јә
БӘПөөз»°Јә КЦ»ъЈә
Дк ФВ ИХ
ЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯЎӯ
ЧӘҪйҝЁЈЁ»ШЦҙБӘЈ©
ЧӘіц»ъ№№Јә №уөҘО»ЧӘҪйөД·юОс¶ФПу ТСУЪ Дк ФВ ИХөҪОТөҘО»ҪУКЬБЛ ·юОсЎЈОТөҘО»өДФрИОТҪЙъКЗ Ј¬БӘПөөз»°КЗ ЎЈ
ҫӯКЦИЛЗ©ГыЈә ЧӘіцөҘО»ЈЁёЗХВЈ©Јә
БӘПөөз»°Јә КЦ»ъЈә
Дк ФВ ИХ
ёҪјю7
ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘПа№ШұЁұнЙПұЁБчіМј°ТӘЗу
Т»ЎўФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘПа№ШұЁұнЙПұЁБчіМ
¶юЎўФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘПа№ШұЁұнЙПұЁКұПЮј°ТӘЗу
ЈЁТ»Ј©ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧчФВұЁұнЈЁұн1Ўўұн1-ўсЎўұн1-ўтЎўұн1-ўуЈ¬ұн2Ўўұн2-ўсЎўұн 2-ўтЈ©ЎЈ
ёчј¶ТҪБЖОАЙъ»ъ№№УҰГҝФВіхј°КұҪ«ЙПФВФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧчұЁұнЈЁұҫ»ъ№№МоРҙІҝ·ЦЈ©ЙПұЁЦБұҫПҪЗшөДПШЈЁКРЎўЗшЈ©ј¶ёҫУЧұЈҪЎ»ъ№№ЎЈёчј¶ёҫУЧұЈҪЎ»ъ№№ёәФрКХјҜЎўХыАнЎў»гЧЬәНЙуәЛәуЈ¬РОіЙЎ°ФӨ·А°¬ЧМІЎДёУӨҙ«ІҘ№ӨЧчФВұЁЈЁ»гЧЬЈ©ұнЎұЈЁұн1Ј©ј°Ў°ФӨ·АГ·¶ҫЎўТТёОДёУӨҙ«ІҘ№ӨЧчФВұЁЈЁ»гЧЬЈ©ұнЈЁұн2Ј©ЎұЈ¬ІўҫЎҝмНкіЙНшВзұЁёжЎЈёчКЎј¶ёҫУЧұЈҪЎ»ъ№№УҰУЪГҝФВ15ИХЗ°НкіЙұҫКЎёчАаФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧчФВұЁұнөДЦрј¶ЙуәЛЎў»гЧЬУлНшВзұЁёжЈ¬ІўЙПұЁЦБЦР№ъјІІЎФӨ·АҝШЦЖЦРРДёҫУЧұЈҪЎЦРРДЎЈ
ЈЁ¶юЈ©ФӨ·А°¬ЧМІЎЎўГ·¶ҫДёУӨҙ«ІҘПөБРёц°ёөЗјЗҝЁЎЈ
°¬ЧМІЎёРИҫФРІъёҫ/»йјмёҫЕ®»щұҫЗйҝцөЗјЗҝЁЈЁұн3-ўсЈ©УҰУЪ»сөГ°¬ЧМІЎёРИҫФРІъёҫ/»йјмёҫЕ®І№ідКФСйСфРФҪб№ыәу5ИХДЪМоРҙНкіЙЎЈ¶ФјИНщТСИ·ХпёРИҫХЯЈ¬ТІУҰФЪұҫҙОБЛҪвЖдёРИҫЧҙМ¬әу5ИХДЪМоРҙНкіЙЎЈ
°¬ЧМІЎёРИҫФРІъёҫИСЙпј°ЛщЙъУӨ¶щөЗјЗҝЁЈЁұн3-ўтЈ©УҰУЪ°¬ЧМІЎёРИҫФРІъёҫІъИмЖЪЈЁ·ЦГдЦБІъәу42ИХЈ©әуөД5ИХДЪМоРҙНкіЙЈ¬¶Ф·ўЙъЧФИ»БчІъЎўИЛ№ӨЦХЦ№ИСЙпЎўЛАНц»тК§·ГөИЖдЛыЗйҝцөД°¬ЧМІЎёРИҫФРІъёҫЈ¬УҰФЪИ·¶ЁЖдҪбҫЦәуөД5ИХДЪМоРҙНкіЙЎЈ
°¬ЧМІЎёРИҫІъёҫј°ЛщЙъ¶щНҜЛж·ГөЗјЗҝЁЈЁұн3-ўуЈ©УҰ·ЦұрУЪ°¬ЧМІЎёРИҫІъёҫЛщЙъ¶щНҜВъ1Ўў3Ўў6Ўў9Ўў12Ўў18ёцФВәу 5ИХДЪМоРҙНкіЙЎЈ
Из°¬ЧМІЎёРИҫІъёҫЛщЙъ¶щНҜТСВъ18ФВБдЈ¬ФЪІ»БЛҪвЖдЧоЦХҪбҫЦЗ°Ј¬УҰФЪЛжәуөД3ёцФВДЪБ¬РшЛж·Г3ҙОЈ¬ФЪИФОЮ·ЁөГөҪёГ¶щНҜөДХп¶ПҪб№ыј°Па№ШРЕПўөДЗйҝцПВЈ¬ҝЙ¶ЁТеОӘ¶щНҜК§·ГЈ¬Н¬КұУҰУЪЧоәуТ»ҙОЛж·ГәуөД5ИХДЪМоРҙНкіЙЎ°°¬ЧМІЎёРИҫІъёҫј°ЛщЙъ¶щНҜЛж·ГөЗјЗҝЁЎұЈЁұн3-ўуЈ©ЎЈ
Г·¶ҫёРИҫФРІъёҫөЗјЗҝЁЈЁұн4-ўсЈ©УҰУЪГ·¶ҫёРИҫФРІъёҫГчИ·ёРИҫәуөД5ИХДЪМоРҙНкіЙЎЈ
Г·¶ҫёРИҫФРІъёҫј°ЛщЙъРВЙъ¶щөЗјЗҝЁЈЁұн4-ўтЈ©УҰУЪГ·¶ҫёРИҫФРІъёҫ·ЦГдәуөД5ИХДЪМоРҙНкіЙЈ¬ФЪ·ЦГдКұЙРОҙНкіЙұҫЦОБЖБЖіМХЯЈ¬ФЪНкіЙБЖіМәуөД5ИХДЪМоРҙНкіЙЎЈ¶Ф·ўЙъЧФИ»БчІъЎўИЛ№ӨЦХЦ№ИСЙпЎўЛАНц»тК§·ГөИЗйҝцөДГ·¶ҫёРИҫФРІъёҫЈ¬УҰФЪИ·¶ЁЖдҪбҫЦәуөД5ИХДЪМоРҙНкіЙЎЈ
ОӘБЛҪвГ·¶ҫёРИҫІъёҫЛщЙъ¶щНҜөДЙъҙжЧҙҝцј°ПИМмГ·¶ҫХп¶ПЗйҝцЈ¬РиТӘУЪ¶щНҜіцЙъәуөД3Ўў6Ўў9Ўў12Ўў15Ўў18ФВКұМṩЛж·Гј°Г·¶ҫПа№ШјмІв·юОсЈ¬ІўФЪГҝҙОЛж·ГәуөД5ИХДЪЈ¬ј°КұМоРҙЎ°Г·¶ҫёРИҫІъёҫЛщЙъ¶щНҜЛж·ГөЗјЗҝЁЎұЈЁұн4-ўуЈ©ЎЈ
ИзГ·¶ҫёРИҫІъёҫЛщЙъ¶щНҜТСВъ18ФВБдЈ¬ФЪІ»БЛҪвЖдЧоЦХҪбҫЦЗ°Ј¬УҰФЪЛжәуөД3ёцФВДЪБ¬РшЛж·Г3ҙОЈ¬ФЪИФОЮ·ЁөГөҪёГ¶щНҜөДХп¶ПҪб№ыј°Па№ШРЕПўЈ¬ҝЙ¶ЁТеОӘ¶щНҜК§·ГЈ¬Н¬КұУҰУЪЧоәуТ»ҙОЛж·ГәуөД5ИХДЪМоРҙНкіЙЎ°Г·¶ҫёРИҫІъёҫЛщЙъ¶щНҜЛж·ГөЗјЗҝЁЎұЈЁұн4-ўуЈ©ЎЈ
ёчТҪБЖОАЙъ»ъ№№УҰУЪёчАаёц°ёөЗјЗҝЁөДЦҪЦК°жМоРҙНкіЙәу5ИХДЪЈ¬НкіЙНшВзұЁёж»тҪ«ЦҪЦКөЗјЗҝЁҪ»УЙПҪЗшёҫУЧұЈҪЎ»ъ№№НкіЙНшВзұЁёжЎЈ
ПШёҫУЧұЈҪЎ»ъ№№әНЈЁ»тЈ©ОАЙъјЖЙъРРХюІҝГЕУҰ¶ФёчТҪБЖОАЙъ»ъ№№ЛжКұНЁ№эНшВзұЁёжөДёчАаЎ°ёц°ёөЗјЗҝЁЎұЈ¬ҪшРРЦрј¶НшВзЙуәЛЈ¬ІўУЪТҪБЖОАЙъ»ъ№№НшВзұЁёжәуөД10ИХДЪНкіЙКЎј¶ЦХЙуЎЈ
ПШЎўКРБҪј¶ёҫУЧұЈҪЎ»ъ№№ёәФрҪ«Па№ШөДФӯКјөЗјЗј°ПөБРёц°ёөЗјЗҝЁұЈГЬБфҙжұё°ёЈ¬Ј¬І»ФЩҪ«ЦҪЦКұЁұнјДНщКЎј¶ЎЈ
ЈЁИэЈ©МоұЁТӘЗуЎЈ
МоРҙЙПКц№ӨЧчФВұЁұнУлПөБРёц°ёөЗјЗҝЁКұЈ¬ТӘЗуК№УГА¶Й«»тәЪЙ«З©ЧЦұКЎўёЦұКЈ¬ДЪИЭНкХыЎўЧјИ·Ј¬ЧЦјЈЗеіюЈ¬МоұЁИЛРиЗ©ГыЈ¬ІўјУёЗөҘО»№«ХВЈ¬ј°КұЙПұЁЎЈ
ИэЎўФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘПа№ШұЁұн
ұн1 ФӨ·А°¬ЧМІЎДёУӨҙ«ІҘ№ӨЧчФВұЁЈЁ»гЧЬЈ©ұнЈЁУЙёҫУЧұЈҪЎ»ъ№№»гЧЬЈ©
КЎЈЁЧФЦОЗшЎўЦұПҪКРЈ© КРЈЁПШЈ©
Дк ФВ
|
ұаәЕ |
По Дҝ |
ИЛКэ |
ЦёұкЛөГч |
||
|
1. |
»йЗ°ұЈҪЎ |
ҪУКЬ»йЗ°ұЈҪЎИЛКэ |
ДР |
|
УЙұн1ЁCўс»гЧЬ»сөГЎЈ |
|
2. |
Е® |
|
|||
|
3. |
ҪУКЬ°¬ЧМІЎЧЙСҜИЛКэ |
ДР |
|
||
|
4. |
Е® |
|
|||
|
5. |
ҪУКЬHIVјмІвИЛКэ |
ДР |
|
||
|
6. |
Е® |
|
|||
|
7. |
HIVјмІвСфРФИЛКэ |
ДР |
|
||
|
8. |
Е® |
|
|||
|
9. |
ФРЖЪ |
ҪУКЬіхҙОІъЗ°ұЈҪЎөДФРёҫКэ |
|
УЙұн1ЁCўт»гЧЬ»сөГЎЈ |
|
|
10. |
ҪУКЬ°¬ЧМІЎЧЙСҜФРёҫКэ |
|
|||
|
11. |
ҪУКЬHIVјмІвФРёҫКэ |
|
|||
|
12. |
HIVјмІвСфРФФРёҫКэ |
|
|||
|
13. |
ЧЎФә·ЦГд |
ЧЎФә·ЦГдІъёҫКэ |
|
||
|
14. |
ФРЖЪҪУКЬ°¬ЧМІЎЧЙСҜІъёҫКэ |
|
|||
|
15. |
ФРЖЪҪУКЬHIVјмІвІъёҫКэ |
|
|||
|
16. |
ЖдЦРФР12ЦЬЗ°ҪУКЬ°¬ЧМјмІвІъёҫКэ |
|
|||
|
17. |
ФР12-28ЦЬҪУКЬ°¬ЧМІЎјмІвІъёҫКэ |
|
|||
|
18. |
ҪцІъКұҪУКЬ°¬ЧМІЎЧЙСҜІъёҫКэ |
|
|||
|
19. |
ҪцІъКұҪУКЬHIVјмІвІъёҫКэ |
|
|||
|
20. |
ҪцІъКұHIVјмІвСфРФІъёҫКэ |
|
|||
|
21. |
HIVјмІвСфРФІъёҫЧЬКэ |
|
|||
|
22. |
ЧЎФә·ЦГд»оІъКэ |
|
|||
|
23. |
HIVСфРФІъёҫЛщЙъ»оІъКэ |
|
|||
|
24. |
·ЗЧЎФә·ЦГд |
·ЗЧЎФә·ЦГдІъёҫКэ |
|
УЙұн1ЁCўу»гЧЬ»сөГЎЈ |
|
|
25. |
ФРЖЪҪУКЬ°¬ЧМІЎЧЙСҜІъёҫКэ |
|
|||
|
26. |
ФРЖЪҪУКЬHIVјмІвІъёҫКэ |
|
|||
|
27. |
ЖдЦРФР12ЦЬЗ°ҪУКЬ°¬ЧМјмІвІъёҫКэ |
|
|||
|
28. |
ФР12-28ЦЬҪУКЬ°¬ЧМІЎјмІвІъёҫКэ |
|
|||
|
29. |
ҪцІъКұҪУКЬHIVјмІвІъёҫКэ |
|
|||
|
30. |
ҪцІъКұHIVјмІвСфРФІъёҫКэ |
|
|||
|
31. |
HIVјмІвСфРФІъёҫКэ |
|
|||
|
32. |
·ЗЧЎФә·ЦГд»оІъКэ |
|
|||
|
33. |
HIVСфРФІъёҫЛщЙъ»оІъКэ |
|
|||
|
34. |
өШЗшІъёҫЧЬКэ |
|
|||
|
35. |
өШЗш»оІъЧЬКэ |
|
|||
МоұЁКұјдЈә МоұЁИЛЈә
МоұЁөҘО»ёәФрИЛЈә МоұЁөҘО»ЈЁёЗХВЈ©Јә
ұн1ЁCўс ФӨ·А°¬ЧМІЎДёУӨҙ«ІҘ№ӨЧчФВұЁұн
ЈЁУЙ»йЗ°ұЈҪЎ»ъ№№МоРҙЈ©
КРЈЁПШЈ© ТҪФәЈЁёҫУЧұЈҪЎФәЈ© Дк ФВ
|
ұаәЕ |
По Дҝ |
|
ИЛКэ |
|
1. |
ҪУКЬ»йЗ°ұЈҪЎИЛКэ |
ДР |
|
|
2. |
Е® |
|
|
|
3. |
ЖдЦРҪУКЬ°¬ЧМІЎЧЙСҜИЛКэ |
ДР |
|
|
4. |
Е® |
|
|
|
5. |
ЖдЦРҪУКЬHIVјмІвИЛКэ |
ДР |
|
|
6. |
Е® |
|
|
|
7. |
ЖдЦРHIVјмІвСфРФИЛКэ |
ДР |
|
|
8. |
Е® |
|
МоұЁКұјдЈә МоұЁИЛЈә
МоұЁөҘО»ёәФрИЛЈә МоұЁөҘО»ЈЁёЗХВЈ©Јә
ұн1ЁCўт ФӨ·А°¬ЧМІЎДёУӨҙ«ІҘ№ӨЧчФВұЁұн
ЈЁУЙЦъІъ»ъ№№МоРҙЈ©
КРЈЁПШЈ© ТҪФәЈЁёҫУЧұЈҪЎФәЈ© Дк ФВ
|
ұаәЕ |
По Дҝ |
ИЛКэ |
ЦёұкЛөГч |
|
|
9. |
ФР
ЖЪ |
ҪУКЬіхҙОІъЗ°ұЈҪЎөДФРёҫКэ |
|
ЦёіхҙОҪУКЬФРЖЪұЈҪЎ·юОсөДФРёҫИЛКэЎЈ |
|
10. |
ҪУКЬ°¬ЧМІЎЧЙСҜФРёҫКэ |
|
ТФ°¬ЧМІЎјмІвПа№ШёжЦӘөЗјЗ»тЧЙСҜөЗјЗ»тЖдЛыјЗВјЧКБПОӘТАҫЭЎЈ |
|
|
11. |
ҪУКЬHIVјмІвФРёҫКэ |
|
ФРЖЪіхҙОҪУКЬHIVјмІвөДФРёҫИЛКэЈ¬ТФ°¬ЧМІЎјмІвҪб№ыұЁёжөҘОӘТАҫЭЎЈ |
|
|
12. |
HIVјмІвСфРФФРёҫКэ |
|
°ьАЁЛщУРФЪФРЖЪҫӯHIVІ№ідКФСйјмІвСфРФөДФРёҫЈ¬ОЮВЫЖдИСЙпҪбҫЦИзәОЎЈ |
|
|
13. |
ЧЎ
Фә
·Ц
Гд |
ЧЎФә·ЦГдІъёҫКэ |
|
°ьАЁФЪұҫ»ъ№№ЧЎФә·ЦГдөДЛщУРІъёҫЈЁә¬ЎЭ28ФРЦЬТэІъөДІъёҫЈ©ЎЈ |
|
14. |
ФРЖЪҪУКЬ°¬ЧМІЎЧЙСҜІъёҫКэ |
|
ұҫ»ъ№№ЧЎФә·ЦГдІъёҫЦРФЪФРЖЪҪУКЬ°¬ЧМІЎЧЙСҜөДИЛКэЈ¬ТАҫЭФРЖЪёжЦӘөЗјЗЎўЧЙСҜјЗВјј°Па№ШРЕПўЧКБПОӘТАҫЭЎЈ |
|
|
15. |
ФРЖЪҪУКЬHIVјмІвІъёҫКэ |
|
ұҫ»ъ№№ЧЎФә·ЦГдІъёҫЦРФЪФРЖЪҪУКЬHIVјмІвөДИЛКэЎЈ |
|
|
16. |
ЖдЦРФР12ЦЬЗ°ҪУКЬHIVјмІвІъёҫКэ |
|
ұҫ»ъ№№ЧЎФә·ЦГдІъёҫЦРФЪФР12ЦЬЗ°ҪУКЬHIVјмІвөДИЛКэЎЈ |
|
|
17. |
ФР12-28ЦЬҪУКЬHIVјмІвІъёҫКэ |
|
ұҫ»ъ№№ЧЎФә·ЦГдІъёҫЦРФЪФР12-28ЦЬҪУКЬHIVјмІвөДИЛКэЎЈ |
|
|
18. |
ҪцІъКұҪУКЬ°¬ЧМІЎЧЙСҜІъёҫКэ |
|
ұҫ»ъ№№ЧЎФә·ЦГдІъёҫЦРФЪФРЖЪОҙҪУКЬ°¬ЧМІЎЧЙСҜУлјмІвЈ¬ҪцФЪЧЎФә·ЦГдКұІЕҪУКЬ°¬ЧМІЎЧЙСҜөДІъёҫИЛКэЈ¬ТФІъКұөЗјЗ»тіцҫЯПа№ШРЕПўІДБПОӘТАҫЭНіјЖЎЈ |
|
|
19. |
ҪцІъКұҪУКЬHIVјмІвІъёҫКэ |
|
ұҫ»ъ№№ЧЎФә·ЦГдІъёҫЦРФЪФРЖЪОҙҪУКЬHIVјмІвЈ¬ҪцФЪЧЎФә·ЦГдКұІЕҪУКЬёГјмІвөДІъёҫИЛКэЈ¬ТАҫЭ·ЦГдөЗјЗј°°¬ЧМІЎјмІвҪб№ыұЁёжөҘМоРҙЎЈ |
|
|
20. |
ҪцІъКұHIVјмІвСфРФІъёҫКэ |
|
ұҫ»ъ№№ЧЎФә·ЦГдІъёҫЦРФЪФРЖЪОҙҪУКЬHIVјмІвЈ¬ҪцФЪЧЎФә·ЦГдКұІЕҪУёГјмІвЈ¬ЗТҫӯHIVІ№ідКФСйјмІвСфРФөДІъёҫИЛКэЎЈ |
|
|
21. |
HIVјмІвСфРФІъёҫЧЬКэ |
|
ФЪұҫ»ъ№№ЧЎФә·ЦГдөДЛщУРҫӯHIVІ№ідКФСйјмІвСфРФөДІъёҫИЛКэЈ¬ОЮВЫЖдФЪФРЖЪ»№КЗІъКұјміцЎЈ |
|
|
22. |
ЧЎФә·ЦГд»оІъКэ |
|
°ьАЁЛщУРЧЎФә·ЦГд»оІъКэЎЈ |
|
|
23. |
HIVСфРФІъёҫЛщЙъ»оІъКэ |
|
ФЪұҫ»ъ№№ЧЎФә·ЦГдҫӯHIVІ№ідКФСйјмІвСфРФІъёҫ·ЦГд»оІъКэЎЈ |
|
ЧўЈәИз№ы1ёцФРІъёҫФЪФРІъЖЪ¶аҙОҪУКЬЧЙСҜЎўјмІвЈ¬ФтҪцЙПұЁ1ҙОЎЈ
МоұЁКұјдЈә МоұЁИЛЈә
МоұЁөҘО»ёәФрИЛЈә МоұЁөҘО»ЈЁёЗХВЈ©Јә
ұн1ЁCўу ФӨ·А°¬ЧМІЎДёУӨҙ«ІҘ№ӨЧчФВұЁұн
ЈЁУЙПШ/КРёҫУЧұЈҪЎ»ъ№№МоРҙЈ©
КРЈЁПШЈ© Дк ФВ
|
ұаәЕ |
По Дҝ |
ИЛКэ |
ЦёұкЛөГч |
|
|
24. |
·ЗЧЎФә·ЦГд |
·ЗЧЎФә·ЦГдІъёҫКэ |
|
УЙИэј¶ұЈҪЎНшВзіЈ№жЙПұЁКэҫЭ»сөГЎЈ |
|
25. |
ФРЖЪҪУКЬ°¬ЧМІЎЧЙСҜІъёҫКэ |
|
ФЪФРЖЪҪУКЬ№э°¬ЧМІЎЧЙСҜөДІъёҫИЛКэЈ¬ТФЎ°ФРІъЖЪұЈҪЎКЦІбЎұјЗВјОӘТАҫЭЎЈ |
|
|
26. |
ФРЖЪҪУКЬHIVјмІвІъёҫКэ |
|
ФЪФРЖЪҪУКЬ№эHIVјмІвөДІъёҫИЛКэЈ¬ТФЎ°ФРІъЖЪұЈҪЎКЦІбЎұјЗВј»тЎ°°¬ЧМІЎјмІвҪб№ыұЁёжөҘЎұОӘТАҫЭЎЈ |
|
|
27. |
ЖдЦРФР12ЦЬЗ°ҪУКЬHIVјмІвІъёҫКэ |
|
ФЪФР12ЦЬЗ°ҪУКЬ№эHIVјмІвөДІъёҫИЛКэЈ¬ТФЎ°ФРІъЖЪұЈҪЎКЦІбЎұјЗВј»тЎ°°¬ЧМІЎјмІвҪб№ыұЁёжөҘЎұОӘТАҫЭЎЈ |
|
|
28. |
ФР12-28ЦЬҪУКЬHIVјмІвІъёҫКэ |
|
ФЪФР12-28ЦЬҪУКЬ№эHIVјмІвөДІъёҫИЛКэЈ¬ТФЎ°ФРІъЖЪұЈҪЎКЦІбЎұјЗВј»тЎ°°¬ЧМІЎјмІвҪб№ыұЁёжөҘЎұОӘТАҫЭЎЈ |
|
|
29. |
ҪцІъКұҪУКЬHIVјмІвІъёҫКэ |
|
ФЪФРЖЪОҙҪУКЬHIVјмІвЈ¬Ҫц·ЦГдКұІЕҪУКЬёГјмІвөДІъёҫИЛКэЈ¬ТАҫЭЎ°ФРІъЖЪұЈҪЎКЦІбЎұјЗВј»тЎ°°¬ЧМІЎјмІвҪб№ыұЁёжөҘЎұМоРҙЎЈ |
|
|
30. |
ҪцІъКұHIVјмІвСфРФІъёҫКэ |
|
ФЪФРЖЪОҙҪУКЬHIVјмІвЈ¬Ҫц·ЦГдКұІЕҪУКЬёГјмІвЈ¬ЗТҫӯHIVІ№ідКФСйјмІвСфРФөДІъёҫИЛКэЎЈ |
|
|
31. |
HIVјмІвСфРФІъёҫКэ |
|
Цё·ЗЧЎФә·ЦГдөДЛщУРҫӯHIVІ№ідКФСйјмІвСфРФөДІъёҫИЛКэЎЈ |
|
|
32. |
·ЗЧЎФә·ЦГд»оІъКэ |
|
Цё·ЗЧЎФә·ЦГдөДЛщУР»оІъКэЎЈ |
|
|
33. |
HIVСфРФІъёҫЛщЙъ»оІъКэ |
|
Цё·ЗЧЎФә·ЦГдөДҫӯHIVІ№ідКФСйјмІвСфРФІъёҫ·ЦГд»оІъКэЎЈ |
|
|
34. |
ПҪЗшІъёҫЧЬКэ |
|
УЙИэј¶ұЈҪЎНшВзіЈ№жЙПұЁКэҫЭ»сөГЈ¬ОӘПҪЗшДЪЧЎФә·ЦГдУл·ЗЧЎФә·ЦГдөДІъёҫИЛКэЧЬәНЎЈ |
|
|
35. |
ПҪЗш»оІъЧЬКэ |
|
УЙИэј¶ұЈҪЎНшВзіЈ№жЙПұЁКэҫЭ»сөГЈ¬ОӘПҪЗшДЪЧЎФә·ЦГдУл·ЗЧЎФә·ЦГдөД»оІъКэЧЬәНЎЈ |
|
МоұЁКұјдЈә МоұЁИЛЈә
МоұЁөҘО»ёәФрИЛЈә МоұЁөҘО»ЈЁёЗХВЈ©Јә
ұн2 ФӨ·АГ·¶ҫЎўТТёОДёУӨҙ«ІҘ№ӨЧчФВұЁЈЁ»гЧЬЈ©ұн
ЈЁУЙёҫУЧұЈҪЎ»ъ№№»гЧЬЈ©
КЎЈЁЧФЦОЗшЎўЦұПҪКРЈ© КРЈЁПШЈ©
Дк ФВ
|
ұаәЕ |
По Дҝ |
ИЛКэ |
ЦёұкЛөГч |
||
|
1. |
ФРЖЪ |
ҪУКЬіхҙОІъЗ°ұЈҪЎөДФРёҫКэ |
|
УЙұн2ЁCўс»гЧЬ»сөГЎЈ |
|
|
2. |
ҪУКЬГ·¶ҫјмІвФРёҫКэ |
|
|||
|
3. |
ЖдЦРЈәГ·¶ҫёРИҫФРёҫКэ |
|
|||
|
4. |
ҪУКЬТТёОұнГжҝ№ФӯјмІвФРёҫКэ |
|
|||
|
5. |
ЖдЦРЈәТТёОұнГжҝ№ФӯСфРФФРёҫКэ |
|
|||
|
6. |
ЧЎФә·ЦГд |
Г·¶ҫ |
ФРЖЪҪУКЬГ·¶ҫјмІвІъёҫКэ |
|
УЙұн2ЁCўс»гЧЬ»сөГЎЈ |
|
7. |
ЖдЦРФР12ЦЬЗ°ҪУКЬГ·¶ҫјмІвІъёҫКэ |
|
|||
|
8. |
ФР12-28ЦЬҪУКЬГ·¶ҫјмІвІъёҫКэ |
|
|||
|
9. |
ҪцІъКұҪУКЬГ·¶ҫјмІвІъёҫКэ |
|
|||
|
10. |
ҪцІъКұХп¶ПОӘГ·¶ҫёРИҫІъёҫКэ |
|
|||
|
11. |
Г·¶ҫёРИҫІъёҫЧЬКэ |
|
|||
|
12. |
Г·¶ҫёРИҫІъёҫЛщЙъ»оІъКэ |
|
|||
|
13. |
ТТёО |
ФРЖЪҪУКЬТТёОұнГжҝ№ФӯјмІвІъёҫКэ |
|
||
|
14. |
ЖдЦРФР12ЦЬЗ°ҪУКЬТТёОұнГжҝ№ФӯјмІвІъёҫКэ |
|
|||
|
15. |
ФР12-28ЦЬҪУКЬТТёОұнГжҝ№ФӯјмІвІъёҫКэ |
|
|||
|
16. |
ҪцІъКұҪУКЬТТёОұнГжҝ№ФӯјмІвІъёҫКэ |
|
|||
|
17. |
ҪцІъКұТТёОұнГжҝ№ФӯСфРФІъёҫКэ |
|
|||
|
18. |
ТТёОұнГжҝ№ФӯСфРФІъёҫЧЬКэ |
|
|||
|
19. |
ТТёОұнГжҝ№ФӯСфРФІъёҫЛщЙъ»оІъКэ |
|
|||
|
20. |
ЖдЦРЈәЧўЙдТТёОГвТЯЗтө°°ЧөД¶щНҜКэ |
|
|||
|
21. |
·ЗЧЎФә·ЦГд |
Г·¶ҫ |
ҪУКЬГ·¶ҫјмІвІъёҫКэ |
|
УЙұн2ЁCўт»гЧЬ»сөГЎЈ |
|
22. |
Г·¶ҫёРИҫІъёҫКэ |
|
|||
|
23. |
|
|
Г·¶ҫёРИҫІъёҫЛщЙъ»оІъКэ |
|
|
|
24. |
ТТёО |
ҪУКЬТТёОұнГжҝ№ФӯјмІвІъёҫКэ |
|
||
|
25. |
ТТёОұнГжҝ№ФӯСфРФІъёҫЧЬКэ |
|
|||
|
26. |
ТТёОұнГжҝ№ФӯСфРФІъёҫЛщЙъ»оІъКэ |
|
|||
|
27. |
ЖдЦРЈәЧўЙдТТёОГвТЯЗтө°°ЧөД¶щНҜКэ |
|
|||
МоұЁКұјдЈә МоұЁИЛЈә
МоұЁөҘО»ёәФрИЛЈә МоұЁөҘО»ЈЁёЗХВЈ©Јә
ұн2ЁCўс ФӨ·АГ·¶ҫЎўТТёОДёУӨҙ«ІҘ№ӨЧчФВұЁұн
ЈЁУЙЦъІъ»ъ№№МоРҙЈ©
КРЈЁПШЈ© ТҪФәЈЁёҫУЧұЈҪЎФәЈ© Дк ФВ
|
ұаәЕ |
По Дҝ |
ИЛКэ |
ЦёұкЛөГч |
||
|
1. |
ФРЖЪ |
ҪУКЬіхҙОІъЗ°ұЈҪЎөДФРёҫКэ |
|
ЦёіхҙОҪУКЬФРЖЪұЈҪЎ·юОсөДФРёҫИЛКэЎЈ |
|
|
2. |
ҪУКЬГ·¶ҫјмІвФРёҫКэ |
|
ФРЖЪіхҙОҪУКЬГ·¶ҫјмІвөДФРёҫИЛКэЈ¬ТФГ·¶ҫјмІвҪб№ыұЁёжөҘОӘТАҫЭЎЈ |
||
|
3. |
ЖдЦРЈәГ·¶ҫёРИҫФРёҫКэ |
|
°ьАЁЛщУРФЪФРЖЪХп¶ПОӘГ·¶ҫёРИҫөДФРёҫЈ¬ОЮВЫЖдИСЙпҪбҫЦИзәОЎЈ |
||
|
4. |
ҪУКЬТТёОұнГжҝ№ФӯјмІвФРёҫКэ |
|
ФРЖЪіхҙОҪУКЬТТёОІЎ¶ҫСӘЗеұкЦҫОпјмІвЈЁТТёОұнГжҝ№Фӯ»тБҪ¶Ф°лЈ©өДФРёҫКэЈ¬ТФјмІвҪб№ыұЁёжөҘОӘТАҫЭЎЈ |
||
|
5. |
ЖдЦРЈәТТёОұнГжҝ№ФӯСфРФФРёҫКэ |
|
°ьАЁЛщУРФЪФРЖЪјміцөДТТёОұнГжҝ№ФӯСфРФФРёҫЈ¬ОЮВЫЖдИСЙпҪбҫЦИзәОЎЈ |
||
|
6. |
ЧЎФә·ЦГд |
Г·¶ҫ |
ФРЖЪҪУКЬГ·¶ҫјмІвІъёҫКэ |
|
ІъёҫЦРФЪФРЖЪҪУКЬГ·¶ҫјмІвөДИЛКэТФЎ°ФРІъЖЪұЈҪЎКЦІбЎұјЗВј»тЎ°Г·¶ҫјмІвҪб№ыұЁёжөҘЎұОӘТАҫЭЎЈ |
|
7. |
ЖдЦРФР12ЦЬЗ°ҪУКЬГ·¶ҫјмІвІъёҫКэ |
|
ІъёҫЦРФЪФР12ЦЬЗ°ҪУКЬГ·¶ҫјмІвөДИЛКэТФЎ°ФРІъЖЪұЈҪЎКЦІбЎұјЗВј»тЎ°Г·¶ҫјмІвҪб№ыұЁёжөҘЎұОӘТАҫЭЎЈ |
||
|
8. |
ФР12-28ЦЬҪУКЬГ·¶ҫјмІвІъёҫКэ |
|
ІъёҫЦРФЪФР12-28ЦЬЗ°ҪУКЬГ·¶ҫјмІвөДИЛКэТФЎ°ФРІъЖЪұЈҪЎКЦІбЎұјЗВј»тЎ°Г·¶ҫјмІвҪб№ыұЁёжөҘЎұОӘТАҫЭЎЈ |
||
|
9. |
ҪцІъКұҪУКЬГ·¶ҫјмІвІъёҫКэ |
|
ІъёҫЦРФЪФРЖЪОҙҪУКЬГ·¶ҫјмІвЈ¬ҪцФЪЧЎФә·ЦГдКұІЕҪУКЬёГјмІвөДІъёҫИЛКэЈ¬ТАҫЭ·ЦГдөЗјЗј°Г·¶ҫјмІвҪб№ыұЁёжөҘМоРҙЎЈ |
||
|
10. |
ҪцІъКұХп¶ПОӘГ·¶ҫёРИҫІъёҫКэ |
|
ІъёҫЦРФЪФРЖЪОҙҪУКЬГ·¶ҫјмІвЈ¬Ҫц·ЦГдКұІЕҪУКЬёГјмІвЎўЗТХп¶ПОӘГ·¶ҫёРИҫөДІъёҫИЛКэЎЈ |
||
|
11. |
Г·¶ҫёРИҫІъёҫЧЬКэ |
|
ЛщУРХп¶ПОӘГ·¶ҫёРИҫөДІъёҫИЛКэЈ¬ОЮВЫЖдФЪФРЖЪ»№КЗІъКұХп¶ПОӘГ·¶ҫёРИҫЎЈ |
||
|
12. |
Г·¶ҫёРИҫІъёҫЛщЙъ»оІъКэ |
|
Г·¶ҫёРИҫІъёҫ·ЦГд»оІъКэЎЈ |
||
|
13. |
ТТёО |
ФРЖЪҪУКЬТТёОұнГжҝ№ФӯјмІвІъёҫКэ |
|
ІъёҫЦРФЪФРЖЪҪУКЬТТёОІЎ¶ҫІЎСӘЗеұкЦҫОпјмІвЈЁТТёОұнГжҝ№Фӯ»тБҪ¶Ф°лЈ©өДИЛКэЈ¬ТФЎ°ФРІъЖЪұЈҪЎКЦІбЎұјЗВј»тЎ°ТТёОјмІвҪб№ыұЁёжөҘЎұОӘТАҫЭЎЈ |
|
|
14. |
ЖдЦРФР12ЦЬЗ°ҪУКЬТТёОұнГжҝ№ФӯјмІвІъёҫКэ |
|
ІъёҫЦРФЪФР12ЦЬЗ°ҪУКЬТТёОІЎ¶ҫІЎСӘЗеұкЦҫОпјмІвЈЁТТёОұнГжҝ№Фӯ»тБҪ¶Ф°лЈ©өДИЛКэЈ¬ТФЎ°ФРІъЖЪұЈҪЎКЦІбЎұјЗВј»тЎ°ТТёОјмІвҪб№ыұЁёжөҘЎұОӘТАҫЭЎЈ |
||
|
15. |
ФР12-28ЦЬҪУКЬТТёОұнГжҝ№ФӯјмІвІъёҫКэ |
|
ІъёҫЦРФЪФР12-28ЦЬЗ°ҪУКЬТТёОІЎ¶ҫІЎСӘЗеұкЦҫОпјмІвЈЁТТёОұнГжҝ№Фӯ»тБҪ¶Ф°лЈ©өДИЛКэЈ¬ТФЎ°ФРІъЖЪұЈҪЎКЦІбЎұјЗВј»тЎ°ТТёОјмІвҪб№ыұЁёжөҘЎұОӘТАҫЭЎЈ |
||
|
16. |
ҪцІъКұҪУКЬТТёОұнГжҝ№ФӯјмІвІъёҫКэ |
|
ІъёҫЦРФЪФРЖЪОҙҪУКЬТТёОІЎ¶ҫСӘЗеұкЦҫОпјмІвЈЁТТёОұнГжҝ№Фӯ»тБҪ¶Ф°лЈ©Ј¬ҪцФЪЧЎФә·ЦГдКұІЕҪУКЬёГјмІвөДІъёҫИЛКэЈ¬ТАҫЭ·ЦГдөЗјЗј°Па№ШјмІвҪб№ыұЁёжөҘМоРҙЎЈ |
||
|
17. |
ҪцІъКұТТёОұнГжҝ№ФӯСфРФІъёҫКэ |
|
ІъёҫЦРФЪФРЖЪОҙҪУКЬТТёОІЎ¶ҫСӘЗеұкЦҫОпјмІвЈЁТТёОұнГжҝ№Фӯ»тБҪ¶Ф°лЈ©Ј¬ҪцЧЎФә·ЦГдКұІЕҪУКЬёГјмІвЎўЗТТТёОұнГжҝ№ФӯСфРФөДІъёҫИЛКэЎЈ |
||
|
18. |
ТТёОұнГжҝ№ФӯСфРФІъёҫЧЬКэ |
|
ЛщУРТТёОұнГжҝ№ФӯСфРФІъёҫИЛКэЈ¬ОЮВЫЖдФЪФРЖЪ»№КЗІъКұјміцЎЈ |
||
|
19. |
ТТёОұнГжҝ№ФӯСфРФІъёҫЛщЙъ»оІъКэ |
|
ТТёОұнГжҝ№ФӯСфРФІъёҫ·ЦГд»оІъКэЎЈ |
||
|
20. |
ЖдЦРЈәЧўЙдТТёОГвТЯЗтө°°ЧөД¶щНҜКэ |
|
ТТёОұнГжҝ№ФӯСфРФІъёҫ·ЦГдөД»оІъ¶щЦРҪУКЬТТёОГвТЯЗтө°°ЧЧўЙдөДИЛКэЎЈ |
||
МоұЁКұјдЈә МоұЁИЛЈә
МоұЁөҘО»ёәФрИЛЈә МоұЁөҘО»ЈЁёЗХВЈ©Јә
ұн2ЁCўт ФӨ·АГ·¶ҫЎўТТёОДёУӨҙ«ІҘ№ӨЧчФВұЁұн
ЈЁУЙПШ/КРёҫУЧұЈҪЎ»ъ№№МоРҙЈ©
КРЈЁПШЈ© Дк ФВ
|
ұаәЕ |
По Дҝ |
ИЛКэ |
ЦёұкЛөГч |
||
|
21. |
·ЗЧЎФә·ЦГд |
Г·¶ҫ |
ҪУКЬГ·¶ҫјмІвІъёҫКэ |
|
ҪУКЬ№эГ·¶ҫјмІвөДІъёҫИЛКэЈ¬ТФЎ°ФРІъЖЪұЈҪЎКЦІбЎұјЗВј»тЎ°Г·¶ҫјмІвҪб№ыұЁёжөҘЎұОӘТАҫЭЎЈ |
|
22. |
Г·¶ҫёРИҫІъёҫКэ |
|
ЛщУРХп¶ПОӘГ·¶ҫёРИҫІъёҫИЛКэЎЈ |
||
|
23. |
Г·¶ҫёРИҫІъёҫЛщЙъ»оІъКэ |
|
ЛщУРГ·¶ҫёРИҫІъёҫ·ЦГд»оІъКэЎЈ |
||
|
24. |
ТТёО |
ҪУКЬТТёОұнГжҝ№ФӯјмІвІъёҫКэ |
|
ҪУКЬ№эТТёОІЎ¶ҫСӘЗеұкЦҫОпјмІвЈЁТТёОұнГжҝ№Фӯ»тБҪ¶Ф°лЈ©өДІъёҫИЛКэЈ¬ТФЎ°ФРІъЖЪұЈҪЎКЦІбЎұјЗВј»тЎ°јмІвҪб№ыұЁёжөҘЎұОӘТАҫЭЎЈ |
|
|
25. |
ТТёОұнГжҝ№ФӯСфРФІъёҫЧЬКэ |
|
ЛщУРТТёОұнГжҝ№ФӯСфРФІъёҫИЛКэЎЈ |
||
|
26. |
ТТёОұнГжҝ№ФӯСфРФІъёҫЛщЙъ»оІъКэ |
|
ЛщУРТТёОұнГжҝ№ФӯСфРФІъёҫ·ЦГд»оІъКэЎЈ |
||
|
27. |
ЖдЦРЈәЧўЙдТТёОГвТЯЗтө°°ЧөД¶щНҜКэ |
|
ТТёОұнГжҝ№ФӯСфРФІъёҫ·ЦГдөД»оІъ¶щЦРҪУКЬТТёОГвТЯЗтө°°ЧЧўЙдөДИЛКэЎЈ |
||
МоұЁКұјдЈә МоұЁИЛЈә
МоұЁөҘО»ёәФрИЛЈә МоұЁөҘО»ЈЁёЗХВЈ©Јә
ұаәЕЈәЎхЎхЎхЎхЎхЎхЎӘЎхЎхЎхЎӘЎхЎхЎхЎхЎӘЎхЎхЎх
ұн3ЁCўсЎў°¬ЧМІЎІЎ¶ҫёРИҫФРІъёҫ/»йјмёҫЕ®»щұҫЗйҝцөЗјЗҝЁЈЁұЈГЬЈ©КЎЈЁЧФЦОЗшЎўКРЈ© ПШЈЁКРЎўЗшЈ© ТҪФәЈЁёҫУЧұЈҪЎФәЈ©
|
Т»Ўў»щұҫЗйҝц РХГыЈә Йн·ЭЦӨәЕЈә . іцЙъИХЖЪЈә Дк ФВ ИХЈЁИзіцЙъИХЖЪІ»ПкЈ¬КөЧгДкБдЈә ЛкЈ© ГсЧеЈә әәЎў ЧіЎў ВъЎў »ШЎў ГзЎў О¬Об¶ыЎў ТНЎў НБјТЎў ГЙ№ЕЎў ІШЎў ЖдЛы ОД»ҜіМ¶ИЈә ОДГӨ/°лОДГӨЎў РЎС§Ўў іхЦРЎў ёЯЦРЈЁә¬ЦРЧЁЎўЦ°ТөёЯЦРЎўјј№ӨѧУөИЈ© ҙуЧЁ»тҙуС§Ўў Л¶Кҝј°ТФЙПЎў І»Пк Ц°ТөЈә С§ЙъЈЁСРҫҝЙъЎўҙуС§ЎўЦРС§Ј©Ўў ҪМКҰЎў ұЈУэФұј°ұЈД·Ўў ІНТыКіЖ·ТөЎў ЙМТө·юОсЎў ТҪОсИЛФұЎў №ӨИЛЎў Е©Гс№ӨЎў Е©ГсЎў ДБГсЎў УжЈЁҙ¬Ј©ГсЎў ёЙІҝЦ°ФұЎў АлНЛИЛФұЎў јТОсј°ҙэТөЎў ЖдЛы Ўў І»Пк »йТцЧҙҝцЈә Оҙ»йЎў іх»йЎў ФЩ»йЎў Н¬ҫУЎў Ал»йЎў ЙҘЕј ФРІъЗйҝцЈә ФРҙОЎў ІъҙОЎў ПЦУРЧУЕ®Кэ ПЦЧЎЦ·ЈЁПкМоЈ©Јә КЎ КР ПШЈЁЗшЈ© ПзЈЁХтЎўҪЦөАЈ© ҙе ЈЁГЕЕЖәЕЈ© »§ҝЪЛщФЪөШЈә КЎ КР ПШЈЁЗшЈ© ПзЈЁХтЎўҪЦөАЈ© ҙе ЈЁГЕЕЖәЕЈ© №ӨЧчөҘО»Јә БӘПөөз»°ЈЁ·ЗұШМоЈ©Јә ФРІъёҫ/»йјмёҫЕ®КфУЪЈә ұҫПШЗшЎў ұҫКРЖдЛыПШЗшЎў ұҫКЎЖдЛыөШКР НвКЎЎў ёЫ°ДМЁЎў Нвј® ЈЁ№ъјТЈ© |
|
¶юЎў°¬ЧМІЎІЎ¶ҫёРИҫПа№ШЗйҝц ГчИ·°¬ЧМІЎІЎ¶ҫёРИҫКұЖЪЈә »йЗ°јмІйЎў ИЛ№ӨБчІъЎў ТэІъЎў ФРЖЪұЈҪЎЎў ІъКұЎў ІъәуЎў ЖдЛы ГчИ·°¬ЧМІЎІЎ¶ҫёРИҫКұјдЈә Дк ФВ ИХ ұҫҙОИСЙпЗ°КЗ·сТСЦӘHIVёРИҫЈЁҪцёРИҫФРІъёҫМоРҙЈ©Јә ·сЎў КЗЈәұҫҙОКЗИ·ХпHIVёРИҫәуөЪ ҙОИСЙп ЧоҝЙДЬөД°¬ЧМІЎІЎ¶ҫёРИҫНҫҫ¶Јә ЧўЙд¶ҫЖ·Ўў РФҙ«ІҘЎў ІЙСӘЈЁҪ¬Ј©Ўў КдСӘ/СӘЦЖЖ·Ўў ДёУӨҙ«ІҘЎў Ц°Төұ©В¶Ўў І»ПкЎў ЖдЛы Па№ШОЈПХРРОӘЈЁҝЙ¶аСЎЈ©Јә УлHIVёРИҫЕдЕј»тДРУСөДРФЙъ»оЎў ¶аРФ°йЎў ЙМТөРФРРОӘЎў ЧўЙдОь¶ҫЎў УРіҘІЙ№©СӘЎў КдСӘ»тК№УГСӘЦЖЖ·Ўў ОЖЙн»тҙ©¶ъөИЙнМеҙМЙЛЎў ТвНвЙЛәҰЎў Ц°Төұ©В¶Ўў ТҪФҙРФёРИҫЎў І»ПкЎў ЖдЛы |
|
ИэЎўХЙ·т/РФ°йЗйҝц РХГыЈә іцЙъИХЖЪЈә Дк ФВ ИХЈЁИзіцЙъИХЖЪІ»ПкЈ¬КөЧгДкБдЈә ЛкЈ© ГсЧеЈә әәЎў ЧіЎў ВъЎў »ШЎў ГзЎў О¬Об¶ыЎў ТНЎў НБјТЎў ГЙ№ЕЎў ІШЎў ЖдЛы ОД»ҜіМ¶ИЈә ОДГӨ/°лОДГӨЎў РЎС§Ўў іхЦРЎў ёЯЦРЈЁә¬ЦРЧЁЎўЦ°ТөёЯЦРЎўјј№ӨѧУөИЈ© ҙуЧЁ»тҙуС§Ўў Л¶Кҝј°ТФЙПЎў І»Пк Ц°ТөЈә С§ЙъЈЁСРҫҝЙъЎўҙуС§ЎўЦРС§Ј©Ўў ҪМКҰЎў ұЈУэФұј°ұЈД·Ўў ІНТыКіЖ·ТөЎў ЙМТө·юОсЎў ТҪОсИЛФұЎў №ӨИЛЎў Е©Гс№ӨЎў Е©ГсЎў ДБГсЎў УжЈЁҙ¬Ј©ГсЎў ёЙІҝЦ°ФұЎў АлНЛИЛФұЎў јТОсј°ҙэТөЎў ЖдЛы Ўў І»Пк HIVјмІвЗйҝцЈә І»ПкЎў ОҙјмІвЎў јмІв HIVјмІвҪб№ыЈә І»ПкЎў ТхРФЎў СфРФЈ¬ГчИ·ёРИҫөДКұјдЈә Дк ФВ ИХЎў І»Пк ЧоҝЙДЬөД°¬ЧМІЎІЎ¶ҫёРИҫНҫҫ¶Јә ЧўЙд¶ҫЖ·Ўў ТмРФҙ«ІҘЎў Н¬РФҙ«ІҘЎў ІЙСӘЈЁҪ¬Ј©Ўў КдСӘ/СӘЦЖЖ·Ўў ДёУӨҙ«ІҘЎў Ц°Төұ©В¶Ўў І»ПкЎў ЖдЛы Па№ШОЈПХРРОӘЈЁҝЙ¶аСЎЈ©Јә ОЮОЈПХРРОӘЎў ¶аРФ°йЎў жОжҪЎў Н¬РФРФРРОӘЎў ЧўЙдОь¶ҫЎў УРіҘІЙ№©СӘЎў КдСӘ»тК№УГСӘЦЖЖ·Ўў ОЖЙн»тҙ©¶ъөИЙнМеҙМЙЛЎў ТвНвЙЛәҰЎў Ц°Төұ©В¶Ўў ТҪФҙРФёРИҫЎў І»ПкЎў ЖдЛы |
|
ЛДЎўұҫҙОҪУКЬФӨ·А°¬ЧМІЎДёУӨҙ«ІҘ·юОсЗйҝц ұҫҙОҪУКЬФӨ·А°¬ЧМІЎДёУӨҙ«ІҘ·юОсөДКұЖЪЈә »йЗ°јмІйЎў ИЛ№ӨБчІъЎў ТэІъЎў ФРЗ°Ўў ФРЖЪЎў ІъКұЎў Іъәу °¬ЧМІЎјмІвЗ°ЧЙСҜЗйҝцЈә ОҙЧЙСҜЎў ЧЙСҜЈ» °¬ЧМІЎјмІвәуЧЙСҜЗйҝцЈә ОҙЧЙСҜЎў ЧЙСҜ |
|
ұЁёжөҘО»ЈЁёЗХВЈ©Јә ұЁёжТҪЙъЈә БӘПөөз»°Јә МоұЁИХЖЪЈә Дк ФВ ИХ |
|
ұёЧўЈЁ·ЗұШМоЈ©Јә |
ұаәЕЈәЎхЎхЎхЎхЎхЎхЎӘЎхЎхЎхЎӘЎхЎхЎхЎхЎӘЎхЎхЎх
ұн3ЁCўтЎў°¬ЧМІЎІЎ¶ҫёРИҫФРІъёҫИСЙпј°ЛщЙъУӨ¶щөЗјЗҝЁЈЁұЈГЬЈ©КЎЈЁЧФЦОЗшЎўКРЈ© ПШЈЁКРЎўЗшЈ© ТҪФәЈЁёҫУЧұЈҪЎФәЈ©
|
РХГыЈә Йн·ЭЦӨәЕЈә . Т»ЎўұҫҙОИСЙпЎўФРІъЖЪұЈҪЎј°·ЦГдЗйҝц ұҫҙОИСЙпД©ҙОФВҫӯКұјдЈә Дк ФВ ИХЈ¬ФӨІъЖЪЈә Дк ФВ ИХЈ¬іхјмФРЦЬЈә ЦЬ ИСЙпҪбҫЦЈә ·ЦГдЎў ЧФИ»БчІъЎў ИЛ№ӨЦХЦ№ИСЙпЈ¬ЦХЦ№ИСЙпФРЦЬЈә ЦЬЎў ЖдЛы КЗ·сК§·ГЈә ОҙК§·ГЎў ТСК§·ГЈ¬К§·ГКұЖЪЈә ФРЦЬ»тІъәу ЦЬ ФРІъЖЪТміЈЗйҝцЈЁ¶аСЎЈ©Јә Оҙ·ўЙъЎў ФзІъЎў ЦРЦШ¶ИЖ¶СӘЎў ИСЙпёЯСӘС№јІІЎЎў МҘДӨФзЖЖЎў ЦНІъЎў ІъәуіцСӘЎў ИСЙпәПІўМЗДтІЎЎў ИСЙпәПІўРДФаІЎЎў ИСЙпәПІўёОІЎЎў ИСЙпГ·¶ҫЎў ЖдЛы ·ЦГд·ҪКҪЈә ЧФИ»·ЦГдЎў ТхөАЦъІъЎў ФсЖЪЖК№¬ІъЎў јұХпЖК№¬ІъЎў І»Пк ·ЦГдКұјдЈә Дк ФВ ИХ Кұ ·ЦЈ¬ ФРЦЬ+ МмЈ¬ЧЬІъіМ РЎКұ ·Ц ·ЦГдөШөгЈә КРј¶ТФЙПЦъІъ»ъ№№Ўў ПШЈЁЗшЈ©ј¶ЦъІъ»ъ№№Ўў ПзЈЁҪЦөАЈ©ј¶ЦъІъ»ъ№№Ўў јТЦРЎў ЖдЛы ІъҝЖІЩЧчЈЁҝЙ¶аСЎЈ©Јә ОЮЎў ІаЗРЎў ИЛ№ӨЖЖДӨЎў МҘОьЎў ІъЗҜЎў №¬ДЪН·ЖӨјаІвЎў І»ПкЎў ЖдЛы »бТхБСЙЛЈә ОЮЎў ўс¶ИБСЙЛЎў ўт¶ИБСЙЛЎў ўу¶ИБСЙЛј°ТФЙП ·ЦГдМҘКэЈә өҘМҘЎў Л«МҘЎў ИэМҘЎў ЖдЛы ЈЁ¶аМҘЗлБнёҪұҫұн·ЦұрМоРҙО§Іъ¶щЎўРВЙъ¶щУР№ШДЪИЭЈ© ФРІъёҫҪбҫЦЈә ҙж»оЎў ЛАНцЈ¬ЛАНцФӯТт Ўў І»Пк О§Іъ¶щЧӘ№йЈә »оІъЎў ЛАМҘЎў ЛАІъЎў ЖЯМмДЪЛАНцЎў І»Пк О§Іъ¶щТміЈЗйҝцЈЁҝЙ¶аСЎЈ©Јә ОЮЎў ФзІъ»төНіцЙъМеЦШЎў РВЙъ¶щ·ОСЧЎў РВЙъ¶щЦППўЎў іцЙъИұПЭ Ўў ЖдЛы Лж·ГЗйҝцЈәФРЖЪЛж·Г ҙО |
|||||
|
¶юЎўФРІъёҫҝ№°¬ЧМІЎІЎ¶ҫТ©ОпУҰУГЗйҝцЈә УГТ©Ўў ОҙУГТ©ЈЁМшЦБЎ°ИэЎўФРІъёҫёҙ·ҪРВЕөГчУГТ©ЗйҝцЎұЈ© ҝӘКјУГТ©КұјдЈә ФРЖЪЈ¬ ФРЦЬЎў ІъКұЎў Іъәу ФРЖЪЈә ОҙУГТ©Ўў УГТ©Ј¬Т©ОпГыіЖЈә + + Ј¬В©·юЗйҝцЈә ОҙВ©·юЎў В©·ю ҙО ІъКұЈә ОҙУГТ©Ўў УГТ©Ј¬Т©ОпГыіЖЈә + + Ј¬В©·юЗйҝцЈә ОҙВ©·юЎў В©·ю ҙО ІъәуЈә ОҙУГТ©Ўў УГТ©Ј¬Т©ОпГыіЖЈә + + Ј¬В©·юЗйҝцЈә ОҙВ©·юЎў В©·ю ҙО НЈЦ№УГТ©ЗйҝцЈә ОҙНЈТ©Ўў ТСНЈТ©Ј¬НЈТ©КұјдЈә ФРЖЪЈ¬ ФРЦЬЎў ІъКұЎў Іъәу Мм |
|||||
|
ИэЎўФРІъёҫёҙ·ҪРВЕөГчУГТ©ЗйҝцЈә УГТ©Ўў ОҙУГТ©ЈЁМшЦБЎ°ЛДЎўФРІъёҫПа№ШјмІвЗйҝцЎұЈ© ҝӘКјУГТ©КұјдЈә ФРЖЪЈ¬ ФРЦЬЎў ІъКұЎў Іъәу НЈЦ№УГТ©ЗйҝцЈә ОҙНЈТ©Ўў ТСНЈТ©Ј¬НЈТ©КұјдЈә ФРЖЪЈ¬ ФРЦЬЎў ІъКұЎў Іъәу Мм |
|||||
|
ЛДЎўФРІъёҫПа№ШјмІвЗйҝцЈә ҪшРР№эјмІвЈЁјмІвМоРҙҪб№ыЈ¬ОҙјмІвУГЎ°/ЎұұнКҫЈ©Ўў ОҙҪшРРИОәОјмІвЈЁМшЦБЎ°ЛДЎўРВЙъУӨ¶щЗйҝцЎұЈ© |
|||||
|
Па№ШјмІв јмІвФРЦЬ/Кұјд |
јмІвҪб№ы ФРЦЬ |
јмІвҪб№ы ФРЦЬ |
јмІвҪб№ы ФРНнЖЪ ФРЦЬ/ ІъКұ |
јмІвҪб№ы Іъәу ЦЬ |
|
|
°ЧПё°ыјЖКэЈЁ´ 109/LЈ© ЧЬБЬ°НПё°ыјЖКэЈЁ´ 109/LЈ© СӘРЎ°ејЖКэЈЁ´ 109/LЈ© СӘәмө°°ЧЈЁg/LЈ© СӘМЗЈЁmmol/LЈ© №ИұыЧӘ°ұГёЈЁALTЈ©ЈЁu/LЈ© №ИІЭЧӘ°ұГёЈЁASTЈ©ЈЁu/LЈ© ЧЬөЁәмЛШЈЁT.BILЈ©ЈЁҰМmol/LЈ© СӘјЎфыЈЁҰМmol/LЈ© СӘДтЛШөӘЈЁmmol/LЈ© CD4Пё°ыјЖКэЈЁёц/mm3Ј© CD8Пё°ыјЖКэЈЁёц/mm3Ј© ІЎ¶ҫФШБҝЈЁҝҪұҙ/ mlЈ© |
. ; . ; ; ; . ; . ; . ; . ; . ; . ; ; ; ; |
. ; . ; ; ; . ; . ; . ; . ; . ; . ; ; ; ; |
. ; . ; ; ; . ; . ; . ; . ; . ; . ; ; ; ; |
. ; . ; ; ; . ; . ; . ; . ; . ; . ; ; ; ; |
|
|
Г·¶ҫ |
ОҙјмІвЎў јмІвЈ¬јмІвКұјдЈә ФРЦЬ І»Пк јмІв·Ҫ·ЁЈә Г·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйЈЁTPPAЎўELISAөИЈ©Ўў ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйЈЁRPRЎўTRUSTөИЈ©Ўў ЖдЛы Г·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвҪб№ыЈә ТхРФЎў СфРФЎў І»И·¶ЁЎў І»Пк ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвҪб№ыЈә ТхРФЎў СфРФЎў І»И·¶ЁЎў І»Пк өО¶ИЈә ОҙјмІвЎў 1:8ТФПВЎў 1:8~1:64Ўў 1:64~1:128Ўў 1:128~1:256Ўў 1:256ТФЙП ЖдЛыјмІвҪб№ыЈәЎЎ ТхРФЎў СфРФЎў І»И·¶ЁЎў І»Пк |
||||
|
ТТёО |
ұнГжҝ№ФӯЈЁHBsAgЈ© |
ОҙјмІвЎў јмІвЈ¬јмІвКұјдЈә ФРЦЬ јмІвҪб№ыЈә ТхРФЎў СфРФЎў І»И·¶ЁЎў І»Пк |
|||
|
eҝ№ФӯЈЁHBeAgЈ© |
ОҙјмІвЎў јмІвЈ¬јмІвКұјдЈә ФРЦЬ јмІвҪб№ыЈә ТхРФЎў СфРФЎў І»И·¶ЁЎў І»Пк |
||||
|
ұыёО |
HCV-IgG |
ОҙјмІвЎў јмІвЈ¬јмІвКұјдЈә ФРЦЬ јмІвҪб№ыЈә ТхРФЎў СфРФЎў І»И·¶ЁЎў І»Пк |
|||
|
HCV-IgM |
ОҙјмІвЎў јмІвЈ¬јмІвКұјдЈә ФРЦЬ јмІвҪб№ыЈә ТхРФЎў СфРФЎў І»И·¶ЁЎў І»Пк |
||||
|
ОеЎўРВЙъУӨ¶щЗйҝцЈЁИзУР¶аёц»оІъУӨ¶щЈ¬Зл·ЦұрМоРҙУӨ¶щ»щұҫЗйҝцј°УГТ©ЗйҝцЈ© РХГыЈә РФұрЈә ДРЎў Е® іцЙъИХЖЪЈә Дк ФВ ИХ іцЙъМеЦШЈә ҝЛ іцЙъЙніӨЈә . АеГЧ Лж·ГЗйҝцЈә Лж·ГЦРЎў ОҙЛж·Г ҙж»оЗйҝцЈә ҙж»оЎў ЛАНцЈ¬ЛАНцФӯТт Ј¬ЛАНцКұјдЈә Дк ФВ ИХ ФӨ·АҪУЦЦЗйҝцЈә ОҙҪУЦЦЎў ТТёОТЯГзөЪТ»ХлЎў ҝЁҪйГзЎў І»Пк |
|||||
|
БщЎўРВЙъУӨ¶щҝ№°¬ЧМІЎІЎ¶ҫТ©ОпУҰУГЗйҝцЈә УГТ©Ўў ОҙУГТ©ЈЁМшЦБЎ°ұЁёжөҘО»ЈЁёЗХВЈ©ҙҰЎұЈ© ҝӘКјУГТ©КұјдЈә Дк ФВ ИХЈ¬НЈЦ№УГТ©КұјдЈә Дк ФВ ИХ Т©ОпГыіЖЈә + Ј¬В©·юЗйҝцЈә ОҙВ©·юЎў В©·ю ҙО |
|||||
|
ұЁёжөҘО»ЈЁёЗХВЈ©Јә ұЁёжТҪЙъЈә БӘПөөз»°Јә МоұЁИХЖЪЈә Дк ФВ ИХ |
|||||
|
ұёЧўЈЁ·ЗұШМоЈ©Јә |
|||||
ФРІъёҫұаәЕЈәЎхЎхЎхЎхЎхЎхЎӘЎхЎхЎхЎӘЎхЎхЎхЎхЎӘЎхЎхЎх
¶щНҜұаәЕЈәЎхЎхЎхЎхЎхЎхЎӘЎхЎхЎхЎӘЎхЎхЎхЎхЎӘЎхЎхЎхЎӘЎх
ұн3ЁCўуЎў°¬ЧМІЎІЎ¶ҫёРИҫІъёҫј°ЛщЙъ¶щНҜЛж·ГөЗјЗҝЁЈЁұЈГЬЈ©КЎЈЁЧФЦОЗшЎўКРЈ© ПШЈЁКРЎўЗшЈ© ТҪФәЈЁёҫУЧұЈҪЎФәЈ©
ФРІъёҫРХГыЈә Йн·ЭЦӨәЕЈә .
¶щНҜРХГыЈә РФұрЈә ДРЎў Е® іцЙъИХЖЪЈә Дк ФВ ИХ
ГсЧеЈә әәЎў ЧіЎў ВъЎў »ШЎў ГзЎў О¬Об¶ыЎў ТНЎў НБјТЎў ГЙ№ЕЎў ІШЎў ЖдЛы
ПЦЧЎЦ·ЈЁПкМоЈ©Јә ПзЈЁХтЎўҪЦөАЈ© ҙе ЈЁГЕЕЖәЕЈ©Ј» БӘПөөз»°ЈЁ·ЗұШМоЈ©Јә
Лж·ГИХЖЪЈә Дк ФВ ИХ ¶щНҜФВБдЈә ФВ Лж·ГИЛРХГыЈә
Т»ЎўёРИҫёҫЕ®Зйҝц
ЈЁТ»Ј©Лж·ГЗйҝцЈә Лж·ГЎў ОҙЛж·ГЎў ТСК§·ГЈ¬К§·ГФӯТт
ЈЁ¶юЈ©ҙж»оЗйҝцЈә ҙж»оЎў ЛАНцЈ¬ЛАНцФӯТт Ўў І»Пк
ЈЁИэЈ©ЧӘҪй·юОсЈә ОҙМṩЎў МṩЈ¬ЧӘҪйФӯТт Ј¬ЧӘҪй»ъ№№
ЈЁЛДЈ©ұЬФРЗйҝцЈә ОҙұЬФРЎў І»Пк
ұЬФРЈ¬ұЬФР·Ҫ·ЁЈЁҝЙ¶аСЎЈ©Јә °ІИ«МЧЎў №¬ДЪҪЪУэЖчЎў ҝЪ·юұЬФРТ©Ўў І»ПкЎў ЖдЛы
ҝӘКјУҰУГұЬФР·Ҫ·ЁКұјдЈә Дк ФВ
¶юЎў¶щНҜЗйҝц
ЈЁТ»Ј©Лж·ГЗйҝцЈә Лж·ГЎў ОҙЛж·ГЎў ТСК§·ГЈ¬К§·ГФӯТт ЈЁ¶щНҜФЪВъ21ФВБдЗ°І»ұЁёжК§·ГЈ©
ЈЁ¶юЈ©ҙж»оЗйҝцЈә ҙж»оЎў ЛАНцЈ¬ЛАНцФӯТт Ј¬ЛАНцКұјдЈә Дк ФВ ИХ
ЈЁИэЈ©ЧӘҪй·юОсЈә ОҙМṩЎў МṩЈ¬ЧӘҪйФӯТт1 Ј¬ЧӘҪй»ъ№№1
ЧӘҪйФӯТт2 Ј¬ЧӘҪй»ъ№№2
ЈЁЛДЈ©ЙъіӨ·ўУэЈәМеЦШЈә І»ПкЎў . З§ҝЛ ДкБдұрМеЦШЖАјЫЈә ПВ ЦР ЙП
ЙніӨЈә І»ПкЎў . АеГЧЈ¬ ДкБдұрЙніӨЖАјЫЈә ПВ ЦР ЙП
ЙніӨұрМеЦШЖАјЫЈә ПВ ЦР ЙП
ЈЁОеЈ©О№Сш·ҪКҪЈә ҙҝДёИйО№СшЎў ИЛ№ӨО№СшЎў »мәПО№СшЎў ЖдЛы
ЈЁБщЈ©ёЁКіМнјУЈә ОҙМнјУЎў ТСМнјУЈ¬ ФВБдҝӘКјМнјУ
ЈЁЖЯЈ©јІІЎЗйҝцЈЁ¶аСЎЈ©Јә Оҙ·ўПЦЎў ІЎАнРФ»ЖргЎў ЙПәфОьөАёРИҫЎў ІЎАнРФё№РәЎў ·ОСЧЎў Ж¶СӘЎў
ШюЩНІЎЎў ЦРЦШ¶ИУӘСшІ»БјЎў І»ПкЎў ЖдЛы
ЈЁ°ЛЈ©Па№ШЦўЧҙЈЁ¶аСЎЈ©Јә Оҙ·ўПЦЎў јдРӘ»тіЦРшРФ·ўИИЎў іЦРшРФҝИЛФЎў ЖӨХоЎў
И«ЙнРФБЬ°НҪбЦЧҙуЎў ҝЪЎўСКІҝДоЦйҫъёРИҫЎў ёОЖўЦЧҙуЎў І»ПкЎў
ЖдЛы
ЈЁҫЕЈ©ФӨ·АҪУЦЦЗйҝцЈә
ҝЁҪйГзЈә ОҙҪУЦЦЎў ҪУЦЦЎў І»Пк
ТТёОТЯГзЈә ОҙҪУЦЦЎў ҪУЦЦЈ¬ЈЁөЪ 1/ 2/ 3ХлЈ©Ўў І»Пк
ј№Ли»ТЦКСЧТЯГзЈә ОҙҪУЦЦЎў ҪУЦЦЈ¬ЈЁөЪ 1/ 2/ 3јБЈ©Ўў І»Пк
ВйХоТЯГзЈә ОҙҪУЦЦЎў ҪУЦЦЎў І»Пк
°Щ°ЧЖЖ»мәПЦЖјБЈә ОҙҪУЦЦЎў ҪУЦЦЈ¬ЈЁөЪ 1/ 2/ 3ХлЈ©Ўў І»Пк
ЖдЛыЈә ОҙҪУЦЦЎў ҪУЦЦЈ¬ Ўў І»Пк
ЈЁК®Ј©HIVјмІвЈә ОҙјмІвЈЁМшЦБЈЁК®ИэЈ©ФӨ·АУҰУГёҙ·ҪРВЕөГчЈ©
ТСјмІвЈ¬јмІвКұјдЈә Дк ФВ ИХ
ЈЁК®Т»Ј©HIVјмІвҪб№ыЈә ТхРФЎў СфРФЎў І»И·¶ЁЎў І»ПкЎў ЖдЛы
ЈЁК®¶юЈ©ұҫҙОЛж·ГЖЪјдHIVјмІв·Ҫ·ЁЈЁ¶аСЎЈ©Јә ФзЖЪәЛЛбјмІвЎў ҝ№МеЙёІйЎў І№ідКФСйЎў
І»ПкЎў ЖдЛы
ЈЁК®ИэЈ©ФӨ·АУҰУГёҙ·ҪРВЕөГчЈә
ОҙУҰУГЎў УҰУГЈ¬ҝӘКјКұјдЈә Дк ФВ ИХ
КЗ·сНЈТ©Јә ·сЎў КЗЈ¬НЈЦ№КұјдЈә Дк ФВ ИХЈ¬
НЈЦ№ФӯТт________________________
ЈЁК®ЛДЈ©ұёЧўЈЁ·ЗұШМоЈ©Јә
ұЁёжөҘО»ЈЁёЗХВЈ©Јә ұЁёжТҪЙъЈә
БӘПөөз»°Јә МоұЁИХЖЪЈә Дк ФВ ИХ
ұаәЕЈәЎхЎхЎхЎхЎхЎхЎӘЎхЎхЎхЎӘЎхЎхЎхЎхЎӘЎхЎхЎх
ұн4ЁCўсЎўГ·¶ҫёРИҫФРІъёҫөЗјЗҝЁКЎЈЁЧФЦОЗшЎўКРЈ© ПШЈЁКРЎўЗшЈ© ТҪФәЈЁёҫУЧұЈҪЎФәЈ©
|
Т»Ўў»щұҫЗйҝц РХ ГыЈә Йн·ЭЦӨәЕЈә . іцЙъИХЖЪЈә Дк ФВ ИХЈЁИзіцЙъИХЖЪІ»ПкЈ¬КөЧгДкБдЈә ЛкЈ© Гс ЧеЈә әә Чі Въ »Ш Гз О¬Об¶ы ТН НБјТ ГЙ№Е ІШ ЖдЛы ОД»ҜіМ¶ИЈә ОДГӨ/°лОДГӨ РЎС§ іхЦР ёЯЦРЈЁә¬ЦРЧЁЎўЦ°ТөёЯЦРЎўјј№ӨѧУөИЈ© ҙуЧЁ»тҙуС§ Л¶Кҝј°ТФЙП І»Пк Ц° ТөЈә С§ЙъЈЁСРҫҝЙъЎўҙуС§ЎўЦРС§Ј©Ўў ҪМКҰЎў ұЈУэФұј°ұЈД·Ўў ІНТыКіЖ·ТөЎў ЙМТө·юОсЎў ТҪОсИЛФұЎў №ӨИЛ Е©Гс№Ө Е©Гс ДБГс УжЈЁҙ¬Ј©Гс ёЙІҝЦ°Фұ АлНЛИЛФұ јТОсј°ҙэТө ЖдЛы І»Пк »йТцЧҙҝцЈә Оҙ»й іх»й ФЩ»й Н¬ҫУ Ал»й ЙҘЕј ФРІъЗйҝцЈә ФРҙО ІъҙО ПЦУРЧУЕ®Кэ јИНщІ»БјИСЙпҪбҫЦЈә ОЮЎў ЧФИ»БчІъ ҙОЎў ЛАМҘ ҙОЎў ЛАІъ ҙОЎў ФзІъ ҙОЎў іцЙъИұПЭ МҘЎў ЖдЛы ұҫҙОИСЙпД©ҙОФВҫӯКұјдЈә Дк ФВ ИХЈ»ФӨІъЖЪЈә Дк ФВ ИХЈ»іхјмФРЦЬЈә ЦЬ ПЦЧЎЦ·ЈЁПкПёЈ©Јә КЎ КР ПШЈЁЗшЈ© ПзЈЁХтЎўҪЦөАЈ© ҙе ЈЁГЕЕЖәЕЈ© »§ҝЪЛщФЪөШЈә КЎ КР ПШЈЁЗшЈ© ПзЈЁХтЎўҪЦөАЈ© ҙе ЈЁГЕЕЖәЕЈ© №ӨЧчөҘО»Јә БӘПөөз»°ЈЁ·ЗұШМоЈ©Јә |
||||||||||||||||||||||||||||||||||||||||||||||||
|
¶юЎўФРІъёҫГ·¶ҫёРИҫПа№ШЗйҝц јИНщКЗ·сХп¶ПОӘГ·¶ҫёРИҫЈә ·с КЗЈ¬Хп¶ПКұјдЈә Дк ФВ ИХЎў І»Пк ұҫҙОХп¶ПГ·¶ҫёРИҫКұЖЪЈә ФРЖЪЈЁ ФРЦЬЈ© ІъКұ Іъәу ЖдЛы_____________ ұҫҙОХп¶ПГ·¶ҫёРИҫКұјдЈә Дк ФВ ИХ ұҫҙОГ·¶ҫХп¶П·ЦЖЪОӘЈә ТюРФ Т»ЖЪ ¶юЖЪ ИэЖЪ І»Пк ЧоҝЙДЬөДГ·¶ҫёРИҫНҫҫ¶Јә РФҙ«ІҘ СӘТәҙ«ІҘ ДёУӨҙ«ІҘ І»Пк ЖдЛы_________________ ХЙ·т/РФ°йДҝЗ°өДГ·¶ҫёРИҫЧҙҝцЈә ОҙјмІвЎў ОҙёРИҫЎў ёРИҫЎў јмІвҪб№ыІ»ПкЎў КЗ·сјмІвІ»Пк ЈЁМоРҙЎ°ОҙјмІвЎұЎўЎ°ОҙёРИҫЎұЎўЎ°Ҫб№ыІ»ПкЎұ»тЎ°КЗ·сјмІвІ»ПкЎұЈ¬МшЦБЎ°ИэЎұЈ© ХЙ·т/РФ°йөДГ·¶ҫХп¶ПКұјдЈә Дк ФВ ИХЎў І»Пк |
||||||||||||||||||||||||||||||||||||||||||||||||
|
ИэЎўФРІъёҫұҫҙОИСЙпГ·¶ҫКөСйКТХп¶ПТАҫЭ
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
ұЁёжөҘО»ЈЁёЗХВЈ©Јә ұЁёжТҪЙъЈә БӘПөөз»°Јә МоұЁИХЖЪЈә Дк ФВ ИХ |
||||||||||||||||||||||||||||||||||||||||||||||||
|
ұёЧўЈЁ·ЗұШМоЈ©Јә |
||||||||||||||||||||||||||||||||||||||||||||||||
ФРІъёҫұаәЕЈәЎхЎхЎхЎхЎхЎхЎӘЎхЎхЎхЎӘЎхЎхЎхЎхЎӘЎхЎхЎх
¶щНҜұаәЕЈәЎхЎхЎхЎхЎхЎхЎӘЎхЎхЎхЎӘЎхЎхЎхЎхЎӘЎхЎхЎхЎӘЎх
ұн4ЁCIIЎўГ·¶ҫёРИҫФРІъёҫј°ЛщЙъРВЙъ¶щөЗјЗҝЁКЎЈЁЧФЦОЗшЎўКРЈ© ПШЈЁКРЎўЗшЈ© ТҪФәЈЁёҫУЧұЈҪЎФәЈ©
|
ФРІъёҫРХГыЈә Йн·ЭЦӨәЕЈә БӘПөөз»°Јә ПЦЧЎЦ·ЈЁПкПёЈ©Јә КЎ КР ПШЈЁЗшЈ© ПзЈЁХтЎўҪЦөАЈ© ҙе ЈЁГЕЕЖәЕЈ©Ј» Т»ЎўФРІъёҫұҫҙОИСЙпј°·ЦГдЗйҝц ИСЙпҪбҫЦЈә ·ЦГд ЧФИ»БчІъЈЁФРЦЬЈә ЦЬЈ© ИЛ№ӨЦХЦ№ИСЙпЈЁЦХЦ№ИСЙпФРЦЬЈә ЦЬЈ© ЖдЛы КЗ·сК§·ГЈә ОҙК§·Г ТСК§·ГЈЁК§·ГКұЖЪЈә ФРЦЬ»тІъәу ЦЬЈ© ФРІъЖЪТміЈЗйҝцЈЁҝЙ¶аСЎЈ©Јә Оҙ·ўЙъ МҘДӨФзЖЖ ІъәуіцСӘ ТТёОёРИҫ HIVёРИҫ ЖдЛы ұҫҙОИСЙпөДД©ҙОФВҫӯКұјдЈә Дк ФВ ИХ ·ЦГдИХЖЪЈә Дк ФВ ИХЈ¬·ЦГдФРЦЬ ЦЬ+ Мм ·ЦГд·ҪКҪЈә ЧФИ»·ЦГд ТхөАЦъІъ ФсЖЪЖК№¬Іъ јұХпЖК№¬Іъ І»Пк ·ЦГдМҘКэЈә өҘМҘ Л«МҘ ИэМҘ ЖдЛы ФРІъёҫҪбҫЦЈә ҙж»о ЛАНцЈ¬ЛАНцФӯТт І»Пк О§Іъ¶щЧӘ№йЈә »оІъ ЛАМҘ ЛАІъ ЖЯМмДЪЛАНц І»Пк О§Іъ¶щТміЈЗйҝцЈЁҝЙ¶аСЎЈ©Јә ОЮ ФзІъ»төНіцЙъМеЦШ РВЙъ¶щ·ОСЧ РВЙъ¶щЦППў іцЙъИұПЭ ЖдЛы |
|||||||||||||||||||||||||||||||||||||||||
|
¶юЎўФРІъёҫГ·¶ҫТ©ОпУҰУГЗйҝцЈә ОҙУГТ©Ўў УГТ©ЈЁСЎФсЎ°ОҙУГТ©ЎұМшЦБЎ°ИэЎұЈ© өЪТ»ёцБЖіМ ҝӘКјКұјдЈә Дк ФВ ИХЈ¬Т©ОпЈә ЖХВіҝЁТтЗаГ№ЛШG ЬРРЗЗаГ№ЛШG Н·жЯЗъЛЙ әмГ№ЛШ ЖдЛы ГҝИХУГБҝ . ЈЁНтU/ҙО»тg/ИХЈ©Ј¬ҪбКшБЖіМКұјдЈә Дк ФВ ИХЈ¬І»Пк өЪ¶юёцБЖіМ ·сЎў КЗ ҝӘКјКұјдЈә Дк ФВ ИХЈ¬Т©ОпЈә ЖХВіҝЁТтЗаГ№ЛШG ЬРРЗЗаГ№ЛШG Н·жЯЗъЛЙ әмГ№ЛШ ЖдЛы ГҝИХУГБҝ . ЈЁНтU/ҙО»тg/ИХЈ©Ј¬ҪбКшБЖіМКұјдЈә Дк ФВ ИХЈ¬І»Пк өЪИэёцБЖіМ ·сЎў КЗ ҝӘКјКұјдЈә Дк ФВ ИХЈ¬Т©ОпЈә ЖХВіҝЁТтЗаГ№ЛШG ЬРРЗЗаГ№ЛШG Н·жЯЗъЛЙ әмГ№ЛШ ЖдЛы ГҝИХУГБҝ . ЈЁНтU/ҙО»тg/ИХЈ©Ј¬ҪбКшБЖіМКұјдЈә Дк ФВ ИХЈ¬І»Пк |
|||||||||||||||||||||||||||||||||||||||||
|
ИэЎўФРІъёҫұҫҙО·ЦГдЗ°»тФРНнЖЪ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвЈә ОҙјмІвЎў јмІв
|
|||||||||||||||||||||||||||||||||||||||||
|
ЛДЎўГ·¶ҫёРИҫФРІъёҫЛщЙъРВЙъ¶щЗйҝц ¶щНҜРХГыЈә РФұрЈә ДР Е® іцЙъМеЦШЈә ҝЛ іцЙъЙніӨЈә . АеГЧ ЈЁТ»Ј©ҙж»оЗйҝцЈә ҙж»о ЛАНцЈ¬ЛАНцФӯТт Ј¬ЛАНцКұјдЈә Дк ФВ ИХ ЈЁ¶юЈ©ЛщЙъУӨ¶щіцЙъәуөДГ·¶ҫјмІв·Ҫ·ЁЈә ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвЈЁҝЙ¶аСЎЈ©Јә ОҙјмІвЎў јмІв
Г·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвЈЁҝЙ¶аСЎЈ©Јә ОҙјмІвЎў јмІв
ЈЁИэЈ©Па№ШЦўЧҙЈЁ¶аСЎЈ©Јә Оҙ·ўПЦ Л®ЕЭ-ҙуреЈ¬әм°ЯЈ¬ЗрХоЈ¬ұвЖҪКӘра ұЗСЧ»тәнСЧ И«ЙнРФБЬ°НҪбЦЧҙу №ЗЛиСЧЈ¬№ЗИн№ЗСЧј°№ЗДӨСЧ Ж¶СӘ ёОЖўЦЧҙу І»Пк ЖдЛы ЈЁЛДЈ©КЗ·сҪУКЬФӨ·АРФЦОБЖЈә ·сЎў КЗЈЁСЎЎ°·сЎұЈ¬МшЦБЎ°ЈЁОеЈ©¶щНҜГ·¶ҫёРИҫХп¶ПЗйҝцЎұЈ© ФӨ·АРФЦОБЖөДТ©ОпГыіЖЈә ЬРРЗЗаГ№ЛШG ЖдЛы Ј»јББҝУГБҝ . ЈЁНтU/kgЈ© ФӨ·АРФЦОБЖҝӘКјКұјдЈә Дк ФВ ИХ ҫа·ЦГдКұјдЈә Мм РЎКұ ·Ц ЈЁОеЈ©РВЙъ¶щГ·¶ҫёРИҫЗйҝцЈә Хп¶ППИМмГ·¶ҫЎў јМРшЛж·ГҙэХп¶ПЈЁСЎФсЎ°јМРшЛж·ГҙэХп¶ПЎұЈ¬МшЦБЎ°°ЛЎұЈ© ЈЁБщЈ©РВЙъ¶щХп¶ПОӘПИМмГ·¶ҫөДТАҫЭЈәЈЁҝЙ¶аСЎЈ© іцЙъКұ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйСфРФЈ¬ЗТөО¶ИҙуУЪөИУЪДёЗЧ·ЦГдЗ°өО¶ИөД4ұ¶Ј¬Г·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйСфРФЈ» ЖӨ·фрӨДӨЛрәҰ»тЧйЦҜұкұҫ°өКУТ°ПФОўҫөЈЁ»т¶ЖТшИҫЙ«Ј©јмІвөҪГ·¶ҫВЭРэМеЈ» Г·¶ҫВЭРэМеIgMҝ№МејмІвСфРФЎЈ ЈЁЖЯЈ©Хп¶ПОӘПИМмГ·¶ҫөДРВЙъ¶щКЗ·сҪУКЬЦОБЖЈә ·с КЗ ЈЁ°ЛЈ©ұёЧўЈЁ·ЗұШМоЈ©Јә |
|||||||||||||||||||||||||||||||||||||||||
|
ұЁёжөҘО»ЈЁёЗХВЈ©Јә ұЁёжТҪЙъЈә БӘПөөз»°Јә МоұЁИХЖЪЈә Дк ФВ ИХ |
|||||||||||||||||||||||||||||||||||||||||
|
ұёЧў |
|||||||||||||||||||||||||||||||||||||||||
ФРІъёҫұаәЕЈәЎхЎхЎхЎхЎхЎхЎӘЎхЎхЎхЎӘЎхЎхЎхЎхЎӘЎхЎхЎх
¶щНҜұаәЕЈәЎхЎхЎхЎхЎхЎхЎӘЎхЎхЎхЎӘЎхЎхЎхЎхЎӘЎхЎхЎхЎӘЎх
ұн4ЁCўуЎўГ·¶ҫёРИҫІъёҫЛщЙъ¶щНҜЛж·ГөЗјЗҝЁ КЎЈЁЧФЦОЗшЎўКРЈ© ПШЈЁКРЎўЗшЈ© ТҪФәЈЁёҫУЧұЈҪЎФәЈ©|
ФРІъёҫРХГыЈә Йн·ЭЦӨәЕЈә Јә ПЦЧЎЦ·ЈЁПкПёЈ©Јә КЎ КР ПШЈЁЗшЈ© ПзЈЁХтЎўҪЦөАЈ© ҙе ЈЁГЕЕЖәЕЈ©Ј» ¶щНҜРХГыЈә РФұрЈә ДРЎў Е® іцЙъИХЖЪЈә Дк ФВ ИХ БӘПөөз»°Јә ¶щНҜФВБдЈә ФВ Лж·ГИХЖЪЈә Дк ФВ ИХ Лж·ГИЛРХГыЈә ЈЁТ»Ј©Лж·ГЗйҝцЈә ОҙЛж·ГЎў Лж·ГЎў ТСК§·ГЈ¬К§·ГФӯТт ЈЁ¶щНҜФЪВъ21ФВБдЗ°І»ұЁёжК§·ГЈ© ЈЁ¶юЈ©ҙж»оЗйҝцЈә ҙж»оЎў ЛАНцЈ¬ЛАНцФӯТт Ј¬ЛАНцКұјдЈә Дк ФВ ИХ ЈЁИэЈ©ЙъіӨ·ўУэЈәМеЦШЈә І»ПкЎў . З§ҝЛЈ¬ ДкБдұрМеЦШЖАјЫЈә ПВЎў ЦРЎў ЙП ЙніӨЈә І»ПкЎў . АеГЧЈ¬ ДкБдұрЙніӨЖАјЫЈә ПВЎў ЦРЎў ЙП ЙніӨұрМеЦШЖАјЫЈә ПВЎў ЦРЎў ЙП ЈЁЛДЈ©О№Сш·ҪКҪЈә ДёИйО№СшЎў ИЛ№ӨО№СшЎў »мәПО№СшЎў ЖдЛы ЈЁОеЈ©Па№ШЦўЧҙ»тјІІЎЈЁҝЙ¶аСЎЈ©Јә Оҙ·ўПЦ Л®ЕЭ-ҙуреЈ¬әм°ЯЈ¬ЗрХоЈ¬ұвЖҪКӘра ұЗСЧ»тәнСЧ И«ЙнРФБЬ°НҪбЦЧҙуЎў №ЗЛиСЧЈ¬№ЗИн№ЗСЧј°№ЗДӨСЧ ІЎАнРФ»Жрг ЙПәфОьөАёРИҫ ё№Рә ·ОСЧ Ж¶СӘЎў ёОЖўЦЧҙу ШюЩНІЎ ЦРЦШ¶ИУӘСшІ»Бј І»Пк ЖдЛы ЈЁБщЈ©Г·¶ҫјмІв·Ҫ·ЁЈә ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвЈЁҝЙ¶аСЎЈ©Јә ОҙјмІвЎў јмІв
Г·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвЈЁҝЙ¶аСЎЈ©Јә ОҙјмІвЎў јмІв
ЈЁЖЯЈ©¶щНҜГ·¶ҫёРИҫЧҙМ¬Јә Хп¶ППИМмГ·¶ҫЈЁјМРшМоРҙЎ°°ЛЎўҫЕЎўК®ЎұЈ©Ўў ЕЕіэГ·¶ҫёРИҫЎў јМРшЛж·ГҙэХп¶ПЎў ЖдЛь ЈЁ°ЛЈ©ПИМмГ·¶ҫХп¶ПТАҫЭЈЁҝЙ¶аСЎЈ©ЈЁПөНіЦРөҜіцҝтМбКҫЈ© іцЙъКұІ»ДЬХп¶ППИМмГ·¶ҫөД¶щНҜЈ¬ИОәОТ»ҙОЛж·ГЦР·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйөО¶ИЙПЙэЈ¬ЗТГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйСфРФЈ» іцЙъКұІ»ДЬХп¶ППИМмГ·¶ҫөД¶щНҜЈ¬ИОәОТ»ҙОЛж·ГЦР·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйУЙТхЧӘСфЈ¬ЗТГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйСфРФЈ» 18ФВБдЗ°І»ДЬХп¶ППИМмГ·¶ҫөД¶щНҜЈ¬18ФВБдәуГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйИФСфРФЈ» ЖӨ·фрӨДӨЛрәҰ»тЧйЦҜұкұҫ°өКУТ°ПФОўҫөЈЁ»т¶ЖТшИҫЙ«Ј©јмІвөҪГ·¶ҫВЭРэМеЈ» Г·¶ҫВЭРэМеIgMҝ№МејмІвСфРФЎЈ ЈЁҫЕЈ©ПИМмГ·¶ҫХп¶ПКұјдЈә Дк ФВ ИХ ЈЁК®Ј©Хп¶ПОӘПИМмГ·¶ҫөД¶щНҜКЗ·сҪУКЬЦОБЖЈә ·с КЗ ЈЁК®Т»Ј©ұёЧўЈЁ·ЗұШМоЈ©Јә |
||||||||||||||||||||||||||||||||||||||||||||||||
|
ұЁёжөҘО»ЈЁёЗХВЈ©Јә ұЁёжТҪЙъЈә БӘПөөз»°Јә МоұЁИХЖЪЈә Дк ФВ ИХ |
||||||||||||||||||||||||||||||||||||||||||||||||
|
ұёЧў |
||||||||||||||||||||||||||||||||||||||||||||||||
ЛДЎў°¬ЧМІЎІЎ¶ҫёРИҫФРІъёҫ/»йјмёҫЕ®өЗјЗҝЁЈЁұЈГЬЈ©МоҝЁЛөГч
ЈЁТ»Ј©ұҫөЗјЗҝЁЦРЈ¬ОҙұкГчЎ°·ЗұШМоЎұөДПоДҝҫщОӘұШРлМоРҙПоЈЁМшЧӘПоДҝіэНвЈ©ЎЈ
ЈЁ¶юЈ©ұҫөЗјЗҝЁЦРЈ¬ОҙұкГчЎ°¶аСЎЎұөДСЎФсМвЈ¬Т»ВЙОӘЎ°өҘСЎЎұЎЈ
ЈЁИэЈ©ұҫөЗјЗҝЁЦРЛщУРөДИХЖЪҫщОӘ№«АъИХЖЪЈ¬Дк·Э4О»ЎўФВ·Э2О»ЎўИХЖЪ2О»ЎЈИфФВ·Э»тИХЖЪІ»Чг2О»КұЈ¬ФтФВ·Э»тИХЖЪөДөЪ1О»МоЎ°0ЎұЎЈФВ·ЭЎўИХЖЪҫщІ»ПкКұЈ¬МоРҙЎ°07ЎұФВЎ°01ЎұИХЈ»ТСЦӘДк·ЭЎўФВ·ЭЈ¬ҪцИХЖЪІ»ПкКұЈ¬МоРҙЎ°15ЎұИХЎЈ
ЈЁЛДЈ©ұа әЕЈә
өЪТ»Іҝ·ЦЈ¬6О»Ј¬РРХюЗш»®ҙъВлЈ¬°ҙ№ъјТНіјЖҫЦ№«ІјұкЧјЦҙРРЈ»
өЪ¶юІҝ·ЦЈ¬3О»Ј¬ТҪФәЦъІъ»ъ№№ұаВлЈ¬УЙөұөШОАЙъҫЦНіТ»ұаЦЖЈ»
өЪИэІҝ·ЦЈ¬4О»Ј¬МоұЁДк¶ИұаВлЈ¬МоРҙМоұЁЛщКфДк·ЭЈ»
өЪЛДІҝ·ЦЈ¬3О»Ј¬ёцИЛЛіРтұаВлЈ¬°ҙГҝёцТҪБЖЦъІъ»ъ№№МоұЁЛіРтТАҙОұаВлЎЈ
Гҝёц»йјмёҫЕ®ЎўГҝёцФРІъёҫөДГҝТ»ҙОИСЙпРл¶ФУҰТ»ёцОЁТ»өДұаәЕЎЈ
ЈЁОеЈ©КЎЈЁЗшЎўКРЈ©ЎўПШЎўТҪФәЈЁёҫУЧұЈҪЎФәЈ©ЈәЗлҫЭКөМоРҙЈ¬ЧўТвУлұаВлөЪТ»Ўў¶юЎўИэІҝ·ЦДЪИЭТ»ЦВЎЈ
ұн3ЁCўс °¬ЧМІЎІЎ¶ҫёРИҫФРІъёҫ/»йјмёҫЕ®»щұҫЗйҝцөЗјЗҝЁ
Т»Ўў»щұҫЗйҝц
РХ ГыЈәЗлМоРҙ°¬ЧМІЎІЎ¶ҫёРИҫФРІъёҫ/»йјмёҫЕ®өДРХГыЈ¬УлЙн·ЭЦӨЈЁ»т»§ҝЪұҫЎўҫь№ЩЦӨөИУРР§ЦӨјюЈ©ЙПөДРХГыТ»ЦВЎЈ
Йн·ЭЦӨәЕЈәұШРлМоРҙЈ¬јИҝЙМоРҙ18О»Йн·ЭЦӨәЕВлЈ¬ТІҝЙМоРҙ15О»Йн·ЭЦӨәЕВлЎЈИз№ыИ·КөОЮ·Ё»сөГЙн·ЭЦӨәЕЈ¬ФтЈә
З°6О»МоРҙМоұЁПШЈЁКРЎўЗшЈ©өДРРХюЗш»®ҙъВлЈ»
өЪ7-10О»МоРҙіцЙъДк·ЭЈ»
өЪ11-12О»МоРҙіцЙъФВ·ЭЈ»
өЪ13-14О»МоРҙіцЙъИХЖЪЈ»
өЪ15-18О»МоРҙЈәЧФ9999ҝӘКјТАҙОДжРтұаРҙЈ¬Из9999Ј¬9998Ј¬9997өИЎЈ
іцЙъИХЖЪЈәЗлМоРҙ№«АъіцЙъөДДкФВИХЎЈИзИ·КөОЮ·Ё»сөГЈ¬ЗлМоРҙЦЬЛкЎЈ
Гс ЧеЈәЗлФЪПаУҰГсЧеЗ°»®Ў°ЎМЎұЎЈИзСЎФсЖдЛыЈ¬ЗлПкПёЛөГчЎЈ
ОД»ҜіМ¶ИЈәЗлФЪПаУҰОД»ҜіМ¶ИЗ°»®Ў°ЎМЎұЎЈОД»ҜіМ¶ИКЗЦёФРІъёҫ/ёҫЕ®ҪУКЬ№ъДЪНвҪМУэЛщИЎөГөДЧоёЯС§Аъ»тУлПЦУРОД»ҜЛ®ЖҪПаөұөДС§АъЎЈОДГӨ/°лОДГӨЈәЦёІ»К¶ЧЦ»тК¶ЧЦІ»Чг1500ёцЈ¬І»ДЬФД¶БНЁЛЧКйұЁЈ¬І»ДЬРҙұгМхөДИЛЈ»РЎС§ЈәЦёҪУКЬЧоёЯТ»ј¶ҪМУэОӘРЎС§іМ¶ИөДұПТөЎўТЮТөЙъЈ¬ТІ°ьАЁГ»УРЙП№эРЎС§Ј¬ө«К¶ЧЦі¬№э1500ёцЈ¬ДЬФД¶БНЁЛЧКйұЁЈ¬ДЬРҙұгМхЈ¬ҙпөҪЙЁГӨұкЧјөДИЛЈ»іхЦРЈәЦёҪУКЬЧоёЯТ»ј¶ҪМУэОӘіхЦРіМ¶ИөДұПТөЎўТЮТөј°ФЪРЈЙъЈ¬јј№ӨѧУЈ¬ПаөұУЪіхЦРөДЈ¬МоРҙЎ°іхЦРЎұЈ»ёЯЦРЈәЦёҪУКЬЧоёЯТ»ј¶ҪМУэОӘЖХНЁёЯЦРЎўЦ°ТөёЯЦРј°ЦРЧЁіМ¶ИөДұПТөЎўТЮТөј°ФЪРЈЙъЈ¬јј№ӨѧУЈ¬ПаөұУЪёЯЦРөДЈ¬МоРҙЎ°ёЯЦРЎұЈ»ҙуЧЁ»тҙуС§ЈәЦёҪУКЬЧоёЯТ»ј¶ҪМУэОӘҙуС§ЧЁҝЖ»тұҫҝЖөДұПТөЎўТЮТөј°ФЪРЈЙъЈ¬НЁ№эЧФС§ҫӯ№э№ъјТНіТ»ҫЩ°мөДЧФС§ҝјКФИЎөГҙуС§ЧЁҝЖ»тұҫҝЖЦӨКйөДЈ¬ТІМоРҙЎ°ҙуЧЁ»тҙуС§ЎұЈ»Л¶Кҝј°ТФЙПЈәЦёҪУКЬЧоёЯТ»ј¶ҪМУэОӘЛ¶КҝСРҫҝЙъј°ТФЙПөДұПТөј°ФЪРЈЙъЎЈ
Ц° ТөЈәЗлФЪПаУҰЦ°ТөЗ°»®Ў°ЎМЎұЎЈ
»йТцЧҙҝцЈәЗлМоРҙұҫҙОҪУКЬФӨ·А°¬ЧМІЎДёУӨҙ«ІҘ·юОсКұөД»йТцЧҙҝцЎЈОҙ»йЦёҙУОҙҪб№э»йЎЈіх»йЦёөЪТ»ҙОҪб»йЈ»ФЩ»йЦёАл»й»тЙҘЕјәуФЩҙОҪб»йЎЈН¬ҫУЦёОҙ°мАн№ъјТ·ЁВЙ»йТцөЗјЗКЦРшЈ¬ө«Н¬ҫУ№ІН¬Йъ»оЎЈАл»йЦёТтёчЦЦФӯТтЈ¬·тЖЮЛ«·ҪТСҪвіэ»йТц№ШПөХЯІўЗТОҙФЩ»йЎЈЙҘЕјЦёЕдЕјИҘКАОҙФЩ»йЎЈ
ФРІъЗйҝцЈәФРҙОЈәМоРҙЛщУРөДИСЙпҙОКэЈЁә¬ұҫҙОЈ©Ј»ІъҙОЈ¬МоРҙјИНщВъ28ЦЬәуИСЙпЦХЦ№өДҙОКэЈ¬І»ҝјВЗИСЙпЦХЦ№·ҪКҪј°ИСЙпҪбҫЦЈЁІ»ә¬ұҫҙОЈ©ЎЈ
ПЦ ЧЎ Ц·ЈәЗлПкПёМоРҙФРІъёҫ/»йјмёҫЕ®ПЦҫУЧЎөШЦ·Ј¬ҫЯМеөҪГЕЕЖәЕЎЈ
»§ҝЪЛщФЪөШЈәЗлПкПёМоРҙФРІъёҫ/»йјмёҫЕ®өД»§ҝЪЛщФЪөШЦ·Ј¬ҫЯМеөҪГЕЕЖәЕЎЈ
№ӨЧчөҘО»ЈәЗлМоРҙФРІъёҫ/»йјмёҫЕ®өД№ӨЧчөҘО»ГыіЖЈ¬Из№ыГ»УР№ӨЧчөҘО»Ј¬ЗлМоРҙЎ°ОЮЎұЎЈ
БӘПөөз»°ЈәЗлМоРҙФРІъёҫ/»йјмёҫЕ®өДБӘПө·ҪКҪЎЈ
ФРІъёҫ/ёҫЕ®КфУЪЈәЗлФЪПаУҰөДАаұрЗ°»®Ў°ЎМЎұЈ¬УГУЪұкК¶ФРІъёҫ/ёҫЕ®ПЦЧЎөШЦ·УлТҪБЖЦъІъ»ъ№№ЛщФЪПҪЗшөД№ШПөЎЈ
¶юЎў°¬ЧМІЎІЎ¶ҫёРИҫПа№ШЗйҝц
ГчИ·°¬ЧМІЎІЎ¶ҫёРИҫКұЖЪЈәҫӯІ№ідКФСйұ»И·ИПёРИҫ°¬ЧМІЎІЎ¶ҫөДКұЖЪЎЈИфСЎФсЖдЛыЈ¬ЗлҫЯМеЛөГчЎЈ
ГчИ·°¬ЧМІЎІЎ¶ҫёРИҫҫЯМеКұјдЈәҫЎҝЙДЬМоРҙФРІъёҫ/ёҫЕ®ҫӯІ№ідКФСйұ»И·ИПёРИҫ°¬ЧМІЎІЎ¶ҫөДҫЯМеКұјдЎЈФВ·ЭІ»ПкКұЈ¬МоРҙЎ°07ЎұФВЎЈИХЖЪІ»ПкКұЈ¬МоРҙЎ°15ЎұИХЎЈ
ұҫҙОИСЙпЗ°КЗ·сТСЦӘHIVёРИҫЈЁҪцёРИҫФРІъёҫМоРҙЈ©ЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИзФЪұҫҙОИСЙпЗ°ТСЦӘHIVёРИҫХЯЈ¬ЗлјЖЛгұҫҙОИСЙпОӘХп¶ПHIVёРИҫәуөДөЪјёҙОИСЙпЎЈ
ЧоҝЙДЬөД°¬ЧМІЎІЎ¶ҫёРИҫНҫҫ¶ЈәёщҫЭ°¬ЧМІЎІЎ¶ҫёРИҫФРІъёҫ/ёҫЕ®өДёЯОЈРРОӘәНОЈПХТтЛШЕР¶ПЖдҝЙДЬРФЧоҙуөДёРИҫНҫҫ¶ЎЈИфСЎФсЖдЛыЈ¬ЗлҫЯМеЛөГчЎЈ
ЧўЙд¶ҫЖ·Јә°ьАЁҫІВц»тјЎИвөИЧўЙд¶ҫЖ·Ј¬МШұрКЗУР№э№ІУГЧўЙдЖчҫӯАъөДЈ¬І»°ьАЁөҘҙҝҝЪОьЎўұЗОьөИІ»ҙМЖЖЖӨ·фЎўХіДӨөДОь¶ҫ·ҪКҪЎЈ
РФ ҙ« ІҘЈәЦёНЁ№эУлТмРФЦ®јдөДРФҪУҙҘҙ«ІҘЎЈ
ІЙСӘЈЁҪ¬Ј©ЈәЦёПЧСӘ/СӘҪ¬өИЎЈ
КдСӘ/СӘЦЖЖ·ЈәЦёКдКЬ№эИ«СӘ/іЙ·ЭСӘ/СӘҪ¬/СӘЦЖЖ·өИЎЈ
ДёУӨҙ«ІҘЈәЦё°¬ЧМІЎёРИҫФРІъёҫНЁ№эИСЙпЎў·ЦГдЎўДёИйО№СшөИ№эіМК№ЖдЛщЙъ¶щНҜұ»ёРИҫЎЈ
Ц°Төұ©В¶ЈәЦёКөСйКТЎўТҪ»ӨЎўФӨ·АұЈҪЎөИУР№ШИЛФұЈ¬ФЪҙУКВ°¬ЧМІЎ·АЦО№ӨЧчј°Па№Ш№ӨЧчөД№эіМЦРТвНвұ»°¬ЧМІЎ¶ҫёРИҫХЯ»т°¬ЧМІЎІЎИЛөДСӘТәЎўМеТәОЫИҫБЛЖЖЛрөДЖӨ·ф»т·ЗОёіҰөАХіДӨЈ¬»тұ»ә¬УР°¬ЧМІЎІЎ¶ҫөДСӘТәЎўМеТәОЫИҫБЛөДХлН·ј°ЖдЛыИсЖчҙМЖЖЖӨ·фҙ«ІҘЎЈ
І» ПкЈәЦёёРИҫНҫҫ¶ОЮ·ЁЕР¶ПЎЈ
Жд ЛыЈәЙПКцОҙБРҫЩЈ¬ө«ҝЙДЬФміЙ°¬ЧМІЎІЎ¶ҫҙ«ІҘөДҪУҙҘК·ЎЈИзФЪҙЛСЎПоЗ°»®Ў°ЎМЎұЈ¬УҰФЪәуГжҝХ°ЧҙҰҪшРРЛөГчЎЈ
Па№ШОЈПХРРОӘЈәҝЙ¶аСЎЈ¬ЗлФЪККәПөДСЎПоЗ°»®Ў°ЎМЎұЎЈИфСЎФсЖдЛыЈ¬ЗлҫЯМеЛөГчЎЈ
УлHIVёРИҫЕдЕј»тДРУСөДРФЙъ»оЈәЦёЕдЕј»т№М¶ЁРФ°йТСұ»И·ИПОӘ°¬ЧМІЎІЎ¶ҫҝ№МеСфРФЎЈ
¶а РФ °йЈәЦё·ЗЙМТөРФөДУРТ»ёц»т¶аёц·З»йТмРФРФ°йЎЈ
ЙМТөРФРРОӘЈәЦёВфТщ»тжОжҪРФРРОӘЎЈ
ЧўЙдОь¶ҫЈәН¬З°ЛщКцЎЈ
УРіҘІЙ№©СӘЈәЦёУРіҘөШПЧЈЁ№©Ј©СӘ»тСӘҪ¬ЎЈ
КдСӘ»тК№УГСӘЦЖЖ·ЈәН¬З°ЛщКцЎЈ
ОЖЙн»тҙ©¶ъөИЙнМеҙМЙЛЈәЦёОЖЙн»тҙ©¶ъөИК№УГИсЖчҙМЙЛЖӨ·фөДРРОӘЎЈ
ТвНвЙЛәҰЈәЦёҝЙДЬФміЙёРИҫөДТвНвөДЙЛәҰЎЈ
Ц°Төұ©В¶ЈәН¬З°ЛщКцЎЈ
ТҪФҙРФёРИҫЈәТтОӘҫНТҪЎўҫНХпЈЁ°ьАЁКЦКхЎўҝЪЗ»ЎўДЪҝъҫөөИЛщУРЗЦИлРФІЩЧчәНёчАаКЦКхЈ©¶шКЬөҪёРИҫЎЈ
І» ПкЈәЦёОЈПХРРОӘОЮ·ЁЕР¶ПЎЈ
Жд ЛыЈәЙПКцОҙБРҫЩЈ¬ө«ҝЙДЬФміЙ°¬ЧМІЎІЎ¶ҫҙ«ІҘөДОЈПХРРОӘЎЈИзФЪҙЛСЎПоЗ°»®Ў°ЎМЎұЈ¬
УҰФЪәуГжҝХ°ЧҙҰҪшРРЛөГчЎЈ
ИэЎўХЙ·т/РФ°йЗйҝц
РХ ГыЈәХЙ·т»тРФ°йөДРХГыЎЈИзХЙ·тј°РФ°йі¬№э1ИЛЈ¬ҝЙБнёҪёГХЕұнёсЙПұЁЎЈ
іцЙъИХЖЪЈәЗлҫЎҝЙДЬМоРҙХЙ·т»тРФ°йөДіцЙъИХЖЪЎЈИзИ·КөОЮ·Ё»сөГЈ¬ЗлМоРҙКөЧгДкБдЎЈ
Гс ЧеЈәЗлФЪПаУҰөДГсЧеЗ°»®Ў°ЎМЎұЎЈИзСЎФсЖдЛыЈ¬ЗлПкПёЛөГчЎЈ
ОД»ҜіМ¶ИЈәЗлФЪПаУҰОД»ҜіМ¶ИЗ°»®Ў°ЎМЎұЎЈҫЯМеЛөГчН¬З°ЎЈ
Ц° ТөЈәЗлФЪПаУҰЦ°ТөЗ°»®Ў°ЎМЎұЎЈ
HIVјмІвЗйҝцЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈСЎФсІ»Пк»тОҙјмІвХЯМшөҪЎ°Па№ШОЈПХРРОӘЈЁ¶аСЎЈ©ЎұҙҰЎЈҫЎҝЙДЬМоРҙЖдГчИ·ёРИҫКұјдЈ¬ҫЯМеЛөГчН¬З°ЎЈ
ЧоҝЙДЬөД°¬ЧМІЎІЎ¶ҫёРИҫНҫҫ¶ЈәЗлФЪПаУҰёРИҫНҫҫ¶З°»®Ў°ЎМЎұЎЈҫЯМеЛөГчН¬З°ЎЈЖдЦРЈ¬
ТмРФҙ«ІҘЈәЦёНЁ№эУлТмРФЦ®јдөДРФҪУҙҘҙ«ІҘЎЈ
Н¬РФҙ«ІҘЈәЦёНЁ№эУлН¬РФЦ®јдөДРФҪУҙҘҙ«ІҘЎЈ
Па№ШОЈПХРРОӘЈәҝЙ¶аСЎЈ¬ЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈҫЯМеЛөГчН¬З°ЎЈЖдЦРЈ¬
¶аРФ°йЈәЦё·ЗЙМТөРФөДУРТ»ёц»т¶аёц·З»йТмРФ/Н¬РФРФ°йЎЈ
Н¬РФРФРРОӘЈәЦёУлН¬РФЦ®јдөДРФРРОӘЎЈ
ЛДЎўұҫҙОҪУКЬФӨ·А°¬ЧМІЎДёУӨҙ«ІҘ·юОсЗйҝц
ұҫҙОҪУКЬФӨ·А°¬ЧМІЎДёУӨҙ«ІҘ·юОсөДКұЖЪЈәЗлёщҫЭұҫҙОҪУКЬ·юОсөДКұЖЪЈ¬ФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИф»йЗ°јмІйөДёҫЕ®»іФРЈ¬Фт°ҙФРёҫөЗјЗЈ¬ФЪЎ°ФРЖЪЎұСЎПоЗ°»®Ў°ЎМЎұЈ¬°ҙФРёҫТӘЗуМоұЁПа№Шёц°ёөЗјЗҝЁЎЈ
°¬ЧМІЎјмІвЗ°ЧЙСҜЗйҝцЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈ
°¬ЧМІЎјмІвәуЧЙСҜЗйҝцЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈ
ұЁёжИЛј°ұЁёжөҘО»РЕПў
ұЁёжөҘО»ЈЁёЗХВЈ©ЈәЗлМоРҙұЁёжөҘО»өДГыіЖЈ¬ІўёЗХВЎЈ
ұЁёжТҪЙъЈәЗлМоРҙұЁёжТҪЙъөДРХГыЎЈ
БӘПөөз»°ЈәЗлМоРҙМоұЁөҘО»БӘПөөз»°ЎЈ
МоұЁИХЖЪЈәЦёМоРҙұҫөЗјЗҝЁөДИХЖЪЎЈ
ұё ЧўЈәҝЙМоРҙТ»Р©ОДЧЦРЕПўЈ¬ТФІ№ідөЗјЗҝЁЦРОҙҫЎөДКВПоЎЈ
»йјмёҫЕ®НкіЙұҫөЗјЗҝЁјҙҪб°ёЎЈ
ұн3ЁCўтЎў°¬ЧМІЎІЎ¶ҫёРИҫФРІъёҫИСЙпј°ЛщЙъУӨ¶щөЗјЗҝЁ
РХ ГыЈәЗлМоРҙ°¬ЧМІЎІЎ¶ҫёРИҫФРІъёҫөДРХГыЈ¬Улұн3ЁCўсөДРХГыТ»ЦВЎЈ
Йн·ЭЦӨәЕЈәУлұн3ЁCўсөДЙн·ЭЦӨәЕТ»ЦВЎЈ
Т»ЎўұҫҙОИСЙпј°ФРІъЖЪұЈҪЎЗйҝц
ұҫҙОИСЙпД©ҙОФВҫӯКұјдЈәЗлМоРҙ№«АъИХЖЪЎЈД©ҙОФВҫӯКұјдЦёЧоәуТ»ҙОФВҫӯАҙіұөДөЪТ»МмЎЈ
ФӨ Іъ ЖЪЈәЗлёщҫЭұҫҙОИСЙпД©ҙОФВҫӯКұјдјЖЛгІўМоРҙФӨІъЖЪЎЈФӨІъЖЪјЖЛ㹫КҪЈәД©ҙОФВҫӯөЪТ»МмөДФВ·ЭКэјх3ЈЁ»тФВ·ЭКэЎЬ3КұјУ9Ј©Ј¬ИХЖЪКэјУ7јҙОӘФӨІъЖЪөДИХЖЪЎЈУҰУГ№«АъИХЖЪјЖЛгЎЈ
іхјмФРЦЬЈәЗлМоРҙФРІъёҫөЪТ»ҙОҪУКЬФРІъЖЪұЈҪЎөДКұјдЎЈФРЦЬЧФұҫҙОИСЙпД©ҙОФВҫӯКұјдҝӘКјјЖЛгЎЈ
ИСЙпҪбҫЦЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈ·ЦГдЦёИСЙпВъ28ЦЬЈЁ196ИХЈ©ј°ТФәуЈ¬МҘ¶щј°ЖдёҪКфОпҙУДёМеГдіцЎЈЧФИ»БчІъЦёЈ¬ИСЙпІ»Чг28ЦЬЎўМҘ¶щМеЦШІ»Чг1000ҝЛЈ¬ОЮИЛОӘТтЛШЗйҝцПВЈ¬ИСЙпЦХЦ№ЎЈИЛ№ӨЦХЦ№ИСЙпЦёЈ¬ИСЙпІ»Чг28ЦЬЎўМҘ¶щМеЦШІ»Чг1000ҝЛЈ¬ИЛОӘёЙФӨөДИСЙпЦХЦ№ЎЈИзСЎФсЖдЛыЈ¬ЗлПкПёЛөГчЎЈ
КЗ·сК§·ГЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈК§·ГКұЖЪЗлМоРҙЧоәуТ»ҙОЛж·ГКұөДФРЦЬ»тІъәуЦЬКэЎЈ
ИСЙпҪбҫЦОӘЎ°ЧФИ»БчІъЎұЎўЎ°ИЛ№ӨЦХЦ№ИСЙпЎұ»тЎ°ЖдЛыЎұХЯЈ¬І»ұШМоРҙұҫөЗјЗҝЁөДЖдУаІҝ·ЦЈ¬МоРҙНкЎ°КЗ·сК§·ГЎұәуЈ¬МшЦБЎ°ұЁёжөҘО»ЎұҙҰЈ¬ІўҪб°ёЎЈ
ФРІъЖЪТміЈЗйҝцЈЁ¶аСЎЈ©ЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЈ¬јІІЎРиҫӯ№эПзј¶ЈЁә¬Ј©ТФЙПТҪБЖОАЙъ»ъ№№Хп¶ПЎЈИфСЎФсЖдЛыЈ¬ЗлҫЯМеЛөГчЎЈ
·ЦГд·ҪКҪЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈЧФИ»·ЦГдЦёМҘ¶щҫӯТхөАЧФИ»ГдіцөД·ЦГд·ҪКҪЈ»ТхөАЦъІъЦёФЪөЪ¶юІъіМ№¬ҝЪҝӘИ«ә󣬶Բ»ДЬҙУТхөАЧФИ»ГдіцөДІъёҫЈ¬ФЛУГЖчРөРӯЦъІъёҫҪ«МҘ¶щГдіцөД·ЦГд·ҪКҪЈ»ФсЖЪЖК№¬ІъЦёБЩІъЗ°өДЖК№¬ІъЈ»јұХпЖК№¬ІъЦёБЩІъТФәуөДЖК№¬ІъЎЈ
·ЦГдКұјдЈәЦёМҘ¶щГдіцөДКұјдЎЈТхөАІъМоРҙЧЬІъіМЎЈФРЦЬТФј°ЧЬІъіМөДјЖЛгН¬З°ЛщКцЎЈ
·ЦГдөШөгЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИфСЎФсЖдЛыЈ¬ЗлҫЯМеЛөГчЎЈ
ІъҝЖІЩЧчЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЈ¬ИфСЎФсЖдЛыЈ¬ЗлПкПёЛөГчЎЈ
»бТхБСЙЛЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈ
·ЦГдМҘКэЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЈ¬ИфСЎФсЖдЛыЈ¬ЗлПкПёЛөГчЎЈ
ФРІъёҫҪбҫЦЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈЛАНцФӯТтЗл°ҙХХЎ°ҫУГсЛАНцТҪС§ЦӨГчКйЎұТӘЗуМоРҙЦұҪУЦВЛАјІІЎГыіЖЎЈ
ТФПВЙжј°¶аМҘО§Іъ¶щј°УӨ¶щөДРЕПўЈ¬ҝЙБнёҪёГұнЙПұЁЎЈ
О§Іъ¶щЧӘ№йЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈ»оІъЦёЈ¬ИСЙп28ЦЬәуЈ¬МҘ¶щНСАлДёМеКұЈ¬УР№эЛДЦЦЙъГьПЦПуЈЁ°ьАЁәфОьЎўРДМшЎўЛжТвјЎКХЛхәНЖкҙшІ«¶ҜЈ©Ц®Т»ХЯЈ»ЛАМҘЦёЈ¬ИСЙп28ЦЬәуМҘ¶щФЪЧУ№¬ДЪЛАНцЈ»ЛАІъЦёЈ¬МҘ¶щФЪГдіц№эіМЦРЛАНцЈ»РВЙъ¶щЖЯМмДЪЛАНцЈЁјҙФзЖЪРВЙъ¶щЛАНцЈ©ЦёЈ¬»оІъ¶щФЪіцЙъәуОҙВъ7МмЛАНцЎЈИф·ўЙъЖЯМмДЪЛАНцЈ¬ФтОЮРиФЪЎ°»оІъЎұСЎПоЗ°»®Ў°ЎМЎұЎЈ
О§Іъ¶щТміЈЗйҝцЈЁ¶аСЎЈ©ЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈјІІЎРиҫӯ№эПзј¶ЈЁә¬Ј©ТФЙПТҪБЖОАЙъ»ъ№№Хп¶ПЈ¬°ьАЁФзІъ»төНіцЙъМеЦШЎўРВЙъ¶щ·ОСЧЈЁ°ьАЁУЪ№¬ДЪЎў·ЦГд№эіМЦРёРИҫөДОьИлРФ·ОСЧЈ¬ТФј°УЪіцЙъәу7МмДЪёРИҫөДРВЙъ¶щФз·ўРН·ОСЧЈ©ЎўРВЙъ¶щЦППўЎўіцЙъИұПЭЎЈИфСЎФсіцЙъИұПЭЈ¬ЗлМоРҙҫЯМеИұПЭАаРНЈ¬ИфСЎФсЖдЛыЈ¬ЗлПкПёЛөГчЎЈ
Лж·ГЗйҝцЈәЗлёщҫЭФРЖЪЛж·ГҙОКэМоРҙПаУҰөДКэЧЦЎЈИз№ыГ»УРЛж·ГЈ¬ЗлМоРҙЎ°00Ўұ»тЎ°0ЎұЎЈ
¶юЎўФРІъёҫҝ№°¬ЧМІЎІЎ¶ҫТ©ОпУҰУГЗйҝц
ЗлёщҫЭФРІъёҫУҰУГҝ№°¬ЧМІЎІЎ¶ҫТ©ОпөДЗйҝцЈ¬ФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИфЎ°ОҙУГТ©ЎұЈ¬МшЦБЎ°ИэЎўФРІъёҫёҙ·ҪРВЕөГчУГТ©ЗйҝцЎұҙҰЎЈ
ҝӘКјУГТ©КұјдЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИфФРЖЪҝӘКјУГТ©Ј¬ЗлМоРҙПаУҰөДФРЦЬЈ¬ФРЦЬөДјЖЛгН¬З°ЛщКцЎЈФРЖЪЦёИСЙпЦББЩІъЗ°Ј»ІъКұЦёБЩІъҝӘКјЦБ·ЦГдҪбКшЈЁМҘ¶щМҘЕМГдіцЈ©Ј¬Иф·ЦГд·ҪКҪОӘЎ°ФсЖЪЖК№¬ІъЎұЈ¬ФтҙУЖК№¬ІъЗ°2РЎКұҝӘКјјЖЛгЈ»ІъәуЦё·ЦГдҪбКшТФәуЎЈ
Т©ОпГыіЖЈәЗлМоРҙУҰУГТ©ОпөД3О»ЛхРҙГыіЖЈ¬ЧўТвМоРҙГҝТ»ёцУГТ©КұЖЪҫЯМеУҰУГТ©ОпөДГыіЖЈ¬¶шІ»КЗМоРҙХыёцФРЖЪЎўІъКұј°ІъәуУГТ©·Ҫ°ёЦРөДЛщУРТ©ОпЎЈіЈУГТ©ОпЛхРҙ°ьАЁЈәЖл¶а·т¶ЁЎӘAZTЈ¬ДООӨАӯЖҪЎӘNVPЈ¬АӯГЧ·т¶ЁЎӘ3TCЈ¬ҝЛБҰЦҘЎӘ LPV/rЈ¬МжЕөёЈОӨЎӘ TDF Ј¬ТА·ЗОӨВЧЎӘEFVөИЎЈ·ЦФРЖЪЎўІъКұЎўІъәуИэёцКұЖЪМоРҙЈ¬ёчКұЖЪЛөГчИзЗ°ЛщКцЎЈ
В©·юЗйҝцЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈ·ЦФРЖЪЎўІъКұЎўІъәуИэёцКұЖЪЈЁёчКұЖЪЛөГчН¬З°ЛщКцЈ©МоРҙЈ¬ИфУРВ©·юЈ¬ЗлМоРҙёГКұЖЪҫЯМеВ©·юөДЧЬҙОКэЎЈ
НЈЦ№УГТ©ЗйҝцЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИфТСНЈТ©Ј¬ЗлМоРҙҫЯМеНЈТ©КұјдЈ¬ёчКұЖЪЛөГчј°ФРЦЬөДјЖЛгН¬З°ЛщКцЎЈ
ИэЎўФРІъёҫёҙ·ҪРВЕөГчУГТ©Зйҝц
ЗлёщҫЭФРІъёҫёҙ·ҪРВЕөГчУГТ©ЗйҝцЈ¬ФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИфЎ°ОҙУГТ©ЎұЈ¬МшЦБЎ°ЛДЎўФРІъёҫПа№ШјмІвЗйҝцЎұҙҰЎЈ
ҝӘКјУГТ©КұјдЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИфФРЖЪҝӘКјУГТ©Ј¬ЗлМоРҙПаУҰөДФРЦЬЈ¬ФРЦЬөДјЖЛг
Н¬З°ЛщКцЎЈФРЖЪЦёИСЙпЦББЩІъЗ°Ј»ІъКұЦёБЩІъҝӘКјЦБ·ЦГдҪбКшЈЁМҘ¶щМҘЕМГдіцЈ©Ј¬Иф·ЦГд·ҪКҪОӘЎ°ФсЖЪЖК№¬ІъЎұЈ¬ФтҙУЖК№¬ІъЗ°2РЎКұҝӘКјјЖЛгЈ»ІъәуЦё·ЦГдҪбКшТФәуЎЈ
НЈЦ№УГТ©ЗйҝцЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИфТСНЈТ©Ј¬ЗлМоРҙҫЯМеНЈТ©КұјдЈ¬ёчКұЖЪЛөГчј°ФРЦЬөДјЖЛгН¬З°ЛщКцЎЈ
ЛДЎўФРІъёҫПа№ШјмІвЗйҝц
ЗлёщҫЭФРІъёҫФРІъЖЪјмІвЗйҝцЈ¬ФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈ
јмІвФРЦЬ/КұјдЈәМоРҙПаУҰөДКэЧЦЎЈФРЦЬөДјЖЛгН¬З°ЛщКцЎЈ
јмІвҪб№ыЈәЗл°ҙХХұҫөЗјЗҝЁТӘЗуөДјмІвҪб№ыөҘО»МоРҙПаУҰөДКэЦөЎЈДіПоОҙҪшРРјмІвөДЈ¬ЗлТФЎ°/ЎұМоРҙЎЈГ·¶ҫЎўТТёОј°ұыёОөДјмІвЗйҝцј°јмІвҪб№ыЈ¬ЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈ
ОеЎўРВЙъУӨ¶щЗйҝц
Из·ЦГд¶аёцРВЙъУӨ¶щЈ¬ЗлБнёҪёГұн·ЦұрМоұЁЎЈ
РХ ГыЈәЗлМоРҙёРИҫІъёҫ·ЦГдУӨ¶щөДРХГыЈ¬УлЎ°іцЙъТҪС§ЦӨГчЎұөДРХГыТ»ЦВЎЈИз№ыЙРОҙИЎГыЈ¬ЗлГиКцОӘЎ°ёРИҫІъёҫРХГы+Ц®ЧУ/Е®ЎұЎЈ
РФ ұрЈәЗлФЪПаУҰРФұрЗ°»®Ў°ЎМЎұЎЈИз№ыБҪРФ»ыРОЈ¬СЎФсПФРФөДДЗёцРФұрЎЈ
іцЙъИХЖЪЈәЗлМоРҙУӨ¶щіцЙъөД№«АъИХЖЪЎЈ
іцЙъМеЦШЈәЗлМоРҙПаУҰКэЦөЈ¬іцЙъМеЦШЦёУӨ¶щіцЙъ1РЎКұДЪөДМеЦШЈ¬өҘО»ОӘЎ°ҝЛЎұЎЈ
іцЙъЙніӨЈәЗлМоРҙУӨ¶щіцЙъ1РЎКұДЪөДЙніӨАеГЧКэЦөЎЈ
Лж·ГЗйҝцЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈЖдЦРЈ¬ОҙЛж·Г°ьАЁ:1ЎўТҪОсИЛФұОҙЦч¶ҜМṩЛж·Г·юОсЈ»2ЎўТҪОсИЛФұЦч¶ҜМṩЛж·Г·юОсЈ¬ө«ОҙБӘПөөҪЛж·Г¶ФПуЎЈ
ҙж»оЗйҝцЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИфРВЙъУӨ¶щЛАНцЈ¬Зл°ҙХХЎ°ҫУГсЛАНцТҪС§ЦӨГчКйЎұМоРҙТӘЗуМоРҙЦұҪУЦВЛАјІІЎГыіЖЎЈ
ФӨ·АҪУЦЦЗйҝцЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈ
БщЎўРВЙъУӨ¶щҝ№°¬ЧМІЎІЎ¶ҫТ©ОпУҰУГЗйҝц
Из·ЦГд¶аёцРВЙъУӨ¶щЈ¬ЗлБнёҪёГұн·ЦұрМоұЁЎЈ
ЗлёщҫЭРВЙъУӨ¶щУҰУГҝ№°¬ЧМІЎІЎ¶ҫТ©ОпөДЗйҝцЈ¬ФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИфЎ°ОҙУГТ©ЎұЈ¬МшЦБЎ°ұЁёжөҘО»ЈЁёЗХВЈ©ЎұҙҰЎЈ
ҝӘКј/НЈЦ№УГТ©КұјдЈәЗлМоРҙПаУҰөД№«АъИХЖЪЎЈ
Т©ОпГыіЖЈәЗлМоРҙУҰУГТ©ОпөД3О»ЛхРҙГыіЖЎЈіЈУГТ©ОпЛхРҙИзЗ°ЛщКцЎЈ
В©·юЗйҝцЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИфУРВ©·юЈ¬ЗлМоРҙҫЯМеВ©·юөДЧЬҙОКэЎЈ
ұЁёжИЛј°ұЁёжөҘО»РЕПў
ұЁёжөҘО»ЈЁёЗХВЈ©ЈәЗлМоРҙұЁёжөҘО»өДГыіЖЈ¬ІўёЗХВЎЈ
ұЁёжТҪЙъЈәЗлМоРҙұЁёжТҪЙъөДРХГыЎЈ
БӘПөөз»°ЈәЗлМоРҙМоұЁөҘО»БӘПөөз»°ЎЈ
МоұЁИХЖЪЈәЦёМоРҙұҫөЗјЗҝЁөДИХЖЪЎЈ
ұё ЧўЈәҝЙМоРҙТ»Р©ОДЧЦРЕПўЈ¬ТФІ№ідөЗјЗҝЁЦРОҙҫЎөДКВПоЎЈ
ұн3ЁCўуЎў°¬ЧМІЎІЎ¶ҫёРИҫІъёҫј°ЛщЙъ¶щНҜЛж·ГөЗјЗҝЁ
ТӘЗуФЪ¶щНҜВъ1Ўў3Ўў6Ўў9Ўў12әН18ёцФВКұОӘ°¬ЧМІЎІЎ¶ҫёРИҫФРІъёҫ/ДёЗЧј°ЛщЙъ¶щНҜМṩЛж·Г·юОсЈ¬ГҝҙОЛж·ГМоРҙТ»ХЕұҫҝЁЎЈ
ФРІъёҫұаәЕЈәЗлМоРҙ°¬ЧМІЎёРИҫФРІъёҫ/¶щНҜДёЗЧөДұаәЕЈ¬ЧўТвУлұн3ЁCўсЎўұн3ЁCўт°¬ЧМІЎІЎ¶ҫёРИҫФРІъёҫөДұаәЕТ»ЦВЎЈ
¶щНҜұаәЕЈәЗ°4¶ОұаәЕЈЁјҙұаәЕөДЗ°16О»Ј©Ул°¬ЧМІЎёРИҫФРІъёҫ/ДёЗЧұаәЕТ»ЦВЎЈЧоәу1О»°ҙұҫҙО·ЦГдУӨ¶щіцЙъөДҙОРтМоРҙЈәИфОӘөҘМҘЈ¬МоЎ°1ЎұЈ»ИфОӘ¶аМҘЈ¬ФтөЪТ»МҘУӨ¶щМоЎ°1ЎұЎўөЪ¶юМҘУӨ¶щМоЎ°2ЎұЈ¬ТФҙЛАаНЖЎЈ
ФРІъёҫРХГыЈәЗлМоРҙ°¬ЧМІЎёРИҫФРІъёҫ/¶щНҜДёЗЧөДРХГыЈ¬Улұн3ЁCўсЎўұн3ЁCўт°¬ЧМІЎІЎ¶ҫёРИҫФРІъёҫөДРХГыТ»ЦВЎЈ
Йн·ЭЦӨәЕЈәЗлМоРҙ°¬ЧМІЎёРИҫФРІъёҫ/¶щНҜДёЗЧөДЙн·ЭЦӨәЕЈ¬Улұн3ЁCўсЎўұн3ЁCўт°¬ЧМІЎІЎ¶ҫёРИҫФРІъёҫЙн·ЭЦӨәЕТ»ЦВЎЈ
¶щНҜРХГыЈәЗлМоРҙ¶щНҜөДРХГыЎЈҫЯМеМоРҙ·Ҫ·ЁН¬З°ЛщКцЎЈ
РФ ұрЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЈ¬ҫЯМеМоРҙ·Ҫ·ЁН¬З°ЛщКцЎЈ
іцЙъИХЖЪЈәЗлМоРҙУӨ¶щіцЙъөД№«АъИХЖЪЈ¬Улұн3ЁCўтУӨ¶щіцЙъИХЖЪТ»ЦВЎЈ
Гс ЧеЈәМоРҙ·Ҫ·ЁН¬З°ЛщКцЎЈ
ПЦ ЧЎ Ц·ЈәМоРҙ·Ҫ·ЁН¬З°ЛщКцЎЈ
БӘПөөз»°ЈәМоРҙ·Ҫ·ЁН¬З°ЛщКцЎЈ
Лж·ГИХЖЪЈәЗлМоРҙҪшРРЛж·ГөДИХЖЪЎЈ
¶щНҜФВБдЈәЗлМоРҙЛж·ГКұУӨ¶щөДКөЧгФВБдЎЈ
Лж·ГИЛРХГыЈәЗлМоРҙЛж·ГИЛРХГыЎЈ
Т»ЎўёРИҫёҫЕ®Зйҝц
Лж·ГЗйҝцЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИзТСК§·ГЈ¬ЗлМоРҙК§·ГФӯТтЎЈ
ҙж»оЗйҝцЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЈ¬ҫЯМеМоРҙ·Ҫ·ЁН¬З°ЛщКцЎЈ
ЧӘҪй·юОсЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИз№ыМṩБЛЧӘҪй·юОсЈ¬ЗлҫЯМеЛөГчЧӘҪйФӯТтј°ЧӘҪй»ъ№№ЎЈ
ұЬФРЗйҝцЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИфСЎФсЖдЛыұЬФР·Ҫ·ЁЈ¬ЗлҫЯМеЛөГчЎЈ
¶юЎў¶щНҜЗйҝц
Лж·ГЗйҝцЈәМоРҙ·Ҫ·ЁН¬З°ЛщКцЎЈИзФЪ¶щНҜВъ18ФВБдәуөД3ёцФВДЪБ¬РшЛж·Г3ҙОҫщОҙЛж·ГөҪ
ИОәОРЕПўЈ¬ФтұЁёжТСК§·ГЈ¬ІўМоРҙК§·ГФӯТтЎЈ
ҙж»оЗйҝцЈәМоРҙ·Ҫ·ЁН¬З°ЛщКцЎЈ
ЧӘҪй·юОсЈәМоРҙ·Ҫ·ЁН¬З°ЛщКцЎЈ
ЙъіӨ·ўУэЈәЗл°ҙөЗјЗҝЁөҘО»МоРҙПаУҰөДКэЦөЎЈДкБдұрМеЦШЎўДкБдұрЙніӨј°ЙніӨұрМеЦШөДЖАјЫ°ҙХХКАҪзОАЙъЧйЦҜ¶щНҜЙъіӨ·ўУэұкЧјҪшРРЎЈДкБдұрМеЦШЎўДкБдұрЙніӨј°ЙніӨұрМеЦШИфөНУЪ2ёцұкЧјІоЈЁ<ЁC2sЈ©Ј¬ЖАјЫОӘПВЈ»ФЪЙПЎўПВ2ёцұкЧјІоЦ®јдЈ¬ЈЁЎЭ ЁC2s ~ < 2sЈ©Ј¬ЖАјЫОӘЦРЈ»өИУЪ»тёЯУЪ2ёцұкЧјІоЈЁЎЭ 2sЈ©Ј¬ЖАјЫОӘЙПЎЈ
О№Сш·ҪКҪЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈҙҝДёИйО№СшЦёЈ¬Ц»УГДёИйО№СшУӨ¶щЈ¬іэО¬ЙъЛШЎўОўБҝФӘЛШЦЖјБ»тТ©ОпНвЈ¬І»ёшУӨ¶щИОәОЖдЛыТәМе»т№ММеЧҙКіОпЈЁ°ьАЁЛ®Ј©Ј»ИЛ№ӨО№СшЦёЈ¬НкИ«ІЙУГЕд·ҪДМЎўКЮИй»тЖдЛыДёИйМжҙъЖ·О№ІёУӨ¶щЈ»»мәПО№СшЦёЈ¬ТФДёИйО№ІёУӨ¶щЈ¬ө«Н¬Кұ»№ТФЖдЛыТәМе»т№ММеЧҙКіОпЈЁ°ьАЁЛ®ЎўЕд·ҪДМЎўЖдЛыКЮИй»тДёИйМжҙъЖ·өИЈ©О№ІёУӨ¶щЈ»ЖдЛыЦёЛж·ГЖЪјдУӨ¶щөДО№Сш·ҪКҪ·ўЙъёДұдЈ¬ЗлҫЯМеЛөГчУЙәОЦЦО№Сш·ҪКҪЧӘұдіЙәОЦЦО№Сш·ҪКҪТФј°ГҝЦЦО№Сш·ҪКҪіЦРшөДКұјдЎЈ
ёЁКіМнјУЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИфТСМнјУЈ¬ЗлМоРҙҝӘКјМнјУөДКөЧгФВБдЈ¬МоұЁТ»ҙОјҙҝЙЎЈ
јІІЎЗйҝцЈЁ¶аСЎЈ©ЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЈ¬јІІЎРиҫӯ№эПзј¶ЈЁә¬Ј©ТФЙПТҪБЖОАЙъ»ъ№№Хп¶ПЎЈИфСЎФсЖдЛыЈ¬ЗлҫЯМеМоРҙјІІЎөДГыіЖЎЈ
Па№ШЦўЧҙЈЁ¶аСЎЈ©ЈәЗлёщҫЭ¶щНҜјТКфЦчЛЯј°ІйМеЛщјыЈ¬ФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИфСЎФсЖдЛыЈ¬ЗлҫЯМеЛөГчЎЈ
ФӨ·АҪУЦЦЗйҝцЈәЗлёщҫЭ¶щНҜФӨ·АҪУЦЦК·өДЗйҝцЈ¬ФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИзҪУЦЦБЛЖдЛыТЯГзЈ¬ЗлПкПёГиКцЎЈИз№ыУӨ¶щФӨ·АҪУЦЦТЯГзөДЦЦАаІ»Н¬УЪ№ъјТГвТЯ№ж»®ЦРТЯГзөДЦЦАаЈ¬ЗлПкПёЛөГчЎЈАэИзЈ¬Из№ыУӨ¶щҪУЦЦБЛГр»оөДј№Ли»ТЦКСЧТЯГзЈ¬РиТӘПкПёЛөГчЎЈ
HIVјмІвЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИфФЪұҫЛж·ГҪЧ¶ОЦР¶аҙОјмІвЈ¬ЗлМоРҙХвёцКұЖЪөЪТ»ёцјмІв·Ҫ·ЁөДҫЯМеИХЖЪЎЈИфОҙјмІвЈ¬МшЦБЎ°ЈЁК®ИэЈ©ФӨ·АУҰУГёҙ·ҪРВЕөГчЎЈ
HIVјмІвҪб№ыЈәЗлҪ«ұҫЛж·ГҪЧ¶ОЦРёьёЯј¶ұрјмІвөДҪб№ыФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИфСЎФсЖдЛыЈ¬ЗлҫЯМеЛөГчЎЈ
HIVјмІв·Ҫ·ЁЈЁҝЙ¶аСЎЈ©ЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈ12ФВБдЗ°УӨ¶щHIVёРИҫФзЖЪХп¶ПјмІвј°12~18ФВБдјдҪшРРөДәЛЛбјмІв№йОӘЎ°ФзЖЪәЛЛбјмІвЎұЈ»18ФВБдј°ТФЙПөДәЛЛбјмІв№йОӘЎ°І№ідКФСйЎұЎЈИфСЎФсЖдЛыЈ¬ЗлҫЯМеЛөГчЎЈ
ФӨ·АУҰУГёҙ·ҪРВЕөГчЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИзТСНЈТ©Ј¬ЗлМоРҙНЈТ©КұјдәННЈТ©ФӯТтЎЈ
ұё ЧўЈәҝЙМоРҙТ»Р©ОДЧЦРЕПўЈ¬ТФІ№ідөЗјЗҝЁЦРОҙҫЎөДКВПоЎЈИз№ыУӨ¶щОӘДёИйО№СшЈ¬ЗТіЦРшУҰУГҝ№ІЎ¶ҫТ©ОпЈ¬ЗлФЪҙЛҙҰМоРҙКЗ·сИФФЪУГТ©ЎўТ©ОпВ©·юЗйҝцј°НЈТ©КұјдЎЈ
ұЁёжИЛј°ұЁёжөҘО»РЕПў
ұЁёжөҘО»ЈЁёЗХВЈ©ЈәЗлМоРҙұЁёжөҘО»өДГыіЖЈ¬ІўёЗХВЎЈ
ұЁёжТҪЙъЈәЗлМоРҙұЁёжТҪЙъөДРХГыЎЈ
БӘПөөз»°ЈәЗлМоРҙМоұЁөҘО»БӘПөөз»°ЎЈ
МоұЁИХЖЪЈәЦёМоРҙұҫөЗјЗҝЁөДИХЖЪЎЈ
ОеЎўГ·¶ҫёРИҫФРІъёҫөЗјЗҝЁМоҝЁЛөГч
ЈЁТ»Ј©ұҫөЗјЗҝЁЦРЈ¬ОҙұкГчЎ°·ЗұШМоЎұөДПоДҝҫщОӘұШРлМоРҙПоЈЁМшЧӘПоДҝіэНвЈ©ЎЈ
ЈЁ¶юЈ©ұҫөЗјЗҝЁЦРЈ¬ОҙұкГчЎ°¶аСЎЎұөДСЎФсМвЈ¬Т»ВЙОӘЎ°өҘСЎЎұЎЈ
ЈЁИэЈ©ұҫөЗјЗҝЁЦРЛщУРөДИХЖЪҫщОӘ№«АъИХЖЪЈ¬Дк·Э4О»ЎўФВ·Э2О»ЎўИХЖЪ2О»ЎЈИфФВ·Э»тИХЖЪІ»Чг2О»КұЈ¬ФтФВ·Э»тИХЖЪөДөЪ1О»МоЎ°0ЎұЎЈФВ·ЭЎўИХЖЪҫщІ»ПкКұЈ¬МоРҙЎ°07ЎұФВЎ°01ЎұИХЈ»ТСЦӘДк·ЭЎўФВ·ЭЈ¬ҪцИХЖЪІ»ПкКұЈ¬МоРҙЎ°15ЎұИХЎЈ
ЈЁЛДЈ©ұа әЕЈә
өЪТ»Іҝ·ЦЈ¬6О»Ј¬РРХюЗш»®ҙъВлЈ¬°ҙ№ъјТНіјЖҫЦ№«ІјұкЧјЦҙРРЈ»
өЪ¶юІҝ·ЦЈ¬3О»Ј¬ТҪФәЦъІъ»ъ№№ұаВлЈ¬УЙөұөШОАЙъҫЦНіТ»ұаЦЖЈ»
өЪИэІҝ·ЦЈ¬4О»Ј¬МоұЁДк¶ИұаВлЈ¬МоРҙМоұЁЛщКфДк·ЭЈ»
өЪЛДІҝ·ЦЈ¬3О»Ј¬ёцИЛЛіРтұаВлЈ¬°ҙГҝёцТҪБЖЦъІъ»ъ№№МоұЁЛіРтТАҙОұаВлЎЈ
ГҝёцФРІъёҫөДГҝТ»ҙОИСЙпРл¶ФУҰТ»ёцОЁТ»өДұаәЕЎЈ
ЈЁОеЈ©КЎЈЁЧФЦОЗшЎўКРЈ©ЎўПШЎўТҪФәЈЁёҫУЧұЈҪЎФәЈ©ЈәЗлҫЭКөМоРҙЈ¬ЧўТвУлұаВлөЪТ»Ўў¶юЎўИэІҝ·ЦДЪИЭТ»ЦВЎЈ
ұн4ЁCўс Г·¶ҫёРИҫФРІъёҫөЗјЗҝЁ
Т»Ўў»щұҫЗйҝц
РХ ГыЈәЗлМоРҙГ·¶ҫёРИҫФРІъёҫөДРХГыЈ¬УлЙн·ЭЦӨЈЁ»т»§ҝЪұҫЎўҫь№ЩЦӨөИУРР§ЦӨјюЈ©ЙПөДРХГыТ»ЦВЎЈ
Йн·ЭЦӨәЕЈәұШРлМоРҙЈ¬јИҝЙМоРҙ18О»Йн·ЭЦӨәЕВлЈ¬ТІҝЙМоРҙ15О»Йн·ЭЦӨәЕВлЎЈИз№ыИ·КөОЮ·Ё»сөГЙн·ЭЦӨәЕЈ¬ФтЈә
З°6О»МоРҙМоұЁПШЈЁКРЎўЗшЈ©өДРРХюЗш»®ҙъВлЈ»
өЪ7-10О»МоРҙіцЙъДк·ЭЈ»
өЪ11-12О»МоРҙіцЙъФВ·ЭЈ»
өЪ13-14О»МоРҙіцЙъИХЖЪЈ»
өЪ15-18О»МоРҙЈәЧФ9999ҝӘКјТАҙОДжРтұаРҙЈ¬Из9999Ј¬9998Ј¬9997өИЎЈ
іцЙъИХЖЪЈәЗлМоРҙ№«АъіцЙъөДДкФВИХЎЈИзИ·КөОЮ·Ё»сөГЈ¬ЗлМоРҙЦЬЛкЎЈ
Гс ЧеЈәЗлФЪПаУҰГсЧеЗ°»®Ў°ЎМЎұЎЈИзСЎФсЖдЛыЈ¬ЗлПкПёЛөГчЎЈ
ОД»ҜіМ¶ИЈәЗлФЪПаУҰОД»ҜіМ¶ИЗ°»®Ў°ЎМЎұЎЈОД»ҜіМ¶ИКЗЦёФРІъёҫ/ёҫЕ®ҪУКЬ№ъДЪНвҪМУэЛщИЎөГөДЧоёЯС§Аъ»тУлПЦУРОД»ҜЛ®ЖҪПаөұөДС§АъЎЈОДГӨ/°лОДГӨЈәЦёІ»К¶ЧЦ»тК¶ЧЦІ»Чг1500ёцЈ¬І»ДЬФД¶БНЁЛЧКйұЁЈ¬І»ДЬРҙұгМхөДИЛЈ»РЎС§ЈәЦёҪУКЬЧоёЯТ»ј¶ҪМУэОӘРЎС§іМ¶ИөДұПТөЎўТЮТөЙъЈ¬ТІ°ьАЁГ»УРЙП№эРЎС§Ј¬ө«К¶ЧЦі¬№э1500ёцЈ¬ДЬФД¶БНЁЛЧКйұЁЈ¬ДЬРҙұгМхЈ¬ҙпөҪЙЁГӨұкЧјөДИЛЈ»іхЦРЈәЦёҪУКЬЧоёЯТ»ј¶ҪМУэОӘіхЦРіМ¶ИөДұПТөЎўТЮТөј°ФЪРЈЙъЈ¬јј№ӨѧУЈ¬ПаөұУЪіхЦРөДЈ¬МоРҙЎ°іхЦРЎұЈ»ёЯЦРЈәЦёҪУКЬЧоёЯТ»ј¶ҪМУэОӘЖХНЁёЯЦРЎўЦ°ТөёЯЦРј°ЦРЧЁіМ¶ИөДұПТөЎўТЮТөј°ФЪРЈЙъЈ¬јј№ӨѧУЈ¬ПаөұУЪёЯЦРөДЈ¬МоРҙЎ°ёЯЦРЎұЈ»ҙуЧЁ»тҙуС§ЈәЦёҪУКЬЧоёЯТ»ј¶ҪМУэОӘҙуС§ЧЁҝЖ»тұҫҝЖөДұПТөЎўТЮТөј°ФЪРЈЙъЈ¬НЁ№эЧФС§ҫӯ№э№ъјТНіТ»ҫЩ°мөДЧФС§ҝјКФИЎөГҙуС§ЧЁҝЖ»тұҫҝЖЦӨКйөДЈ¬ТІМоРҙЎ°ҙуЧЁ»тҙуС§ЎұЈ»Л¶Кҝј°ТФЙПЈәЦёҪУКЬЧоёЯТ»ј¶ҪМУэОӘЛ¶КҝСРҫҝЙъј°ТФЙПөДұПТөј°ФЪРЈЙъЎЈ
Ц° ТөЈәЗлФЪПаУҰЦ°ТөЗ°»®Ў°ЎМЎұЎЈ
»йТцЧҙҝцЈәЗлМоРҙұҫҙОҪУКЬФӨ·АГ·¶ҫДёУӨҙ«ІҘ·юОсКұөД»йТцЧҙҝцЎЈОҙ»йЦёҙУОҙҪб№э»йЎЈіх»йЦёөЪТ»ҙОҪб»йЈ»ФЩ»йЦёАл»й»тЙҘЕјәуФЩҙОҪб»йЎЈН¬ҫУЦёОҙ°мАн№ъјТ·ЁВЙ»йТцөЗјЗКЦРшЈ¬ө«Н¬ҫУ№ІН¬Йъ»оЎЈАл»йЦёТтёчЦЦФӯТтЈ¬·тЖЮЛ«·ҪТСҪвіэ»йТц№ШПөХЯІўЗТОҙФЩ»йЎЈЙҘЕјЦёЕдЕјИҘКАОҙФЩ»йЎЈ
ФРІъЗйҝцЈәФРҙОЈәМоРҙЛщУРөДИСЙпҙОКэЈЁә¬ұҫҙОЈ©Ј»ІъҙОЈ¬МоРҙјИНщВъ28ЦЬәуИСЙпЦХЦ№өДҙОКэЈ¬І»ҝјВЗИСЙпЦХЦ№·ҪКҪј°ИСЙпҪбҫЦЈЁІ»ә¬ұҫҙОЈ©ЎЈ
јИНщІ»БјИСЙпҪбҫЦЈәМоРҙФРІъёҫјИНщҫӯАъөДІ»БјИСЙпҪбҫЦҙОЈЁМҘЈ©КэЈ¬°ьАЁЧФИ»БчІъЎўЛАМҘЎўЛАІъЎўФзІъәНіцЙъИұПЭөИЈ¬ИзУРЖдЛыЗйҝцЈ¬ЗлЧўГчЎЈ
ұҫҙОИСЙпД©ҙОФВҫӯКұјдЈәЗлМоРҙ№«АъИХЖЪЎЈД©ҙОФВҫӯКұјдЦёЧоәуТ»ҙОФВҫӯАҙіұөДөЪТ»МмЎЈ
ФӨ Іъ ЖЪЈәЗлёщҫЭұҫҙОИСЙпД©ҙОФВҫӯКұјдјЖЛгІўМоРҙФӨІъЖЪЎЈФӨІъЖЪјЖЛ㹫КҪЈәД©ҙОФВҫӯөЪТ»МмөДФВ·ЭКэјх3ЈЁ»тФВ·ЭКэЎЬ3КұјУ9Ј©Ј¬ИХЖЪКэјУ7јҙОӘФӨІъЖЪөДИХЖЪЎЈУҰУГ№«АъИХЖЪјЖЛгЎЈ
іхјмФРЦЬЈәЗлМоРҙФРІъёҫөЪТ»ҙОҪУКЬФРІъЖЪұЈҪЎөДКұјдЎЈФРЦЬЧФұҫҙОИСЙпД©ҙОФВҫӯКұјдҝӘКјјЖЛгЎЈ
ПЦ ЧЎ Ц·ЈәЗлПкПёМоРҙФРІъёҫПЦҫУЧЎөШЦ·Ј¬ҫЯМеөҪГЕЕЖәЕЈ¬іЗХтөШЦ·өДЎ°РЎЗшЎұөИН¬УЪЎ°ҙеЎұЎЈ
»§ҝЪЛщФЪөШЈәЗлПкПёМоРҙФРІъёҫөД»§ҝЪЛщФЪөШЦ·Ј¬ҫЯМеөҪГЕЕЖәЕЈ¬іЗХтөШЦ·өДЎ°РЎЗшЎұөИН¬УЪЎ°ҙеЎұЎЈ
№ӨЧчөҘО»ЈәЗлМоРҙФРІъёҫөД№ӨЧчөҘО»ГыіЖЈ¬Из№ыГ»УР№ӨЧчөҘО»Ј¬ЗлМоРҙЎ°ОЮЎұЎЈ
БӘПөөз»°ЈәЗлМоРҙФРІъёҫөДБӘПө·ҪКҪЎЈ
¶юЎўГ·¶ҫёРИҫПа№ШЗйҝц
јИНщКЗ·сХп¶ПОӘГ·¶ҫёРИҫЈәЎ°јИНщЎұКЗЦёФРІъёҫФЪұҫҙОИСЙпөДД©ҙОФВҫӯЗ°И·ИПёРИҫЈ¬ИзХп¶ПОӘГ·¶ҫёРИҫЈ¬ФтМоРҙҫЯМеөДХп¶ПКұјдЈ¬ИфөГІ»өҪХп¶ПКұјдЈ¬ЗлСЎФсЎ°І»ПкЎұЎЈ
ұҫҙОХп¶ПГ·¶ҫёРИҫКұЖЪЈә·ЦОӘФРЖЪЎўІъКұЎўІъәу»тЖдЛыЈ¬ИзФЪФРЖЪХп¶ПёРИҫЈ¬ЗлМоРҙҫЯМеФРЦЬЎЈ
ұҫҙОХп¶ПГ·¶ҫёРИҫКұјдЈәҫЎҝЙДЬМоРҙФРІъёҫұ»И·ХпёРИҫГ·¶ҫөДҫЯМеКұјдЎЈФВ·ЭІ»ПкКұЈ¬МоРҙЎ°07ЎұФВЎЈИХЖЪІ»ПкКұЈ¬МоРҙЎ°15ЎұИХЎЈ
ұҫҙОГ·¶ҫХп¶П·ЦЖЪЈә·ЦОӘТюРФГ·¶ҫЎўТ»ЖЪГ·¶ҫЎў¶юЖЪГ·¶ҫЎўИэЖЪГ·¶ҫ»тІ»ПкЎЈ
ЧоҝЙДЬөДГ·¶ҫёРИҫНҫҫ¶ЈәёщҫЭГ·¶ҫёРИҫФРІъёҫөДёЯОЈРРОӘәНОЈПХТтЛШЕР¶ПЖдҝЙДЬРФЧоҙуөДёРИҫНҫҫ¶ЎЈИфСЎФсЖдЛыЈ¬ЗлҫЯМеЛөГчЎЈ
РФ ҙ« ІҘЈәЦёНЁ№эУлТмРФЦ®јдөДРФҪУҙҘҙ«ІҘЎЈ
СӘТәҙ«ІҘЈәЦёКдКЬ№эИ«СӘ/іЙ·ЭСӘ/СӘҪ¬/СӘЦЖЖ·өИЎЈ
ДёУӨҙ«ІҘЈәЦёГ·¶ҫёРИҫФРІъёҫНЁ№эИСЙпЎў·ЦГдөИ№эіМК№ЖдЛщЙъ¶щНҜұ»ёРИҫЎЈ
І» ПкЈәЦёёРИҫНҫҫ¶ОЮ·ЁЕР¶ПЎЈ
Жд ЛыЈәЙПКцОҙБРҫЩЈ¬ө«ҝЙДЬФміЙГ·¶ҫҙ«ІҘөДҪУҙҘК·ЎЈИзФЪҙЛСЎПоЗ°»®Ў°ЎМЎұЈ¬УҰФЪәуГжҝХ°ЧҙҰҪшРРЛөГчЎЈ
ХЙ·т/РФ°йДҝЗ°өДГ·¶ҫёРИҫЧҙМ¬ЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈСЎФсОҙјмІвЎўОҙёРИҫЎўјмІвҪб№ыІ»ПкЈ¬»тКЗ·сјмІвІ»ПкХЯМшөҪЎ°ИэЎўФРІъёҫұҫҙОИСЙпГ·¶ҫКөСйКТХп¶ПТАҫЭЎұҙҰЎЈ
ХЙ·т/РФ°йөДГ·¶ҫХп¶ПКұјдЈәҫЎҝЙДЬМоРҙЖдИ·ХпёРИҫКұјдЈ¬ҫЯМеЛөГчН¬З°ЎЈ
ИэЎўФРІъёҫұҫҙОИСЙпГ·¶ҫХп¶ПјмІвЗйҝц
·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСй·Ҫ·Ёј°КұјдЈәЗлёщҫЭұҫҙОҪУКЬ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСй¶ЁБҝјмІвөДҪб№ыұЁёжөҘЈ¬ФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈКФСй·Ҫ·Ё°ьАЁЈәҝмЛЩСӘҪ¬·ҙУҰЛШ»·ЧҙҝЁЖ¬КФСйЈЁјтіЖRPRЈ©ЎўјЧұҪ°·әмІ»јУИИСӘЗеКФСйЈЁјтіЖTRUSTЈ©Ўў»тЖдЛыјмІв·Ҫ·ЁЎЈН¬КұМоРҙЛщСЎјмІв·Ҫ·ЁөДөО¶ИҪб№ыәНПаУҰөДјмІвКұјдЎЈ
Г·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйКөСй·Ҫ·Ёј°КұјдЈәЗлёщҫЭұҫҙОҪУКЬГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйөДјмІвЗйҝцЈ¬ФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈјмІв·Ҫ·Ё°ьАЁЈәГ·¶ҫВЭРэМеҝЕБЈДэјҜКФСйЈЁјтіЖTPPAЈ©ЎўГёБӘГвТЯОьёҪКФСйЈЁјтіЖELISAЈ©ЎўГвТЯІгОц·Ё-ҝмЛЩјмІвЈЁRTЈ©»тЖдЛыјмІв·Ҫ·ЁЈ¬Н¬КұМоРҙЛщСЎјмІв·Ҫ·ЁөДјмІвКұјдЎЈ
Г·¶ҫВЭРэМеIgMҝ№МејмІвЈәЗлФЪПаУҰөДСЎПоЗ°»®Ў°ЎМЎұЈ¬ІўМоРҙјмІвКұјдЎЈ
°өКУТ°ПФОўҫөГ·¶ҫВЭРэМејмІвЈәЗлФЪПаУҰөДСЎПоЗ°»®Ў°ЎМЎұЈ¬ІўМоРҙјмІвКұјдЎЈ
ұЁёжИЛј°ұЁёжөҘО»РЕПў
ұЁёжөҘО»ЈЁёЗХВЈ©ЈәЗлМоРҙұЁёжөҘО»өДГыіЖЈ¬ІўёЗХВЎЈ
ұЁёжТҪЙъЈәЗлМоРҙұЁёжТҪЙъөДРХГыЎЈ
БӘПөөз»°ЈәЗлМоРҙМоұЁөҘО»БӘПөөз»°ЎЈ
МоұЁИХЖЪЈәЦёМоРҙұҫөЗјЗҝЁөДИХЖЪЎЈ
ұё ЧўЈәҝЙМоРҙТ»Р©ОДЧЦРЕПўЈ¬ТФІ№ідөЗјЗҝЁЦРОҙҫЎөДКВПоЎЈ
ұн4ЁCўтЎўГ·¶ҫёРИҫФРІъёҫј°ЛщЙъРВЙъ¶щөЗјЗҝЁ
ФРІъёҫұаәЕЈәЗлМоРҙГ·¶ҫёРИҫФРІъёҫ/¶щНҜДёЗЧөДұаәЕЈ¬ЧўТвУлұн4ЁCўсГ·¶ҫёРИҫФРІъёҫөЗјЗҝЁөДұаәЕТ»ЦВЎЈ
¶щНҜұаәЕЈәЗ°4¶ОұаәЕЈЁјҙұаәЕөДЗ°16О»Ј©УлГ·¶ҫёРИҫФРІъёҫ/ДёЗЧұаәЕТ»ЦВЎЈЧоәу1О»°ҙұҫҙО·ЦГдУӨ¶щіцЙъөДҙОРтМоРҙЈәИфОӘөҘМҘЈ¬МоЎ°1ЎұЈ»ИфОӘ¶аМҘЈ¬ФтөЪТ»МҘУӨ¶щМоЎ°1ЎұЎўөЪ¶юМҘУӨ¶щМоЎ°2ЎұЈ¬ТФҙЛАаНЖЎЈГ·¶ҫёРИҫФРІъёҫЛщЙъ¶щНҜЈ¬Гҝёц¶щНҜ·ЦұрМоұЁТ»ХЕұҫөЗјЗҝЁЎЈ
ФРІъёҫРХГыЈәЗлМоРҙГ·¶ҫёРИҫФРІъёҫ/ДёЗЧөДРХГыЈ¬Улұн4ЁCўсГ·¶ҫёРИҫФРІъёҫөЗјЗҝЁөДРХГыТ»ЦВЎЈ
Йн·ЭЦӨәЕЈәЗлМоРҙГ·¶ҫёРИҫФРІъёҫ/ДёЗЧөДЙн·ЭЦӨәЕЈ¬Улұн4ЁCўсГ·¶ҫёРИҫФРІъёҫЙн·ЭЦӨәЕТ»ЦВЎЈ
БӘПөөз»°ЈәЗлМоРҙДЬБӘПөөҪГ·¶ҫёРИҫФРІъёҫөДөз»°ЎЈ
ПЦ ЧЎ Ц·ЈәМоРҙ·Ҫ·ЁН¬З°ЛщКцЎЈ
Т»ЎўФРІъёҫұҫҙОИСЙпј°·ЦГдЗйҝц
ИСЙпҪбҫЦЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈ·ЦГдЦёИСЙпВъ28ЦЬЈЁ196ИХЈ©ј°ТФәуЈ¬МҘ¶щј°ЖдёҪКфОпҙУДёМеГдіцЎЈЧФИ»БчІъЦёЈ¬ИСЙпІ»Чг28ЦЬЎўМҘ¶щМеЦШІ»Чг1000ҝЛЈ¬ОЮИЛОӘТтЛШЗйҝцПВЈ¬ИСЙпЦХЦ№ЎЈИЛ№ӨЦХЦ№ИСЙпЦёЈ¬ИСЙпІ»Чг28ЦЬЎўМҘ¶щМеЦШІ»Чг1000ҝЛЈ¬ИЛОӘёЙФӨөДИСЙпЦХЦ№ЎЈИзСЎФсЧФИ»БчІъ»тИЛ№ӨЦХЦ№ИСЙпЈ¬ЗлМоРҙПаУҰөДФРЦЬЈ¬ИзСЎФсЖдЛыИСЙпҪбҫЦЈ¬ЗлПкПёЛөГчЎЈ
КЗ·сК§·ГЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈК§·ГКұЖЪЗлМоРҙЧоәуТ»ҙОЛж·ГКұөДФРЦЬ»тІъәуЦЬКэЎЈ
ИСЙпҪбҫЦОӘЎ°ЧФИ»БчІъЎұЎўЎ°ИЛ№ӨЦХЦ№ИСЙпЎұ»тЎ°ЖдЛыЎұХЯЈ¬І»ұШМоРҙұҫөЗјЗҝЁөДЖдУаІҝ·ЦЈ¬МоРҙНкЎ°КЗ·сК§·ГЎұәуЈ¬МшЦБЎ°ұЁёжөҘО»ЎұҙҰЈ¬ІўҪб°ёЎЈ
ФРІъЖЪТміЈЗйҝцЈә°ьАЁМҘДӨФзЖЖЎўІъәуіцСӘЎўәПІўТТёОёРИҫЎўәПІўHIVёРИҫ»тЖдЛыЗйҝцЎЈ
ұҫҙОИСЙпД©ҙОФВҫӯКұјдЈәЗлМоРҙ№«АъИХЖЪЎЈД©ҙОФВҫӯКұјдЦёЧоәуТ»ҙОФВҫӯАҙіұөДөЪТ»МмЎЈ
·ЦГдИХЖЪЈәЦёМҘ¶щГдіцөДИХЖЪЎЈ
·ЦГдФРЦЬЈәЦёМҘ¶щГдіцКұФРІъёҫЛщҙҰөДФРЦЬЎЈ
·ЦГд·ҪКҪЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈЧФИ»·ЦГдЦёМҘ¶щҫӯТхөАЧФИ»ГдіцөД·ЦГд·ҪКҪЈ»ТхөАЦъІъЦёФЪөЪ¶юІъіМ№¬ҝЪҝӘИ«ә󣬶Բ»ДЬҙУТхөАЧФИ»ГдіцөДІъёҫЈ¬ФЛУГЖчРөРӯЦъІъёҫҪ«МҘ¶щГдіцөД·ЦГд·ҪКҪЈ»ФсЖЪЖК№¬ІъЦёБЩІъЗ°өДЖК№¬ІъЈ»јұХпЖК№¬ІъЦёБЩІъТФәуөДЖК№¬ІъЎЈ
·ЦГдМҘКэЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЈ¬ИфСЎФсЖдЛыЈ¬ЗлПкПёЛөГчЎЈ
ФРІъёҫҪбҫЦЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈЛАНцФӯТтЗл°ҙХХЎ°ҫУГсЛАНцТҪС§ЦӨГчКйЎұТӘЗуМоРҙЦұҪУЦВЛАјІІЎГыіЖЎЈ
О§Іъ¶щЧӘ№йЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈ»оІъЦёЈ¬ИСЙп28ЦЬәуЈ¬МҘ¶щНСАлДёМеКұЈ¬УР№эЛДЦЦЙъГьПЦПуЈЁ°ьАЁәфОьЎўРДМшЎўЛжТвјЎКХЛхәНЖкҙшІ«¶ҜЈ©Ц®Т»ХЯЈ»ЛАМҘЦёЈ¬ИСЙп28ЦЬәуМҘ¶щФЪЧУ№¬ДЪЛАНцЈ»ЛАІъЦёЈ¬МҘ¶щФЪГдіц№эіМЦРЛАНцЈ»РВЙъ¶щЖЯМмДЪЛАНцЈЁјҙФзЖЪРВЙъ¶щЛАНцЈ©ЦёЈ¬»оІъ¶щФЪіцЙъәуОҙВъ7МмЛАНцЎЈИф·ўЙъЖЯМмДЪЛАНцЈ¬ФтОЮРиФЪЎ°»оІъЎұСЎПоЗ°»®Ў°ЎМЎұЎЈ
О§Іъ¶щТміЈЗйҝцЈЁ¶аСЎЈ©ЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈјІІЎРиҫӯ№эПзј¶ЈЁә¬Ј©ТФЙПТҪБЖОАЙъ»ъ№№Хп¶ПЈ¬°ьАЁФзІъ»төНіцЙъМеЦШЎўРВЙъ¶щ·ОСЧЈЁ°ьАЁУЪ№¬ДЪЎў·ЦГд№эіМЦРёРИҫөДОьИлРФ·ОСЧЈ¬ТФј°УЪіцЙъәу7МмДЪёРИҫөДРВЙъ¶щФз·ўРН·ОСЧЈ©ЎўРВЙъ¶щЦППўЎўіцЙъИұПЭЎЈИфСЎФсіцЙъИұПЭЈ¬ЗлМоРҙҫЯМеИұПЭАаРНЈ¬ИфСЎФсЖдЛыЈ¬ЗлПкПёЛөГчЎЈ
¶юЎўФРІъёҫГ·¶ҫТ©ОпУҰУГЗйҝц
ЗлёщҫЭФРІъёҫУҰУГЦОБЖГ·¶ҫТ©ОпөДЗйҝцЈ¬ФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИфЎ°ОҙУГТ©ЎұЈ¬МшЦБЎ°ИэЎўФРІъёҫ·ЦГдЗ°»тФРНнЖЪ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвЎұҙҰЎЈ
УГТ©ПкПёРЕПўЈә
өЪТ»ёцБЖіМЈәМоРҙөЪТ»ёцБЖіМҝӘКјУГТ©өДКұјдЈЁҫЯМеөДДкФВИХЈ©Ј¬ФЪПаУҰөДТ©ОпГыіЖЗ°»®Ў°ЎМЎұЈ¬МоРҙГҝИХУГБҝЎўТФј°ұҫБЖіМҪбКшКұјдЈЁҫЯМеөДДкФВИХЈ©ЎЈ
өЪ¶юёцБЖіМЈәМоРҙ·Ҫ·ЁН¬өЪТ»ёцБЖіМөДМоРҙ·Ҫ·ЁЎЈ
өЪИэёцБЖіМЈәМоРҙ·Ҫ·ЁН¬З°ЛщКцЎЈ
НЁ№эЙПКцУГТ©ПкПёРЕПўөДөЗјЗЈ¬ҝЙјЖЛгКЧёцБЖіМУлЧоәуТ»ёцБЖіМөДјдёфЎўЦОБЖТ©ОпЦЦАаәНУГТ©КұЖЪ·ЦІјөИЦёұкЈ¬ҙУ¶шҪшТ»ІҪЕР¶ПФРІъёҫКЗ·сҪУКЬБЛ№ж·¶ЦОБЖЎЈ
ИэЎўФРІъёҫ·ЦГдЗ°»тФРНнЖЪ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІв
ФРІъёҫ·ЦГдЗ°»тФРНнЖЪ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвЈәМоРҙГ·¶ҫёРИҫФРІъёҫФЪ·ЦГдЗ°»тФРНнЖЪҪУКЬ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвөДЗйҝцЈ¬ЗлФЪПаУҰөДјмІв·Ҫ·ЁЗ°»®Ў°ЎМЎұЎЈН¬КұМоРҙЛщСЎјмІв·Ҫ·ЁөД¶ЁРФҪб№ыЎўөО¶ИҪб№ыј°јмІвКұјдЈ¬ҫЯМеЛөГчН¬З°ЎЈ
ЛДЎўГ·¶ҫёРИҫФРІъёҫЛщЙъРВЙъ¶щЗйҝц
РХ ГыЈәЗлМоРҙ¶щНҜөДРХГыЈ¬УҰУлЎ°іцЙъТҪС§ЦӨГчЎұөДРХГыТ»ЦВЎЈИз№ыЙРОҙИЎГыЈ¬ЗлГиКцОӘЎ°ёРИҫФРІъёҫРХГы+Ц®ЧУ/Е®ЎұЎЈ
РФ ұрЈәЗлФЪПаУҰРФұрЗ°»®Ў°ЎМЎұЎЈИз№ыБҪРФ»ыРОЈ¬СЎФсПФРФөДДЗёцРФұрЎЈ
іцЙъМеЦШЈәЗлМоРҙПаУҰКэЦөЈ¬іцЙъМеЦШЦёУӨ¶щіцЙъ1РЎКұДЪөДМеЦШЈ¬өҘО»ОӘЎ°ҝЛЎұЎЈ
іцЙъЙніӨЈәЗлМоРҙУӨ¶щіцЙъ1РЎКұДЪөДЙніӨАеГЧКэЦөЎЈ
ҙж»оЗйҝцЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИзГ·¶ҫёРИҫІъёҫЛщЙъ¶щНҜТСЛАНцЈ¬ЗлМоРҙЛАНцФӯТтј°ЛАНцКұјдЈ¬ТӘЗуМоРҙҫЯМеөДДкЎўФВЎўИХЎЈ
ЛщЙъУӨ¶щіцЙъәуөДГ·¶ҫјмІв·Ҫ·ЁЈә°ьАЁ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвЎўГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвЎўГ·¶ҫВЭРэМеIgMҝ№МејмІвәН°өКУТ°ПФОўҫөГ·¶ҫВЭРэМејмІвЈә
·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвЈәМоРҙГ·¶ҫёРИҫІъёҫЛщЙъУӨ¶щіцЙъәуҪУКЬ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйөДЗйҝцЈ¬ЗлФЪПаУҰөДјмІв·Ҫ·ЁЗ°»®Ў°ЎМЎұЎЈН¬КұМоРҙЛщСЎјмІв·Ҫ·ЁөДөО¶ИҪб№ыј°јмІвКұјдЈ¬ҫЯМеЛөГчН¬З°ЎЈ
Г·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвЈәМоРҙГ·¶ҫёРИҫІъёҫЛщЙъУӨ¶щіцЙъәуҪУКЬГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйөДЗйҝцЈ¬ЗлФЪПаУҰөДјмІв·Ҫ·ЁЗ°»®Ў°ЎМЎұЎЈН¬КұМоРҙЛщСЎјмІв·Ҫ·ЁөДөО¶ИҪб№ыј°јмІвКұјдЈ¬ҫЯМеЛөГчН¬З°ЎЈ
Г·¶ҫВЭРэМеIgMҝ№МејмІвЈәЗлФЪПаУҰөДСЎПоЗ°»®Ў°ЎМЎұЈ¬ІўМоРҙјмІвКұјдЎЈ
°өКУТ°ПФОўҫөГ·¶ҫВЭРэМејмІвЈәЗлФЪПаУҰөДСЎПоЗ°»®Ў°ЎМЎұЈ¬ІўМоРҙјмІвКұјдЎЈ
Па№ШЦўЧҙЈЁ¶аСЎЈ©ЈәЗлёщҫЭ¶щНҜјТКфЦчЛЯј°ІйМеЛщјыЈ¬ФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИфСЎФсЖдЛыЈ¬ЗлҫЯМеЛөГчЎЈ
КЗ·сҪУКЬҪшРРФӨ·АРФЦОБЖЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈ¶щНҜФӨ·АРФЦОБЖЦёХчЈәФРЖЪОҙҪУКЬ№ж·¶РФЦОБЖЈ¬°ьАЁФРЖЪОҙҪУКЬИ«іМЎўЧгБҝөДЗаГ№ЛШЦОБЖЈ¬»тҪУКЬ·ЗЗаГ№ЛШ·Ҫ°ёЦОБЖЈ¬»тФЪ·ЦГдЗ°1ёцФВДЪІЕҪшРРҝ№Г·¶ҫЦОБЖөДФРІъёҫЛщЙъ¶щНҜЈ»ФРЖЪҪУКЬ№э№ж·¶РФЦОБЖЈ¬іцЙъКұ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйСфРФЎўөО¶ИІ»ёЯУЪДёЗЧ·ЦГдЗ°өО¶ИөД4ұ¶өД¶щНҜЎЈИфОҙҪУКЬФӨ·АРФЦОБЖЈ¬ФтМшЦБЎ°ОеЎў¶щНҜГ·¶ҫёРИҫХп¶ПЗйҝцЎұЎЈИфҪУКЬБЛФӨ·АРФЦОБЖЈ¬ФтМоРҙПкПёөДФӨ·АРФЦОБЖТ©ОпГыіЖЎўУГТ©јББҝЎўФӨ·АРФЦОБЖҝӘКјКұјдЎўТФј°ҫаАл·ЦГдөДКұјдөИЈ¬ИзҫаАл·ЦГдКұјдөДМмКэОӘёцО»КэЈ¬ФтФЪМмКэЗ°ГжөДөЪТ»ёцҝХёсДЪМоРҙЎ°0ЎұЈ¬АэИзЎ°07МмЎұЈ¬Ифҫа·ЦГдКұјдөДҫЯМеЎ°·ЦЎұІ»ПкЈ¬ФтМоРҙЎ°00ЎұЎЈ
РВЙъ¶щГ·¶ҫёРИҫЗйҝц: ЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИзЎ°Хп¶ППИМмГ·¶ҫЎұЈ¬ФтјМРш»ШҙрЎ°БщЎўРВЙъ¶щХп¶ПОӘПИМмГ·¶ҫөДТАҫЭЎұәНЎ°ЖЯЎўХп¶ПОӘПИМмГ·¶ҫөД¶щНҜКЗ·сҪУКЬЦОБЖЎұЈ¬ИфСЎФсЎ°јМРшЛж·ГҙэХп¶ПЎұФтМшЦБЎ°°ЛЎўұёЧўЎұҙҰЈ¬ёщҫЭЗйҝцІ№ідЛөГчПа№ШРЕПўЈ¬ІўМоРҙЎ°ұЁёжИЛј°ұЁёжөҘО»РЕПўЎұәуНкіЙұн4-IIЎЈ
РВЙъ¶щХп¶ПОӘПИМмГ·¶ҫөДТАҫЭЈЁҝЙ¶аСЎЈ©ЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈ
Хп¶ПОӘПИМмГ·¶ҫөДРВЙъ¶щКЗ·сҪУКЬЦОБЖЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈ
ұё ЧўЈәҝЙМоРҙТ»Р©ОДЧЦРЕПўЈ¬ТФІ№ідөЗјЗҝЁЦРОҙҫЎөДКВПоЎЈ
ұЁёжИЛј°ұЁёжөҘО»РЕПў
ұЁёжөҘО»ЈЁёЗХВЈ©ЈәЗлМоРҙұЁёжөҘО»өДГыіЖЈ¬ІўёЗХВЎЈ
ұЁёжТҪЙъЈәЗлМоРҙұЁёжТҪЙъөДРХГыЎЈ
БӘПөөз»°ЈәЗлМоРҙМоұЁөҘО»БӘПөөз»°ЎЈ
МоұЁИХЖЪЈәЦёМоРҙұҫҪб°ёөЗјЗҝЁөДИХЖЪЎЈ
ұн4ЁCIIIЎўГ·¶ҫёРИҫІъёҫЛщЙъ¶щНҜЛж·ГөЗјЗҝЁ
ТӘЗуФЪ¶щНҜВъ3Ўў6Ўў9Ўў12Ўў15әН18ёцФВКұОӘГ·¶ҫёРИҫІъёҫЛщЙъ¶щНҜМṩЛж·Г·юОсЈ¬ГҝҙОЛж·ГМоРҙТ»ХЕұҫҝЁЈ¬Иф¶щНҜФЪДіҙОЛж·Г№эіМЦРұ»Хп¶ПОӘПИМмГ·¶ҫёРИҫ»тТСГчИ·ЕЕіэёРИҫЈ¬ФтМоұЁНкіЙН¬ЖЪ¶ФУҰөДЛж·ГөЗјЗҝЁәуҪб°ёЎЈ
ФРІъёҫұаәЕЈәЗлМоРҙГ·¶ҫёРИҫФРІъёҫөДұаәЕЈ¬ЧўТвУлұн4ЁCўсЎўIIГ·¶ҫёРИҫФРІъёҫөЗјЗҝЁөДұаәЕТ»ЦВЎЈ
¶щНҜұаәЕЈәЗ°4¶ОұаәЕЈЁјҙұаәЕөДЗ°16О»Ј©УлГ·¶ҫёРИҫФРІъёҫұаәЕТ»ЦВЎЈЧоәу1О»°ҙұҫҙО·ЦГдУӨ¶щіцЙъөДҙОРтМоРҙЈәИфОӘөҘМҘЈ¬МоЎ°1ЎұЈ»ИфОӘ¶аМҘЈ¬ФтөЪТ»МҘУӨ¶щМоЎ°1ЎұЎўөЪ¶юМҘУӨ¶щМоЎ°2ЎұЈ¬ТФҙЛАаНЖЎЈГ·¶ҫёРИҫФРІъёҫЛщЙъ¶щНҜЈ¬Гҝёц¶щНҜ·ЦұрМоұЁТ»ХЕұҫөЗјЗҝЁЎЈЧўТвУлұн4ЁCўтұЈіЦТ»ЦВЎЈ
ФРІъёҫРХГыЈәЗлМоРҙГ·¶ҫёРИҫФРІъёҫөДРХГыЈ¬Улұн4ЁCўсЎўIIГ·¶ҫёРИҫФРІъёҫөЗјЗҝЁөДРХГыТ»ЦВЎЈ
Йн·ЭЦӨәЕЈәЗлМоРҙГ·¶ҫёРИҫФРІъёҫөДЙн·ЭЦӨәЕЈ¬Улұн4ЁCўсЎўIIГ·¶ҫёРИҫФРІъёҫЙн·ЭЦӨәЕТ»ЦВЎЈ
ПЦ ЧЎ Ц·ЈәМоРҙ·Ҫ·ЁН¬З°ЛщКцЎЈ
¶щНҜРХГыЎўРФұрУліцЙъИХЖЪЈәУлұн4ЁCўтұЈіЦТ»ЦВ
БӘПөөз»°ЈәЗлМоРҙДЬ№»БӘПөөҪГ·¶ҫёРИҫФРІъёҫј°ЛщЙъ¶щНҜөДөз»°әЕВл
¶щНҜФВБдЈәЗлМоРҙЛж·ГКұУӨ¶щөДКөЧгФВБдЎЈ
Лж·ГИХЖЪЈәЗлМоРҙҪшРРЛж·ГөДИХЖЪЎЈ
Лж·ГИЛРХГыЈәЗлМоРҙЛж·ГИЛРХГыЎЈ
Лж·ГЗйҝцЈәМоРҙ·Ҫ·ЁН¬З°ЛщКцЎЈИзТСК§·ГЈ¬ЗлМоРҙК§·ГФӯТтЈЁ¶щНҜФЪВъ21ФВБдЗ°І»ДЬұЁёжК§·ГЈ©ЎЈ
ҙж»оЗйҝцЈәМоРҙ·Ҫ·ЁН¬З°ЛщКцЎЈ
ЙъіӨ·ўУэЈәЗл°ҙөЗјЗҝЁөҘО»МоРҙПаУҰөДКэЦөЎЈДкБдұрМеЦШЎўДкБдұрЙніӨј°ЙніӨұрМеЦШөДЖАјЫ°ҙХХКАҪзОАЙъЧйЦҜ¶щНҜЙъіӨ·ўУэұкЧјҪшРРЎЈДкБдұрМеЦШЎўДкБдұрЙніӨј°ЙніӨұрМеЦШИфөНУЪ2ёцұкЧјІоЈЁ<ЁC2sЈ©Ј¬ЖАјЫОӘПВЈ»ФЪЙПЎўПВ2ёцұкЧјІоЦ®јдЈ¬ЈЁЎЭ ЁC2s ~ < 2sЈ©Ј¬ЖАјЫОӘЦРЈ»өИУЪ»тёЯУЪ2ёцұкЧјІоЈЁЎЭ 2sЈ©Ј¬ЖАјЫОӘЙПЎЈ
О№Сш·ҪКҪЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈДёИйО№СшЦёЈ¬Ц»УГДёИйО№СшУӨ¶щЈ¬іэО¬ЙъЛШЎўОўБҝФӘЛШЦЖјБ»тТ©ОпНвЈ¬І»ёшУӨ¶щИОәОЖдЛыТәМе»т№ММеЧҙКіОпЈЁ°ьАЁЛ®Ј©Ј»ИЛ№ӨО№СшЦёЈ¬НкИ«ІЙУГЕд·ҪДМЎўКЮИй»тЖдЛыДёИйМжҙъЖ·О№ІёУӨ¶щЈ»»мәПО№СшЦёЈ¬ТФДёИйО№ІёУӨ¶щЈ¬ө«Н¬Кұ»№ТФЖдЛыТәМе»т№ММеЧҙКіОпЈЁ°ьАЁЛ®ЎўЕд·ҪДМЎўЖдЛыКЮИй»тДёИйМжҙъЖ·өИЈ©О№ІёУӨ¶щЈ»ЖдЛыЦёЛж·ГЖЪјдУӨ¶щөДО№Сш·ҪКҪ·ўЙъёДұдЎЈ
Па№ШЦўЧҙ»тјІІЎЈЁҝЙ¶аСЎЈ©ЈәЗлёщҫЭ¶щНҜјТКфЦчЛЯј°ІйМеЛщјыЈ¬ФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈјІІЎРиҫӯ№эПзј¶ЈЁә¬Ј©ТФЙПТҪБЖОАЙъ»ъ№№Хп¶ПЎЈИфСЎФсЖдЛыЈ¬ЗлҫЯМеЛөГчЎЈ
Г·¶ҫјмІв·Ҫ·ЁЈә°ьАЁ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвЎўГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвЎўГ·¶ҫВЭРэМеIgMҝ№МејмІвәН°өКУТ°ПФОўҫөГ·¶ҫВЭРэМејмІвЎЈ
·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвЈәМоРҙГ·¶ҫёРИҫІъёҫЛщЙъ¶щНҜұҫҙОЛж·ГКұҪУКЬ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйөДЗйҝцЈ¬ЗлФЪПаУҰөДјмІв·Ҫ·ЁЗ°»®Ў°ЎМЎұЎЈН¬КұМоРҙЛщСЎјмІв·Ҫ·ЁөДөО¶ИҪб№ыј°јмІвКұјдЈ¬ҫЯМеЛөГчН¬З°ЎЈ
Г·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйјмІвЈәМоРҙГ·¶ҫёРИҫІъёҫЛщЙъ¶щНҜұҫҙОЛж·ГКұҪУКЬГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйөДЗйҝцЈ¬ЗлФЪПаУҰөДјмІв·Ҫ·ЁЗ°»®Ў°ЎМЎұЎЈН¬КұМоРҙЛщСЎјмІв·Ҫ·ЁөДөО¶ИҪб№ыј°јмІвКұјдЈ¬ҫЯМеЛөГчН¬З°ЎЈ
Г·¶ҫВЭРэМеIgMҝ№МејмІвЈәЗлФЪПаУҰөДСЎПоЗ°»®Ў°ЎМЎұЈ¬ІўМоРҙјмІвКұјдЎЈ
°өКУТ°ПФОўҫөГ·¶ҫВЭРэМејмІвЈәЗлФЪПаУҰөДСЎПоЗ°»®Ў°ЎМЎұЈ¬ІўМоРҙјмІвКұјдЎЈ
¶щНҜГ·¶ҫёРИҫЧҙМ¬ЈәЗлФЪПаУҰСЎПоЗ°»®Ў°ЎМЎұЎЈИзЎ°Хп¶ППИМмГ·¶ҫЎұЈ¬ФтјМРш»ШҙрЎ°°ЛЎўҫЕЎўК®ЎұЈ¬ИфЎ°ЕЕіэГ·¶ҫёРИҫЎұФтМшЦБЎ°К®Т»ЎўұёЧўЎұҙҰЈ¬ёщҫЭЗйҝцІ№ідЛөГчПа№ШРЕПўЈ¬ІўМоРҙЎ°ұЁёжИЛј°ұЁёжөҘО»РЕПўЎұәуҪб°ёЎЈИфСЎФсЎ°јМРшЛж·ГҙэХп¶ПЎұ ФтМшЦБЎ°К®Т»ЎўұёЧўЎұҙҰЈ¬ёщҫЭЗйҝцІ№ідЛөГчПа№ШРЕПўЈ¬ІўМоРҙЎ°ұЁёжИЛј°ұЁёжөҘО»РЕПўЎұәуНкіЙұҫҪЧ¶ОЛж·ГҝЁөДМоРҙЈ¬ФЪ3ёцФВәујМРшҝӘХ№Лж·Г№ӨЧчІўұЁёжПа№ШРЕПўЎЈ
ПИМмГ·¶ҫХп¶ПТАҫЭЈЁҝЙ¶аСЎЈ©ЈәЗлПкПёФД¶БёчёцСЎПоЈ¬ёщҫЭКөјКХп¶ПТАҫЭҪшРРСЎФсЈ¬ЗлФЪПаУҰөДСЎПоЗ°»®Ў°ЎМЎұЎЈ
ПИМмГ·¶ҫХп¶ПКұјдЈәЦёГчИ·Хп¶ПОӘПИМмГ·¶ҫКұөДҫЯМеөДКұјдЎЈ
Хп¶ПОӘПИМмГ·¶ҫөД¶щНҜКЗ·сҪУКЬЦОБЖЈәЗлФЪПаУҰөДСЎПоЗ°»®Ў°ЎМЎұ
ұё ЧўЈәҝЙМоРҙТ»Р©ОДЧЦРЕПўЈ¬ТФІ№ідЛж·ГҝЁЦРОҙҫЎөДКВПоЎЈ
ұЁёжИЛј°ұЁёжөҘО»РЕПў
ұЁёжөҘО»ЈЁёЗХВЈ©ЈәЗлМоРҙұЁёжөҘО»өДГыіЖЈ¬ІўёЗХВЎЈ
ұЁёжТҪЙъЈәЗлМоРҙұЁёжТҪЙъөДРХГыЎЈ
БӘПөөз»°ЈәЗлМоРҙМоұЁөҘО»БӘПөөз»°ЎЈ
МоұЁИХЖЪЈәЦёМоРҙұҫЛж·ГҝЁөДИХЖЪЎЈ
ёҪјю8
ФӨ·А°¬ЧМІЎЎўГ·¶ҫәНТТёОДёУӨҙ«ІҘ№ӨЧч»щҙЎұнёс
ұн8-1 ФӨ·А°¬ЧМІЎ/Г·¶ҫ/ТТёОДёУӨҙ«ІҘГв·СјмІвІЙСӘөЗјЗұн
әюДПКЎ КРЎўЦЭ ПШКРЗш ТҪФә/ОАЙъФә/ҪЦөАЙзЗш
|
РтәЕ |
ІЙСӘИХЖЪ |
РХГы |
ДкБд |
ФРЦЬ |
ФРёҫұҫИЛөз»° |
»§ҝЪЛщФЪөШ |
СӘСщ АҙФҙ |
ЧЙСҜЗйҝц |
ФРёҫ»тјТКфЗ©Гы |
ЛНјм ИХЖЪ |
ЛНјм ТҪЙъ |
јмІв»ъ№№ |
·ҙАЎҪб№ы |
Ҫб№ы·ҙАЎИХЖЪ |
ұёЧў |
|||
|
ФРЖЪіхЙё |
ІъКұіхЙё |
°¬ЧМІЎ |
Г·¶ҫ |
ТТёО |
||||||||||||||
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ұёЧўЈәҙЛұн№©јмІв»ъ№№»тІЙСӘөгК№УГЎЈұҫұнТ»КҪБҪ·ЭЈ¬Т»·ЭУЙІЙСӘөҘО»ұЈҙжЈ¬Т»·ЭұкұҫЛНјмКұЙПҪ»јмІв»ъ№№ЎЈ
ұн 8-2 ФӨ·АФРІъёҫ°¬ЧМІЎ/Г·¶ҫ/ТТёОДёУӨҙ«ІҘГв·СјмІвөЗјЗұн
әюДПКЎ КРЎўЦЭ ПШКРЗш ТҪФә/ёҫУЧұЈҪЎФә
|
РтәЕ |
РХГы |
ДкБд |
ФРЦЬ |
ФРёҫ ұҫИЛөз»° |
СӘСщАҙФҙ |
ЛНјмөҘО» |
КХөҪұкұҫКұјд |
јмІв·Ҫ·Ё |
јмІвҪб№ы |
јмІвИЛ |
јмІвКұјд |
Ҫб№ы·ҙАЎ |
||||||
|
ФРЖЪіхЙё |
ІъКұіхЙё |
°¬ЧМІЎ |
Г·¶ҫ |
ТТёО |
°¬ЧМІЎ |
Г·¶ҫ |
ТТёО |
Кұјд |
·ҙАЎ ¶ФПу |
|||||||||
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ұёЧўЈә1ЎўҙЛұн№©јмІв»ъ№№өДКөСйКТК№УГЎЈ 2ЎўјмІвҪб№ыЈәТхРФТФЎ°ЎӘЎұЈ»СфРФТФЎ°+ЎұұнКҫЎЈ
|
ұн8-3 °¬ЧМІЎёРИҫФРІъёҫЛж·ГЗйҝцөЗјЗұн |
||||||||||||||||||||||||||
|
әюДПКЎ КРЎўЦЭ ПШКРЗшёҫУЧұЈҪЎФәЈЁЛщЈ© МоұЁКұјдЈә МоұЁИЛЈә |
||||||||||||||||||||||||||
|
ФРІъёҫұаәЕ |
РХГы |
ДкБд |
ЧЎЦ· |
өз»° |
И·ИП°¬ЧМІЎёРИҫКұЖЪ |
Д©ҙОФВҫӯ |
ФӨІъЖЪ |
ФРІъёҫПа№ШјмІв |
ФРІъёҫУГТ©Зйҝц |
·ЦГдТҪФә |
·ЦГдКұјд |
ИСЙпҪбҫЦ |
О§Іъ¶щЧӘ№й |
УӨ¶щКЗ·сФӨ·АУГТ© |
Лж·ГЗйҝц |
ЧӘҪй »ъ№№ |
ФрИОИЛ |
|||||||||
|
CD4+Пё°ы |
ІЎ¶ҫФШБҝ |
Т©ОпГыіЖ |
ҝӘКјУГТ©Кұјд |
НЈЦ№УГТ©Кұјд |
ФРЖЪ |
ІъКұ |
ІъИмЖЪ |
|||||||||||||||||||
|
өЪ1ҙО |
өЪ2ҙО |
өЪ3ҙО |
өЪ4ҙО |
өЪ1ҙО |
өЪ2ҙО |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ұёЧўЈә1ЎўҙЛұн№©ПШј¶ёҫУЧұЈҪЎ»ъ№№Лж·Г°¬ЧМІЎёРИҫФРІъёҫКұУГЎЈ2ЎўҙЛұнУл°¬ЧМІЎёРИҫФРІъёҫёц°ёҝЁЦҪЦКұЁұнТ»ІўҪЁөөұЈҙжЎЈ3ЎўИ·ИП°¬ЧМІЎёРИҫКұЖЪЈәФРЗ°И·ХпөДМоЎ°ФРЗ°ЎұЈ¬ФРЖЪИ·ХпөДМоРҙПкПёөДФРЦЬЈ¬ІъКұЎўІъәуИ·ХпөДёц°ёМоРҙЎ°ІъәуЎұ»тЎ°ІъәуЎұЎЈ4ЎўФРІъёҫПа№ШјмІвЈәЧцБЛјмІвМоЎ°ЎМЎұЈ¬ОҙЧцјмІвМоЎ°ЎБЎұЎЈ5ЎўИСЙпҪбҫЦЈәМоЎ°·ЦГдЎұЎўЎ°ЧФИ»БчІъЎұЎўЎ°ИЛ№ӨЦХЦ№ИСЙпЎұЈЁЧўГчФРЦЬЈ©ЎЈ6ЎўО§Іъ¶щЧӘ№йЈәМоЎ°»оІъЎўЎ°ЛАМҘЎўЎ°ЛАІъЎўЎ°ЖЯМмДЪЛАНцЎўЎ°І»ПкЎЈ7ЎўЛж·ГЗйҝцЈәФЪПаУҰөДЛж·ГКұЖЪМоЎ°ЎМЎұЎЈ8ЎўЧӘҪй»ъ№№ЈәЦХЦ№ИСЙпХЯЎўІъёҫІъәуВъ42Мм»тФРІъёҫБч¶ҜөҪНвөШәуОӘЖдјМРшМṩ·юОсөДТҪБЖОАЙъ»ъ№№ЎЈ9ЎўұҫұнУЙКРј¶НіТ»»гЧЬәуГҝёцФВ15ИХЗ°ЙПұЁЦБКЎј¶hnsfyamy@126.comЎЈ
|
ұн8-4 Г·¶ҫёРИҫФРІъёҫЛж·ГЗйҝцөЗјЗұн |
|||||||||||||||||||||||
|
әюДПКЎ КРЎўЦЭ ПШКРЗшёҫУЧұЈҪЎФәЈЁЛщЈ© МоұЁКұјдЈә МоұЁИЛЈә |
|||||||||||||||||||||||
|
ФРІъёҫұаәЕ |
РХГы |
ДкБд |
ЧЎЦ· |
өз»° |
И·ИПГ·¶ҫёРИҫКұЖЪ |
Д©ҙОФВҫӯ |
ФӨІъЖЪ |
ФРІъёҫУГТ©Зйҝц |
Лж·ГЗйҝц |
·ЦГдТҪФә |
·ЦГдКұјд |
ИСЙпҪбҫЦ |
О§Іъ¶щЧӘ№й |
РВЙъ¶щіцЙъКұ·ЗГ·¶ҫВЭРэМеҝ№ФӯөО¶И |
КЗ·сҪшРРФӨ·АРФЦОБЖ |
КЗ·сХп¶ПОӘПИМмГ·¶ҫ |
И·ХпОӘПИМмГ·¶ҫөДФВБд |
ЧӘҪй»ъ№№ |
ФрИОИЛ |
||||
|
өЪТ»ёцБЖіМ |
өЪ¶юёцБЖіМ |
өЪИэёцБЖіМ |
КЧҙОјмІвКұ·ЗГ·¶ҫВЭРэМеҝ№ФӯөО¶И |
ФРЖЪЛж·ГКұ·ЗГ·¶ҫВЭРэМеҝ№ФӯөО¶И |
·ЦГдЗ°»тФРНнЖЪ·ЗГ·¶ҫВЭРэМеҝ№ФӯөО¶И |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ұёЧўЈә1ЎўҙЛұн№©ПШј¶ёҫУЧұЈҪЎ»ъ№№Лж·ГГ·¶ҫёРИҫФРІъёҫКұУГЎЈ2ЎўҙЛұнГ·¶ҫёРИҫФРІъёҫёц°ёҝЁЦҪЦКұЁұнТ»ІўҪЁөөұЈҙжЎЈ3ЎўИ·ИПГ·¶ҫёРИҫКұЖЪЈәФРЗ°И·ХпөДМоЎ°ФРЗ°ЎұЈ¬ФРЖЪИ·ХпөДМоРҙПкПёөДФРЦЬЈ¬ІъКұЎўІъәуИ·ХпөДёц°ёМоРҙЎ°ІъәуЎұ»тЎ°ІъәуЎұЎЈ4ЎўФРІъёҫУГТ©ЗйҝцЈәОҙУГТ©МоЎ°ЎБЎұЈ¬УГТ©ЗлМоРҙЎ°ЎұУГТ©өДФРЦЬәНТ©ОпГыіЖЎұЎЈ5ЎўЛж·ГЗйҝцЈәЗлМоРҙ·ЗГ·¶ҫВЭРэҝ№Меҝ№ФӯөО¶ИЈ¬ОҙјмІвМоЎ°ЎБЎұЎЈ6ЎўИСЙпҪбҫЦЈәМоЎ°·ЦГдЎұЎўЎ°ЧФИ»БчІъЎұЎўЎ°ИЛ№ӨЦХЦ№ИСЙпЎұЈЁЧўГчФРЦЬЈ©ЎЈ6ЎўО§Іъ¶щЧӘ№йЈәМоЎ°»оІъЎўЎ°ЛАМҘЎўЎ°ЛАІъЎўЎ°ЖЯМмДЪЛАНцЎўЎ°І»ПкЎұЎЈ7ЎўЧӘҪй»ъ№№ЈәФРІъёҫБч¶ҜөҪНвөШәуОӘЖдјМРшМṩ·юОсөДТҪБЖОАЙъ»ъ№№ЎЈ8ЎўұҫұнУЙКРј¶НіТ»»гЧЬәуГҝёцФВ15ИХЗ°ЙПұЁЦБКЎј¶hnsfyamy@126.comЎЈ
|
ұн 8-5 °¬ЧМІЎёРИҫІъёҫЛщЙъ¶щНҜЛж·ГЗйҝцөЗјЗұн |
|||||||||||||||||||||||
|
әюДПКЎ КРЎўЦЭ ПШКРЗшёҫУЧұЈҪЎФәЈЁЛщЈ© МоұЁКұјдЈә МоұЁИЛЈә |
|||||||||||||||||||||||
|
ІъёҫұаәЕ |
ІъёҫРХГы |
¶щНҜРХГы |
ЧЎЦ·әН»§ҝЪөШЦ· |
·ЦГдТҪФә |
·ЦГдИХЖЪ |
ДёУӨЧи¶ПУГТ©Зйҝц |
Лж·Гј°ЙПұЁЗйҝц |
јмІвј°ЈЁФзЖЪЈ©Хп¶П |
HIVёРИҫЧҙМ¬ |
ЧӘҪй»ъ№№ |
ФрИОИЛ |
||||||||||||
|
Т©ОпГыіЖ |
ҝӘКјУГТ©Кұјд |
НЈЦ№УГТ©Кұјд |
1ФВБд |
3ФВБд |
6ФВБд |
9ФВБд |
12ФВБд |
18ФВБд |
ФзЖЪХп¶П |
ҝ№МејмІв |
|||||||||||||
|
6ЦЬБд |
3ФВБд |
ЖдЛы |
12ФВБд |
18ФВБд |
ЖдЛы |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ұёЧўЈә1.ҙЛұн№©ПШј¶ёҫУЧұЈҪЎ»ъ№№¶щұЈҝЖЛж·Г°¬ЧМІЎёРИҫІъёҫЛщЙъ¶щНҜКұК№УГЈЁОЮВЫКЗ·сГв·СјмІвЈ¬ЛщУР°¬ЧМІЎёРИҫІъёҫЛщЙъ¶щНҜҫщРиЛж·ГІўөЗјЗЈ©ЎЈ2ЎўҙЛұнУл°¬ЧМІЎЛж·Гёц°ёҝЁЦҪЦКұЁұнТ»ІўҪЁөөұЈҙжЎЈ3ЎўФӯФтЙПТӘЗу°¬ЧМІЎёРИҫІъёҫЛщЙъ¶щНҜј°КұҪшРРФзЖЪХп¶ПИ·ХпЎЈИзОҙҪшРРФзЖЪХп¶ПөДЈ¬ЗлМоРҙҝ№МејмІвЗйҝцЎЈ4ЎўІъёҫұаәЕУл°¬ЧМІЎЛж·Гёц°ёҝЁЙПөДұаәЕТ»ЦВЎЈ5ЎўДёУӨЧи¶ПУГТ©ЗйҝцЈ¬МоРҙ¶щНҜҝ№ІЎ¶ҫУГТ©ЗйҝцЈ¬°ьАЁТ©ОпГыіЖЎўҝӘКјУГТ©КұјдәННЈЦ№УГТ©КұјдЎЈ6ЎўјмІвј°ЈЁФзЖЪЈ©Хп¶ПЈәТхРФЎўСфРФ»тІ»И·¶ЁЎЈ7ЎўHIVёРИҫЧҙМ¬ЈәТхРФЎўСфРФ»тІ»И·¶ЁЎЈ8ЎўЧӘҪй»ъ№№ЈәОӘВъ18ФВБд¶щНҜМṩ°¬ЧМІЎҝ№ІЎ¶ҫЦОБЖөДТҪБЖ»ъ№№ЎЈ9ЎўұҫұнУЙКРј¶НіТ»»гЧЬәуГҝёцФВ15ИХЗ°ЙПұЁЦБКЎј¶hnsfyamy@126.comЎЈ |
|||||||||||||||||||||||
|
ұн 8-6 Г·¶ҫёРИҫІъёҫЛщЙъ¶щНҜЛж·ГЗйҝцөЗјЗұн |
|||||||||||||||||||||||||||
|
әюДПКЎ КРЎўЦЭ ПШКРЗшёҫУЧұЈҪЎФәЈЁЛщЈ© МоұЁКұјдЈә МоұЁИЛЈә |
|||||||||||||||||||||||||||
|
ІъёҫұаәЕ |
ІъёҫРХГы |
¶щНҜРХГы |
ЧЎЦ·әН»§ҝЪөШЦ· |
·ЦГдТҪФә |
·ЦГдИХЖЪ |
ДёУӨЧи¶ПУГТ©Зйҝц |
Лж·Гј°ЙПұЁЗйҝц |
КЗ·сПИМмГ·¶ҫёРИҫ |
ПИМмГ·¶ҫИ·ХпКұјд |
ПИМмГ·¶ҫХп¶ПТАҫЭ |
ЧӘҪй»ъ№№ |
ФрИОИЛ |
|||||||||||||||
|
Т©ОпГыіЖ |
Т©ОпјББҝ |
ЦОБЖҝӘКјКұјд |
1ФВБд |
3ФВБд |
6ФВБд |
9ФВБд |
12ФВБд |
15ФВБд |
18ФВБд |
||||||||||||||||||
|
јмІв |
Лж·Г |
јмІв |
Лж·Г |
јмІв |
Лж·Г |
јмІв |
Лж·Г |
јмІв |
Лж·Г |
јмІв |
Лж·Г |
јмІв |
Лж·Г |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ұёЧўЈә1ЎўҙЛұн№©ПШј¶ёҫУЧұЈҪЎ»ъ№№¶щұЈҝЖЛж·ГГ·¶ҫёРИҫФРІъёҫЛщЙъ¶щНҜКұК№УГЈЁОЮВЫКЗ·сГв·СјмІвЈ¬ЛщУРГ·¶ҫёРИҫФРІъёҫЛщЙъ¶щНҜҫщРиЛж·ГІўөЗјЗЈ©ЎЈ2ЎўҙЛұнУлГ·¶ҫЛж·Гёц°ёҝЁЦҪЦКұЁұнТ»ЖрҪЁөөұЈҙжЎЈ3ЎўІъёҫұаәЕУлГ·¶ҫЛж·Гёц°ёҝЁЙПөДұаәЕТ»ЦВЎЈ4ЎўДёУӨЧи¶ПУГТ©ЗйҝцЈ¬МоРҙ¶щНҜГ·¶ҫФӨ·АРФЦОБЖЗйҝц»тПИМмГ·¶ҫ¶щЦОБЖЗйҝцЈ¬°ьАЁТ©ОпГыіЖЎўјББҝәНЦОБЖҝӘКјКұјдЎЈ5ЎўЛж·Гј°ЙПұЁЗйҝцЈәёчФВБдПаУҰјмІвАёРиМоРҙГ·¶ҫјмІв·Ҫ·ЁәНјмІвҪб№ыЈЁТхРФ»тСфРФЈ©Ј¬ИфјмІв·Ҫ·ЁОӘ·ЗГ·¶ҫВЭРэМеҝ№ФӯСӘЗеС§КФСйРиұЁёжөО¶ИҪб№ыЎЈ6ЎўПИМмГ·¶ҫИ·ХпКұјдәНХп¶ПТАҫЭҪцИ·ХпОӘПИМмГ·¶ҫөД¶щНҜМоРҙЎЈ7ЎўЧӘҪй»ъ№№ЈәОӘВъ18ФВБд¶щНҜМṩПИМмГ·¶ҫЦОБЖөДТҪБЖ»ъ№№ЎЈ9ЎўұҫұнУЙКРј¶НіТ»»гЧЬәуГҝёцФВ15ИХЗ°ЙПұЁЦБКЎј¶hnsfyamy@126.comЎЈ |
|||||||||||||||||||||||||||
ұн 8-7 ФӨ·А°¬ЧМІЎ/Г·¶ҫ/ТТёОДёУӨҙ«ІҘГв·СУГТ©өЗјЗұн
әюДПКЎ КРЎўЦЭ ПШКРЗшёҫУЧұЈҪЎФәЈЁТҪФәЈ© ПоДҝГыіЖЈә
|
УГТ©Кұјд |
»щұҫЗйҝц |
УГТ©Зйҝц |
ұёЧў |
ұҫИЛЗ©Гы ЈЁја»ӨИЛЈ© |
ТҪЙъ/»ӨКҝЗ©Гы |
|||||
|
РХГы |
ДкБд |
ЧЎЦ· |
БӘПөөз»° |
Т©Ж·1 |
Т©Ж·2 |
Т©Ж·3 |
||||
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ұёЧўЈә1ЎўҙЛұнУЙЦОБЖ»ъ№№МоРҙЎЈ2ЎўЗл·ЦПоДҝМоРҙЎЈ

ЙЁТ»ЙЁФЪКЦ»ъҙтҝӘөұЗ°Ті